Классификация химических реакций
Реферат по химии ученика 11 класса средней шк.№ 653 Николаева Алексея
В качестве классификационных признаков могут быть выбраны следующие:
1. Число и состав исходных веществ и продуктов реакции.
2. Агрегатное состояние реагентов и продуктов реакции.
3. Число фаз, в которых находятся участники реакции.
4. Природа переносимых частиц.
5. Возможность протекания реакции в прямом и обратном направлении.
6. Тепловой эффект.
7. Явление катализа.
Классификация по числу и составу исходных веществ и продуктов реакции.
Реакции соединения.
При реакциях соединения из нескольких реагирующих веществ относительно простого состава получается одно вещество более сложного состава:
A + B + C = D
Как правило, эти реакции сопровождаются выделением тепла, т.е. приводят к образованию более устойчивых и менее богатых энергией соединений.
Неорганическая химия.
Реакции соединения простых веществ всегда носят окислительно-восстановительный характер. Реакции соединения, протекающие между сложными веществами, могут происходить как без изменения валентности:
СаСО3 + СО2 + Н2О = Са(НСО3)2,
так и относиться к числу окислительно-восстановительных:
2FеСl2 + Сl2 = 2FеСl3.
Органическая химия.
В органической химии такие реакции часто называют реакциями присоединения. В них обычно участвуют соединения, содержащие двойную или тройную связь. Разновидности реакций присоединения: гидрирование, гидратация, гидрогалогенирование, полимеризация. Примеры данных реакций:
to
Н2С = СН2 + Н2 → CН3 – СН3
этилен этан
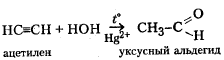
to
HC=CH + HCl → H2C=CHCl
ацетилен хлорвинил
to
n СН2=СН2 → (-СН2-СН2-)n
этилен полиэтилен
Реакции разложения.
Реакции разложения приводят к образованию нескольких соединений из одного сложного вещества:
А = В + С + D.
Продуктами разложения сложного вещества могут быть как простые, так и сложные вещества.
Неорганическая химия.
Из реакций разложения, протекающих без изменения валентных состояний, следует отметить разложение кристаллогидратов, оснований, кислот и солей кислородсодержащих кислот:
to | ||
CuSO4 5H2O | = | CuSO4 + 5H2O |
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Проведение хроматографического анализа в условиях не полностью разделенных пиков
Программа peak2Немировский А.М. При проведении хроматографического анализа часто встречаются случаи, в которых пики не полностью раздел
- Ионометрия. Метод градуировочного графика
- Ионная хроматография. Добавка электролита
Немировский А.М. В этой работе пойдет речь об эффекте, который вызывает добавка электролита в элюент. В книге А.М. Долгоносова, М.М.Сеняви
- Непредельные углеводороды ряда ацетилена (алкины)
Алкины — алифатические непредельные углеводороды, в молекулах которых между углеродными атомами имеется одна тройная связь.Углеводор
- Ионометрическое титрование
Немировский А.М.Процедура ионометрического титрования несложна. В анализируемую пробу, в которую погружены ионоселективный электрод
- Ионометрия. Метод добавок
Интерес к методу добавок в ионометрии вызывается тем, что он играет более значительную роль, чем метод добавок в других методах анализа
- Ионометрия и электродинамика
Немировский А.М.Глубокое знакомство с литературными источниками, посвященными ионометрии, выявляет фатальную склонность авторов испо
Copyright © https://www.referat-web.com/. All Rights Reserved
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

