Ионная хроматография. Добавка электролита
Немировский А.М.
В этой работе пойдет речь об эффекте, который вызывает добавка электролита в элюент. В книге А.М. Долгоносова, М.М.Сенявина, И.Н.Волощика "Ионный обмен и ионная хроматография" (Москва,"Наука",1993г.) описан случай, когда при ионообменном разделении анионов добавка электролита вызывала увеличение пика гидрокарбоната при использовании карбонатного элюента.
Для того чтобы пояснить позицию авторов книги, рассмотрим подробнее схему определения анионов. Разделение анионов проводится на анионообменной смоле, причем в качестве элюента используются растворы солей слабых кислот, таких как карбонаты, бораты и т.п. После обычной разделительной колонки ставится подавительная катионообменная. В ней происходит превращение солей разделяемых анионов в кислоты, концентрации которых затем регистрируется кондуктометрическим датчиком.
Исходя из этого, авторы книги объяснили эффект увеличения высоты пика гидрокарбоната тем обстоятельством, что угольная кислота, которая образуется после подавительной колонки, обладает меньшей электропроводностью, чем остальные кислоты. Добавка же электролита в элюент поднимает общую электропроводность раствора, что и вызывает существенное увеличение пика гидрокарбоната. Такое объяснение мне показалось не убедительным, что и привело к дополнительным исследованиям этого процесса.
Опыты проводились с ионообменником ХИКС-1. В качестве элюента использовался карбонатный раствор с добавкой нитрата натрия. Раствор готовился следующим образом. Взвешивались равные навески безводного карбоната и гидрокарбоната натрия. После растворения солей, в элюент добавлялся нитрат натрия. В итоге раствор содержал 0,005М карбонатов и 0,001М нитрата натрия. Подавительная колонка содержала смолу КУ-2. Опыты проводились на хроматографе ХПИ-1 с кондуктометрическим датчиком.
Помимо ожидаемого эффекта увеличения высоты пика гидрокарбоната в 4-5 раз, был отмечен один любопытный факт, который не был замечен авторами вышеупомянутой книги. Оказалось, что добавка электролита вызывает появление еще одного пика. Расположение пика определяется анионом электролита, т.е. если электролит содержит нитрат, то появляется пик на том месте, где обычно должен быть нитрат. Но это не обычный пик, а впадина. Кроме того, существует следующая закономерность: по мере того как от пробы к пробе возрастает содержание HCO3- , увеличивается абсолютная величина этого необычного пика.
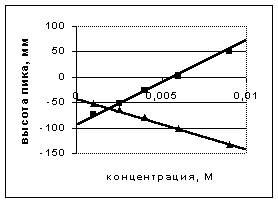
На рисунке показаны результаты калибровки хроматографа по гидрокарбонату. Прямая N1 иллюстрирует изменение высоты пиков гидрокарбоната, а прямая N2 - высоты необычных пиков нитрата. Отрицательные высоты пиков говорят о том, что вместо пиков на хроматограмме присутствуют впадины.
На основании этих результатов можно сделать вывод о том, что карбонаты можно определять не только по пику гидрокарбоната, но еще и по пику нитрата!
Попробуем объяснить наблюдаемые явления.
Рассмотрим поведение пробы в тот момент, когда она попадает на ионообменник. Поскольку ионообменный процесс основан на том, что ионы анализируемого вещества вытесняют ионы гидрокарбоната, то естественно предположить, что избыток HCO3- в пробе вытеснит ионы нитрата с поверхности смолы. Поэтому содержание ионов нитрата в подвижной фазе будет больше, чем обычно. Значит налицо повышение электропроводности элюента. Этот процесс будет наблюдаться постоянно по мере продвижения по колонке пика избытка гидрокарбоната. В конце концов, на выходе из колонки будет регистрироваться суммарный сигнал HCO3- и избытка нитрата, что вытеснил гидрокарбонат.
Развивая эту идею далее, можно объяснить появление пика нитрата. Поскольку HCO3 все время вытесняет нитрат с ионообменной смолы, то это препятствует формированию пика нитрата. Недостаток же гидрокарбоната будет вызывать усиленное поглощение нитрата смолой, что в итоге приводит к формированию пика нитрата. Таким образом, изложенная выше гипотеза наиболее полно описывает влияние добавок электролита на хроматографический процесс.
В заключение следует сказать о том, что помимо опытов с добавкой нитрат натрия, проводились эксперименты с фосфатом натрия и хлоридом калия. Результаты были аналогичны тем, что были получены с добавкой в элюент нитрата натрия.
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Непредельные углеводороды ряда ацетилена (алкины)
Алкины — алифатические непредельные углеводороды, в молекулах которых между углеродными атомами имеется одна тройная связь.Углеводор
- Ионометрическое титрование
Немировский А.М.Процедура ионометрического титрования несложна. В анализируемую пробу, в которую погружены ионоселективный электрод
- Ионометрия. Метод добавок
Интерес к методу добавок в ионометрии вызывается тем, что он играет более значительную роль, чем метод добавок в других методах анализа
- Ионометрия и электродинамика
Немировский А.М.Глубокое знакомство с литературными источниками, посвященными ионометрии, выявляет фатальную склонность авторов испо
- Ионометрическое определение хлоридов в растворах хроматов
Немировский А.М.Задача определения хлоридов в хроматных растворах пришла от гальваников. Дело в том, что в травильных ваннах необходим
- Химический метод Винклера для определения растворенного кислорода
Каверин А.В.Среди методов определения концентрации растворенного кислорода самым старым, но до сих пор не потерявшим своей актуальнос
- Химико-аналитические свойства ионов d-элементов
Ионы d-элементов 1В группыРеакции обнаружения ионов меди Сu2+Действие группового реагента H2S. Сероводород образует в подкисленных раств
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

