Синтез 4-метоксифенола
Общие сведения
Применение пара-метоксифенола
Литературный поиск. Азосоединения и диазосоединения
Диазосоединения
Ароматические диазониевые соединения
Замещение диазониевой группы водородом
Замещение диазониевой группы гидроксилом
Замещение диазониевой группы другими группами
Получение ариларсоновых и арилстибоновых кислот
Действие щелочей. Образование диазотатов
Взаимодействие солей диазония с аминами
Образование аминоазосоединений
Восстановление диазосоединений. Образование арилгидразинов
Получение 4-метоксифенола из диазосоединения
Использованная литература
Общие сведения
4-Метоксифенол (гидрохинона монометиловый эфир, пара-метоксифенол, 4-Гидроксианизол) – ромбические кристаллы (растворитель перекристаллизации - вода). Молекулярная масса: 124,14. Температура плавления (в °C): 53. Температура кипения (в °C): 243 Растворимость: бензол: легко растворим, вода: растворим, диэтиловый эфир: легко растворим, этанол: легко растворим.
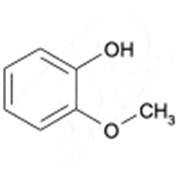
Применение пара-метоксифенола
Пара-метоксифенол широко используется в народном хозяйстве в качестве ингибитора преждевременной полимеризации полиэфирных и эпоксидных смол. Таким образом, он является незаменимым компонентом полиэфирных смол, ряда видов технических пластиков, конструкц. пластмассы, полиэфирных волокон,
Полиэфирная смола используется при ручном формовании стеклопластика и машинном изготовлении стеклопластика. Стеклопластик, полученный с применением данной полиэфирной смолы, составляет удачную конкуренцию стеклу: пропускает свет, не бьется, долговечен, может выпускаться профилем, аналогичным профилю основного кровельного материала, что исключает расходы на организацию рам. При остеклении прозрачным стеклопластиком 1/3 крыши помещения площадью 700 м2 затраты за счет экономии электроэнергии окупаются за один год.
Стеклопластиковый ламинат состоит из двух материалов, которые в сумме обладают более высокими характеристиками , нежели каждый из них в отдельности. Один из компонентов, стекловолокно, рассматривался в предыдущей главе. Второй элемент композита - смола. Наука, занимающаяся пластиками, создала такое количество различных видов смол, что остается только диву даваться, как самим химикам еще удается в них ориентироваться. Однако применительно к стеклопластиковому судостроению, мы имеем дело всего с несколькими их типами .Два вида смол, наиболее часто применяемые для постройки стеклопластиковых лодок - это эпоксидные и полиэфирные. Для начала мы уделим немного внимания эпоксидным смолам, в силу редкости их применения. Абсолютное большинство смол, использующихся в судостроении, составляют так называемые ненасыщеные полиэфирные, независимо от того, кто строит - профессионалы или любители. Именно поэтому данный тип заслуживает наиболее подробного рассмотрения.
Как эпоксидные, так и полиэфирные смолы относятся к разряду термореактивных смол. Это означает, что их отверждение происходит за счет химической реакции и впоследствии их нельзя вернуть назад в жидкое состояние путем теплового воздействия (как это возможно с термопластичными смолами). Термореактивные смолы представляют собой сиропообразные жидкости различной степени вязкости и обладают рядом специфических свойств.
До сих пор наиболее широко используемым типом смол в стеклопластиковом судостроении остаются полиэфирные. Физико-механические свойства у полиэфирных смол несколько хуже чем у эпоксидных и их химическая стойкость также ниже. Тем не менее, применительно к судостроению все эти факторы не играют решающей роли и перевешиваются сравнительной дешевизной, возможностью быстрого отверждения при комнатной температуре, простотой изготовления и легкостью в обращении. Долговременная химическая стойкость и долговечность полиэфирных смол считаются вполне достаточными для большинства стеклопластиковых лодок.
Полиэфиры - это продукты нефтехимии, берущие свое начало в ходе процесса перегонки нефти. Пускай это покажется чересчур усложненным, но мы все же опишем в общих чертах процесс их производства.
Для приготовления смолы различные ангидриды, многоосновные кислоты, гликоли и стирол получают из бензола, пропилена и этилена, затем они смешиваются вместе и "варятся" в больших емкостях до образования "базовой" смолы. В какой-то момент технологического процесса происходит разбавление базовой смолы стиролом, который составляет значительную часть полиэфирной смолы (от трети до половины конечного продукта). После разбавления смолы стиролом она готова к продаже, необходимо только внести добавки, определяемые спецификой сферы применения конкретной смолы. Естественно, производитель способен играть составом смолы. Он может добавлять в нее различные наполнители, акселераторы и прочие модификаторы, что приводит к появлению множества самых разных полиэфирных смол. Большое значение при этом имеет сфера применения конечного продукта, в чем мы далее убедимся.
Если бы обрисованный выше процесс приготовления полиэфирной смолы был доведен до своего конца, в результате мы получили бы полностью отвержденную массу. Но поскольку мы фактически прерываем этот процесс на полпути, смола оказывается лишь частично полимеризованной. Отгруженная на этой стадии смола хранит в себе запущенную в ходе "варки" реакцию и через достаточный промежуток времени неизбежно перейдет в твердое состояние сама по себе. Именно поэтому приобретать и использовать следует только свежую смолу, старая смола не обладает необходимыми свойствами уже только оттого, что зашла слишком далеко в своей естественной полимеризации. Большинство производителей смол поступает правильно, давая гарантию свежести товара у себя и своих дистрибьюторов. Как правило, срок годности полиэфирной смолы составляет всего шесть месяцев, хотя при надлежащих условиях хранения год или даже два не являются чем-то из ряда вон выходящим. Срок можно продлить и более, если хранить смолу в холодильнике (не замораживая). Смола должна храниться в сухом прохладном месте, куда не попадают прямые солнечные лучи и где температура не слишком превышает +20 градусов.
Полиэфирные смолы относятся к веществам, для которых воздух является ингибитором. Это означает, что поверхность смолы, контактирующая с воздухом, не отверждается (по крайней мере, полностью). Даже когда смола перейдет в твердое состояние, ее поверхность по-прежнему будет оставаться липкой. Чтобы дать смоле возможность полного отверждения и избавиться от липкости, ее надо изолировать от воздуха. Этого можно добиться двумя способами.
Как правило, приобретается специальная смола, содержащая в составе изолирующую добавку, которой обычно является воск. Как только смола наносится, повышение ее температуры в ходе экзотермической реакции заставляет воск всплыть на поверхность, перекрыть доступ воздуха и дает смоле возможность встать. Такие полиэфирные смолы с содержанием воска относятся к отделочным, т.к. используются в заключительном слое всего изделия. Немного погодя мы расскажем о том, как самим изготовить такую смолу.
Второй способ отверждения предполагает изоляцию поверхности от воздуха после нанесения смолы при помощи какого-либо вида пленочного покрытия. Это может быть, к примеру, материал типа целлофана или майлара (тот и другой именуют разделительными пленками); изолирующий слой можно создать, нанося сверху поливиниловый спирт (PVA) при помощи краскопульта. Все эти методы изоляции, однако, ограничиваются небольшими участками и годятся лишь в случае ремонта. Для отверждения заключительного слоя стеклопластика большинству любителей следует использовать смолу с содержанием воска.
Смолы, не содержащие восковой добавки, как упомянутые выше отделочные, относятся к конструкционным. Таким образом, конструкционные смолы не содержат воска. Отделочные смолы содержат воск.
На всем протяжении процесса постройки, за исключением последних слоев, должна использоваться конструкционная смола. Причина этого заключается в том, что стеклопластик представляет собой неоднородный материал, о чем зачастую многие не в курсе. Стеклопластик – это набор слоев стекловолоконного армирования, каждый из которых пропитан смолой и приклеен к соседнему. Можно построить полную аналогию с листом фанеры и ее склееными слоями шпона.
Поверхности слоев ламината, пропитанных конструкционной смолой, сохраняют липкость в процессе набора толщины и обеспечивают прочную связь с последующими слоями. Эти связи называют промежуточными. Если бы для целей ламинирования использовалась отделочная смола, для обеспечения адгезии слоев всплывающий к поверхности воск необходимо было удалять перед каждым последующим слоем, и существует только два способа, как это сделать.
Во-первых, воск с поверхности можно попытаться смыть или стереть растворителем типа ацетона. Однако данный метод , по крайней мере в отношении больших площадей, имеет такой минус, что по ходу процесса воск накапливается и больше размазывается вокруг. Второй, и наиболее эффективный метод - удалить воск шлифованием. При ламинировании будет крайне утомительным делом, если каждый новый слой необходимо будет подвергать такой обработке перед укладкой последующего. Поэтому наш вам совет – в первую очередь использовать конструкционную смолу, чтобы процесс ламинирования можно было вести непрерывно. При этом будет обеспечена надежная промежуточная связь слоев, которая в случае применения отделочной смолы всегда была бы под вопросом. К вощеной поверхности смола просто не клеится.
Литературный поиск. Азосоединения и диазосоединения
Диазосоединения
В число диазосоединений, в широком понимании этого термина, включаются диазосоединения жирного ряда общей формулы RCHN2, а также такие соединения, у которых один из атомов азота диазогруппы присоединен к циклическому или гетероциклическому ядру. Последнему типу диазосоединений соответствует общая формула RN2X. Целесообразным является рассмотрение обоих типов диазосоединений в отдельности.
Ароматические диазониевые соединения
Действие азотистой кислоты на холодный водный раствор анилина и его гомологов в присутствии умеренного избытка разбавленной минеральной кислоты ведет к образованию солей диазония, например хлористого арилдиазония R(Сl)N≡N. Такие соли могут быть при определенных условиях выделены в виде твердых кристаллических продуктов, не растворимых в эфире, и более или менее легко растворимых в воде. Хлористые и азотнокислые соли имеют в водных растворах нейтральную реакцию и ионизированы приблизительно в такой же степени, как и соответственные аммониевые соли. В растворах хлористых или сернокислых солей можно обычными реакциями обнаружить наличие хлор- или сульфат-иона. Анион соли можно реакцией обменного разложения заменить другим анионом, если растворимость солей благоприятствует подобной реакции. Таким путем были, например, получены трудно растворимые диазониевые соли хромовой, железосинеродистой, пикриновой и вольфрамовой кислот.
Кроме того, по этому же способу были получены, исходя из хлористого бензоил-р-аминофенилдиазония, кристаллические углекислая и азотистокислая соль. При действии цианистого калия и сернистокислых солей на соли диазония наблюдается другое течение реакции. При действии платинохлористоводородной кислоты или хлорного золота в соляной кислоте на соли диазония образуются соответственные хлорплатинаты или хлораураты. Кроме того, известен ряд других двойных солей фенилдиазония или его гомологов, например комплексные соли с SnCl2 состава D2.SnCl4 с сулемой состава D.HgCl2, с цианистым серебром состава D•Ag(CN)2 (D — обозначает арилдиазоний RN2—).
Комплексные соединения, образующиеся из солей диазония и солей тяжелых металлов, были в последние годы широко изучены рядом наших исследователей с целью выяснения возможности их использования для получения металлорганических соединений.
Галоидные соли диазония способны к образованию полигалоидных солей и в этом свойстве можно усмотреть аналогию с перйодидами аммония; при действии бромной воды на хлористый или бромистый фенилдиазоний образуется пербромид состава С6Н5N2IВr2. Описаны также другие соли подобного типа, например С6Н5N2ClI2, С6Н5N2ICl2 и др. Диазониевые соединения, поскольку они являются солями, напоминают по своим свойствам соли аммония и тетрааммониевых оснований. Сходство с солями четвертичных аммониевых оснований выражается кроме того в способности к образованию сильнощелочных растворов гидратов окиси диазония при действии влажной окиси серебра на хлористый арилдиазоний. Подобного рода гидраты окиси диазония являются нестойкими и поэтому не могут быть выделены в свободном состоянии. Измерения электропроводности их водных растворов показали, что гидраты окиси диазония являются сильными основаниями, так как их константы электролитической диссоциации лежат между константами едких щелочей и аммиака. При нейтрализации гидратов окиси диазония кислотами образуются соли диазония.
Эта реакция может быть использована для ацидиметрического титрования этих солей при применении, метилоранжа в качестве индикатора. Соли диазония являются соединениями нестойкими; многие из них разлагаются в водных растворах при температуре выше 5°. В сухом состоянии многие из них взрывают, что особенно наблюдается в случае содержания некоторых определенных анионов. Например, азотнокислый фенилдиазоний очень чувствителен к удару и при нагревании взрывает с исключительной силой. Пикраты и хромовокислые соли тоже чувствительны к удару и сильно взрывают. Применение хромовокислых солей диазония в качестве взрывчатых веществ было запатентовано. Имеются указания, что перхлорат фенилдиазония даже во влажном состоянии взрывает при трении.
Наиболее важные реакции солей диазония связаны с диазогруппой. При определенных условиях группу диазония можно заменить самыми различными группами, например —Вг, —С1, —J, —CN, —CNS, —CNO, —NO2, арилом и др. Подобного рода реакции широко применяются для получения замещенных ароматических углеводородов. Кроме того, большое значение имеют также другие реакции солей диазония: при их восстановлении образуются арилгидразины, при взаимодействии с аминами и фенолами образуются замещенные азосоединения, окисление их ведет к получению нитраминов.
Замещение диазониевой группы водородом
Один из наиболее ранних способов, примененных для замещения диазогруппы водородом, состоит в кипячении диазониевой соли со спиртом. Впоследствии было установлено, что при этом образуются также в большем или меньшем количестве жирноароматические эфиры. При нагревании сернокислого фенилдиазония с метиловым спиртом образуется анизол с 70%-ным выходом, наряду с небольшим количеством бензола. Следовательно, взаимодействие солей диазония со спиртами может протекать в двух направлениях.
1. 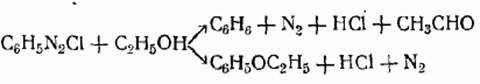
Многочисленные детальные исследования этой реакции привели к выводу, что основными факторами, от которых зависит относительное количество образующихся двух продуктов, являются характер заместителей в ароматическом ядре и природа спирта. В общем можно отметить, что при применении метилового спирта образуется больше эфира, чем при работе с другими спиртами. Вообще для низших спиртов жирного ряда было установлено, что количество образующегося эфира уменьшается с увеличением молекулярного веса спирта; при кипячении сернокислого фенилдиазония с этиловым спиртом выход жирноароматического эфира составляет 60%, с пропиловым спиртом — 50%, а в случае кипячения с амиловым спиртом брожения выход эфира снижается до 30%. При наличии в бензольном ядре некоторых заместителей (галоидов, нитрогрупп, карбоксильных групп) количество образовавшегося продукта замещения диазогруппы водородом повышается за счет снижения выхода эфира. Этот факт имеет большое значение, так как это единственная реакция, при которой возможно отщепление группы диазония у нитропроизводных солей диазония без восстановления нитрогруппы.
Прибавление щелочи, алкоголята натрия или цинковой пыли к спиртовому раствору соли диазония способствует замещению диазониевой группы водородом. При этом образуется, кроме того, заметное количество дифенила.
Замещение диазониевой группы водородом может быть также осуществлено при применении других методов, как-то: действием щелочного раствора соли двухвалентного олова, или же при действии фосфорноватистой кислоты.
Замещение диазониевой группы гидроксилом
При нагревании водного раствора сернокислого фенилдиазония образуется фенол. Та же реакция наблюдается и в случае других арилдиазониевых солей:
![]()
Для получения фенолов, по этому способу рекомендуется применять сульфаты диазония, а не хлористые или азотнокислые соли, так как в этих случаях процесс, хотя и идет в указанном направлении, сопровождается образованием и других продуктов. Из хлористого арилдиазония в присутствии избытка соляной кислоты, прибавленной при диазотировании, образуется заметное количество. Хлорзамещенных фенолов, а из азотнокислой соли образуется большое количество нитрофенолов. Ниже приводятся примеры, служащие для иллюстрации этого способа замены диазониевой группы гидроксилом Успешность описанного способа получения фенолов находится в зависимости от стойкости исходных солей диазония в водном растворе. Соли диазония, получающиеся из анилина и его гомологов, разлагаются очень легко с образованием соответствующих фенолов. Наличие нитрогруппы или галоидов в ароматическом ядре обычно повышает стойкость диазониевой группы. Например, водный раствор хлористого 2,4,6-трихлор-фенилдиазония можно кипятить, но образования фенола при этом не происходит. То же наблюдается и для сернокислого 2,4,6-трибромфенилдиазония. Некоторые соли диазония, получающиеся из аминоантрахинонов, являются чрезвычайно стойкими и могут быть перекристаллизованы из горячей воды.
При этом способе получения фенолов может встретиться осложнение, состоящее в том, что сравнительно стойкие диазосоединения могут сочетаться с фенолом по мере его образования. Например, из диазотированной нафтионовой кислоты образуется а-нафтол-4-сульфоновая кислота, всегда несколько загрязненная азопродуктом. Для устранения этих затруднений было предложено видоизменение способа получения фенолов из сравнительно стойких солей диазония. Этот метод состоит в нагревании концентрированного раствора соли диазония с серной кислотой такой концентрации, чтобы смесь кипела при 50°. Хотя в отдельных случаях, например из солей 2,6-дибромфенилдиазония, были получены удовлетворительные результаты, все же метод не приводит к хорошим результатам при более стойких солях диазония, что, без сомнения, объясняется стабилизирующим действием умеренно разбавленной серной кислоты на подобные соли. Более удобным способом получения фенолов из стойких солей диазония является нагревание последних с разбавленной серной кислотой и сернокислым натрием до 135—145°. По этому же способу можно также получить, хотя и с плохим выходом, трихлор- и трибромфенолы из соответствующих солей диазония. Кроме того, метод оказался пригодным для получения 2,5-дихлорфенола, 2,4-дибромфенола, 3-хлор-р-крезола, 3-бром-р-крезола и 3,5-дибром-р-крезола из соответственных арилдиазониевых солей25.
При действии кислоты на соль арилдиазония, содержащую в о-положении метильную группу, может наблюдаться и другое направление реакции. Например, при осторожном нагревании диазотированного 4-нитро-о-толуидина образуется смесь 4-нитро-о-крезола и 4-нитроиндазола. То же наблюдается и для диазониевых солей, полученных из 5-нитро-4-амино-т-ксилола. Наличие параллельной реакции, протекающей наряду с основной, было также установлено в случае обработки диазониевых солей, получающихся из мезидина, о-толуидина или 4-амино-т-ксилола, разбавленным раствором щелочи. Однако при этих условиях продукт реакции содержал азосоединение, получившееся в результате сочетания диазониевой соли с образовавшимся в процессе реакции индазолом хлором или бромом, так как для этой цели имеются более совершенные методы. С другой стороны, этот метод вполне пригоден для получения ароматических йодзамещенных путем прибавления йодистого натрия к раствору соли диазония, содержащему избыток минеральной кислоты.
Введение азидной группы в ароматическое ядро осуществляется прибавлением азида натрия к кислому раствору соли: диазония. Этот метод применялся для получения моно-, ди- и триазидопроизводных ароматических углеводородов. Для замещения диазониевой группы хлором или бромом удобнее всего применять способ Зандмейера или Гаттермана. Реакция Гаттермана применяется для замещения диазониевой группы хлором, бромом, группой — CNO,—CN и др. Способ состоит в прибавлении медной бронзы или порошка меди к раствору соответственной соли диазония. Ниже приводится пример, иллюстрирующий применение этого способа. Введение хлора или брома в ароматическое ядро при помощи реакции Зандмейера заключается в прибавлении раствора однобромистой или однохлористой меди в какой-либо кислоте к раствору соли диазония и в последующем нагревании смеси. По этой же реакции при применении цианистой меди в растворе цианистого калия или роданистой меди в растворе роданистого калия можно диазониевую группу заменить группой — CN или — CNS.
Замещение диазониевой группы другими группами
Замещение арильными радикалами. Неоднократно наблюдалось, что при проведении описанных выше реакций замещения диазониевой группы образуется большее или меньшее количество производных дифенила. В особенности это отмечается для солей нитрофенилдиазония; например, при действии однохлористой меди на диазотированный о-нитранилин в условиях реакции Зандмейера образуется лишь немного о-хлорнитробензола, а основным продуктом реакции является 2,2'-дииитродифенил. Такое же явление наблюдается и при хлористых диазониевых солях, полученных из m-нитранилина, 5-хлор-2-нитранилина, 3-нитро-р-толуидииа, 2-нитро-р-толуидина, 6-нитро-о-толуидина, 5-нитро-о-толуидина, 4-нитро-о-толуидина; замещение диазониевой группы хлором в этих случаях является только второстепенной реакцией. Выход образующихся при этом производных дифенила всецело зависит от условий опыта. Однако при тщательном регулировании условий реакции 3андмейера можно добиться очень хорошего выхода т-нитрохлорбензола из m-нитранилина.
Некоторые соли диазония, для которых реакция Зандмейера протекает нормально, дают производные дифенила при действии цинковой пыли, порошка меди или порошка железа в спиртовой среде. В этих условиях из водного раствора сульфата фенилдиазония выделяется дифенил, из диазотированного β-нафтиламина — β,β'-динафтил.При этой реакции образуется заметное, количества продукта, который не гонится с водяным паром. Этот продукт состоит, главным образом, из дифенилбензола (I), дидифенила (II) и дидифенилбензола (III). Выход этих высших углеводородов повышается, если реакция проводится в уксусной кислоте, содержащей некоторое количество муравьиной кислоты.
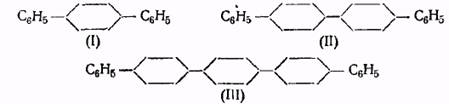
Описанный способ получения дифенила через диазониевые соли был применен для интересного синтеза фенантрена и его производных. При прибавлении порошка меди к водному раствору диазониевой соли, полученной из а-фенил-о-аминокоричной кислоты, происходит отщепление диазогруппы и соединение между собой фенильных групп с образованием фенантренкарбоновой кислоты.
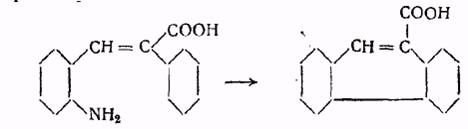
Эта реакция была применена для синтеза и других производных фенантрена.
Интрамолекулярная конденсация этого типа наблюдается также при нагревании диазониевых солей, получающихся из некоторых замещенных о-аминобензофенонов. Из о-оксипроизводных замещенных бензофенонов получаются в качестве побочных продуктов флуореноны.
Другой способ получения дифенила и его производных основан на взаимодействии диазоангидрида с ароматическими углеводородами. Если к смеси р-нитрофенилдиазотата натрия и бензола прибавить уксусную кислоту в количестве, достаточном для выделения свободного диазоангидрида, образуется с хорошим выходом р-нитродифенил
![]()
Впоследствии этот способ в несколько видоизмененном виде был применен для получения большого числа производных дифенила. Однако этот процесс сопровождается другими реакциями, приводящими к замене диазониевой группы водородом и к образованию азосоединений. Способ работы ясен из приводимого примера. По этому способу дифенил был также получен взаимодействием фенилдиазотата натрия с бензолом, но выход достигал лишь 11%. Если вместо бензола ввести в реакцию тиофен, образуется соответственно фенилтиофен. В реакцию вступают также нитробензол, образующий с фенилдиазотатом натрия 4-нитродифенил, бромбензол и бензонитрил. В качестве исходных продуктов можно применять соли диазония, получающиеся из хлор- или броманилинов, толуидинов, нитранилинов, т- и р-аминобензонитрила, р-аминодифенила. К сожалению, выходы при применении этих продуктов невысоки и обычно составляют 10—40% от теоретических. Вопрос о механизме этой реакции освещается в работе Грив и Хей.
Дифенил и его производные можно также получить прибавлением сухого хлористого арилдиазония к ароматическому углеводороду, например бензолу или нафталину, смешанному с некоторый количеством безводного хлористого алюминия. Таким образом при взаимодействии хлористого фенилдиазония с бензолом образуется дифенил, а с нафталином — смесь а- и р-фенилнафталинов. Этот способ был использован также для получения фенилпиридина и фенилхинолина, причем в этих случаях отпадала необходимость прибавления хлористого алюминия
![]()
Замещение диазониевой группы нитрогруппой. Такое замещение наблюдается при действии закиси меди и азотистой кислоты на раствор нитрата арилдиазония. Кроме того, для этой же цели можно воспользоваться и другим способом, заключающимся в прибавлении порошка меди к водному раствору или суспензии двойной соли азотнокислого диазония с азотистокислой окисью ртути или в действии избытка азотистокислого калия и суспензии солей меди на соль диазония Замещение диазониевой группы остатком сернистой кислоты. Процесс в общих чертах состоит в насыщении раствора сернокислого диазония в разбавленной серной кислоте сернистым газом и в последующем прибавлении порошка меди. Этот способ был применен с успехом для получения фенилсульфиновой кислоты и большого количества ее гомологов, а также галоидо- и алкоксизамещенных. В некоторых случаях, например, исходя из m-толуидина, по этому способу, получается сульфиновая кислота лишь с плохим выходом. Томас ввел изящное видоизменение способа выделения сульфиновых кислот, состоящее в осаждении их в виде солей окиси железа из кислого раствора.
Эта соль при действии раствора едкого натра превращается в растворимую натриевую соль фенилсульфиновой кислоты с выделением осадка гидрата окиси железа. При подкислении полученного раствора выделяется свободная сульфиновая кислота, которую можно экстрагировать эфиром.
Получение ариларсоновых и арилстибоновых кислот
Замещение диазониевой группы группой — АsО3Н2 обычно осуществляется действием мышьяковистокислого натрия в щелочном растворе на соли диазония Получение тиофенолов, ароматических сульфидов и дисульфидов из солей диазония. Общий способ получения тиофенолов из солей диазония был предложен Лейкартом. Способ состоит в смешивании охлажденных льдом растворов хлористого диазония с ксантогеновокислым калием в эквимолекулярном соотношении. При последующем нагревании образуется эфир этилксантогеновой кислоты, из которого при омылении спиртовой щелочью выделяется тиофенол.
![]()
При действии сернистых солей щелочных металлов на растворы солей диазония образуются соответствующие сульфиды и дисульфиды; иногда при этом получаются также тиофенолы. Этот способ дает хорошие результаты в особенности для получения дисульфида из диазотированной антраниловой кислоты.
Действие щелочей. Образование диазотатов
При прибавлении раствора фенилдиазония к избытку холодного концентрированного водного раствора едкого кали выделяется калиевая соль состава С6Н5N2ОК. Если при этом, не допускать повышения температуры смеси, свежеприготовленная соль способна сочетаться с β-нафтолом. Если же калиевую соль нагреть с избытком едкого кали, способность ее сочетаться с β-нафтолом исчезает, хотя при подкислении соляной кислоты снова образуется хлористый диазоний. Это указывает на существование двух изомерных калиевых солей состава С6Н5N2ОК, отличающихся по отношению к β-нафтолу. Эти соли не являются производными гидрата окиси диазония, так как при действии уксусной кислоты на одну из изомерных солей выделяется диазогидрат С6Н5N2ОH, обладающий кислыми свойствами и растворимый в эфире. Из другой соли при этом образуется диазоангидрид (С6Н5N2)2О. Калиевым солям приписывают строение С6Н5N:NОK, допускающее по теории Гантцша-Вернера существование двух стереоизомерных форм/
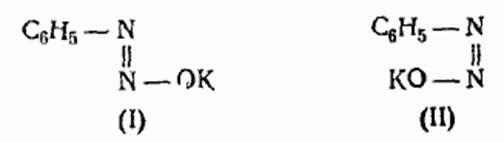
Конфигурацию (II) приписывают лабильной калиевой соли, которая сочетается с -нафтолом и превращается при нагревании со щелочью в стереоизомерную форму (I). Возможно, что в свете работ последнего времени о стереоизомерных формах оксимов окажется правильным другое представление о пространственном расположении изомерных калиевых солей. Вместо часто применяемого обозначения син- и анти- для различения обоих стереоизомеров было предложено ввести для этой цели обозначение лабильной и стабильной форм. Аналогично описанным двум стереоизомерным формам калиевых солей существуют два пространственных изомера цианистых солей, образующихся при смешении солей диазония с концентрированным водно-спиртовым раствором цианистого калия при —10°. Образующиеся таким способом диазоцианиды являются окрашенными веществами, трудно растворимыми в воде. По свойствам они резко отличаются от истинных цианистых солей диазония, получающихся при упаривании смеси гидрата окиси диазония с синильной кислотой и представляющих, как и цианистые соли щелочных металлов, бесцветные вещества, растворимые в воде. Лабильные диазоцианиды способны сочетаться β-нафтолом, но при хранении они постепенно теряют эту способность, причем переход в стабильную форму сопровождается, кроме того, повышением температуры плавления продукта.
При нагревании диазотата со щелочью до 130° он теряет способность сочетаться с β-нафтолом и превращается в стабильную соль. Из хлористого р-нитрофенилдиазония можно получить стойкий диазотат при более низкой температуре. При подкислении обеих стереоизомерных солей минеральными кислотами образуется соль диазония, при прибавлении же уксусной кислоты проявляется различие свойств обеих солей. Из лабильной формы при этом образуются диазоангидриды — окрашенные, взрывчатые твердые вещества, которые в результате гидролиза в щелочной среде превращаются в диазотаты. Из стабильных же диазотатов образуются диазогидраты C6H5N:NOH, растворимые в органических растворителях, например эфире, бензоле, хлороформе. При взбалтывании эфирного раствора с водной щелочью они переходят в водный слой в результате образования диазотатов. В водном растворе, а также в хлороформе или бензоле они, по-видимому, с различной скоростью изомеризуются в первичные нитрозамины.
![]()
При взаимодействии солей диазотатов с йодистыми алкилами образуются вторичные нитрозамины, с галоидангидридами кислот — нитрозоанилиды. При взбалтывании хлористого бензоила со щелочным раствором фенилдиазотата натрия образуется нитрозобензанилид. При действии уксусного ангидрида на щелочной раствор р-толилдиазотата натрия образуется нитрозоацетат-р-толуидид:
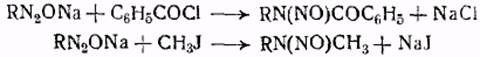
В связи с легкостью превращения диазотатов в нитрозосоединения интересно отметить, что при окислении диазосоединений в щелочной среде образуются нитрамины.
![]()
Взаимодействие солей диазония с аминами
Образование диазоаминосоединений. Присоединение солей диазония к первичным или вторичным аминам ведет к образованию в качестве первичного продукта реакции диазоаминосоединения.
![]()
Реакция протекает очень легко с вторичными аминами жирного ряда и осуществляется прибавлением нейтрального раствора соли диазония к водному раствору амина при 0°. Первичные алифатические амины, за исключением бензиламина, вступают в реакцию с образованием бисдиазоаминосоединений типа RN(N2C6H5)2. В некоторых случаях при определенных экспериментальных условиях удается получить продукт, содержащий значительное количество монодиазоаминосоединения.
Реакция с первичными ароматическими аминами может протекать в обоих направлениях, но обычно сопровождается образованием монодиазоаминосоединения. Операция заключается в смешении концентрированного раствора соли диазония с водным раствором солянокислой соли соответственного амина и в последующем прибавлении уксуснокислого натрия. Аналогичный процесс может быть также осуществлен прибавлением раствора соли диазония к спиртовому или уксуснокислому раствору амина с последующим добавлением уксуснокислого натрия.
При соблюдении описанных условий из некоторых первичных ароматических аминов может получиться значительное количество изомерного аминоазосоединения. Этот процесс наблюдается в особенности в случае применения аминопроизводных нафталина, из которых образуется почти исключительно аминоазосоединение. Из алкилариламинов, у которых водород в р-положении не замещен, легче получается аминоазосоединение, чем диазоаминосоединение. Из m-фенилендиамина образуется аминоазосоединение. Наличие заместителей в бензольном ядре сказывается на легкости образования или на выходе аминоазосоединений. Подробное освещение этого вопроса можно найти в работе Моргана и Миклтуйта, в которой проводятся ссылки на более ранние исследования. При получении диазоаминосоединений можно иногда встретиться еще с большим осложнением, состоящим в том, что образующийся продукт обладает другим строением. Например, при взаимодействии диазотированного р-нафтиламина с 4-т-ксилидином образуется т-ксилил-4-азо-β-нафтиламин. Такое направление реакции, по-видимому, объясняется обменным разложением амино- и диазогрупп — процессом, неоднократно наблюдавшимся в случае солянокислых солей аминов и солей диазония. При смешении водных растворов диазосульфаниловой кислоты и р-толуидина образуется некоторое количество сульфаниловой кислоты и хлористого р-толилдиазония.
Образование бисдиазоаминосоединений из ароматических аминов происходит при действии солей диаз
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Синтез бензальанилина
Федеральное агентство по образованиюГосударственное образовательное учреждениевысшего профессионального образования«САМАРСКИЙ Г
- Физико-химические закономерности формирования тонкопленочных металлополимерных систем из газовой фазы
- Физико-химические основы адсорбционной очистки воды от органических веществ
Объем потребляемой в мире воды достигает 4 трлн. м3 в год, а преобразованию со стороны человека подвергается практически вся гидросфера.
- Физико-химические основы хроматографического процесса
- Физико-химические свойства йода и его соединений
Йод открыт французским химиком Куртуа в 1811 году, он относится к VII группе периодической системы Д.И. Менделеева. Порядковый номер элемен
- Синтез диэтилового эфира малоновой кислоты. Свойства и основные методы получения сложных эфиров
Федеральное агентство по образованиюГосударственное образовательное учреждение высшего профессионального образованияСамарский го
- Синтез замещенных пирролов
Федеральное агентство по образованиюМосковская государственная академиятонкой химической технологииим. М.В. ЛомоносоваФакультет: Био
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

