Амины
.
Аминами называются органические производные аммиака, в котором один, два или все три атома водорода замещены на углеводородные радикалы ( предельные, непредельные, ароматические).
Название аминов производят от названия углеводородного радикала с добавлением окончания –амин или от названия соответствующего углеводорода с приставкой амино-.
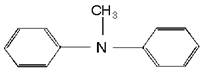 Примеры:
Примеры:
CH3 – NH2 CH3 – NH – C2H5
метиламин метилэтиламин мтилдифениламин
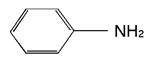
фениламин
(анилин)
В зависимости от числа атомов водорода, замещенных в аммиаке на углеводородные радикалы, различают первичные, вторичные и третичные амины:
R
![]()
R- NH2 R – NH – R’ R – N – R”
первичный амин вторичный амин третичный амин
Где R, R’, R’’ – углеводородные радикалы.
Первичные, вторичные и третичные амины можно получить, проводя алкилирование (введение алкильного радикала) аммиака. При этом происходит постепенное замещение атомов водорода аммиака на радикалы, и образуется смесь аминов:
NH3 + CH3I --- CH3NH2 + HI
CH3NH2 + CH3I --- (CH3)2NH + HI
(CH3)2NH + CH3I --- (CH3)2N + HI
Обычно в смеси аминов преобладает один из них в зависимости от соотношения исходных веществ.
Для получения вторичных и третичных аминов можно использовать реакцию аминов с галогеналкилами:
(CH3)2NH + C2H5Br --- (CH3)2NC2H5 + HBr
Амины можно получить восстановлением нитросоединений. Обычно нитросоединения подвергают каталитическому гидрированию водородом:
C2H5NO2 + 3H2 --- C2H5NH2 + 2H2O
Этот метод используется в промышленности для получения ароматических аминов .
Предельные амины. При обычных условиях метил амин CH3NH2, диметиламин (CH3)2NH, триметиламин (CH3)3N и этиламин C2H5NH2 – газы с запахом, напоминающим запах аммиака. Эти амины хорошо растворимы в воде. Более сложные амины – жидкости, высшие амины – твердые вещества.
Для аминов характерны реакции присоединения, в результате которых образуются алкиламиновые соли. Например, амины присоединяют галогеноводороды:
(CH3)2NH2 +HCl --- ((CH3)2NH3)Cl
хлорид этиламмония
(CH3)2NH + HBr --- ((CH3)2NH2)Br
бромид диметиламмония
(CH3)3N + HI --- ((CH3)3NH)I
иодид триметиламмония
Тритичные амины присоединяют галогенопроизводные углеводорода с образованием тетраалкиламмониевых солей, например:
(C2H5)3N + C2H5I --- ((C2H5)4N)I
Алкиламониевые соли растворимы в воде и в некоторых органических растворителях. При этом они диссоциируют на ионы:
((C2H5)4N)I === ((C2H5)4N)+ + I-
В результате водные и неводные растворы этих солей проводят электрический ток. Химическая связь в алкиламмониевых соединениях ковалентная, образованная по донорно-акцепторному механизму:
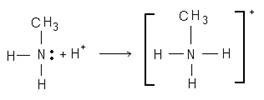
Ион метиламмония
Как и аммиак, в водных растворах амины проявляют свойства оснований. В их растворах появляются гидроксид-ионы за счет образования алкиламониевых оснований:
C2H5NH2 + H2O === (C2H5NH3)+ + OH-
Щелочную реакцию растворов аминов можно обнаружить при помощи индикаторов.
Амины горят на воздухе с выделением CO2, азота и воды, например:
4(C2H5)2NH + 27O2 --- 16CO2 + 2N2 + 22H2O
Первичные, вторичные и третичные амины можно различить, используя азотную кислоту HNO2. при взаимодействии этой кислоты с первичными аминами образуется спирт и выделяется азот:
CH3 – NH2 + HNO2 --- CH3 – OH + N2 +H2O
Вторичные амины дают азотистой кислотой нитрозосоединения, которые имеют характерный запах:
CH3 – NH2 – CH3 + HNO2 --- (CH3)2 – N==NO+H2O
Третичные амины не реагируют азотистой кислотой.
АнилинC6H5NH2 является важнейшим ароматическим амином. Он представляет собой бесцветную маслянистую жидкость, которая кипит при температуре 184,4 0 С.
Анилин был впервые получен в XIX в. русским химиком-органиком Н. Н. Зининым, который использовал реакцию восстановления нитробензола сульфидом аммония (NH4)2S. В промышленности анилин получают каталитическим гидрированием нитробензола с использованием медного катализатора:
C6H5 – NO2 + 3H2 -cu-- C6H5 – NH2 + 2H2O
Старый способ восстановления нитробензола, который потерял промышленное значение, заключается в использовании в качестве восстановителя железа в присутствии кислоты.
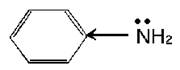 По химическим свойствам анилин во многом аналогичен предельным аминам, однако по сравнению с ними является более слабым основанием, что обусловлено влиянием бензольного кольца. Свободная электронная пора атома азота, с наличием которой связаны основные свойства, частично втягивается в П – электронную систему бензольного кольца:
По химическим свойствам анилин во многом аналогичен предельным аминам, однако по сравнению с ними является более слабым основанием, что обусловлено влиянием бензольного кольца. Свободная электронная пора атома азота, с наличием которой связаны основные свойства, частично втягивается в П – электронную систему бензольного кольца:
Уменьшение электронной плотности на атоме азота снижает основные свойства анилина. Анилин образует соли лишь с сильными кислотами. Например, с хлороводородной кислотой он образует хлорид фениламмония:
C6H5NH2 + HCl --- (C6H5NH3)Cl
Азотная кислота образует с анилином диазосоединения:
C6H5 – NH2 + NaNO2 +2HCl --- (C6H5 – N+==N)Cl- + NaCl + 2H2O
Диазосоединения, особенно ароматические. Имеют большое значение в синтезе органических красителей.
Некоторые особые свойства анилина обусловлены наличием в его молекуле ароматического ядра. Так, анилин легко взаимодействует в растворах с хлором и бромом, при этом происходит замещение атомов водорода в бензольном ядре, находящихся в орто- и пара-положенияхк аминогруппе:
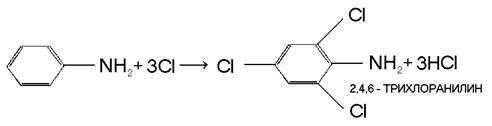
Анилин сульфируется при нагревании с серной кислотой, при этом образуется сульфаниловая кислота:
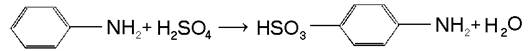
Сульфаниловая кислота – важнейший промежуточный продукт при синтезе красителей и лекарственных препаратов.
Гидрированием анилина в присутствии катализаторов можно получить циклогексиламин:
C6H5 – NH2 + 3H2 --- C6H11 – NH2
Анилин используется в химической промышленности для синтеза многих органических соединений, в том числе красителей и лекарств.
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Ампульное производство гентамицина сульфата
- Анализ и технологическая оценка химического производства
- Анализ лекарственной формы состава: Rp.: Amidopyrini 0,3 Dibazoli 0,02
- Аналитические весы
СОСТОЯНИЕ ИЗУЧЕННОСТИ ВОПРОСА Идея создания электронных лабораторных весов аналитичес-кого класса точности (до 0.0001 г) возникла после п
- Аргон инертный газ
Общие сведения об открытиях благородных газов К благородным газам относятся гелий, неон, аргон, криптон, ксенон и радон. По своим свойств
- Ароматичні вуглеводні
Опорний конспектна тему:"Ароматичні вуглеводні"Виконав:учень 10 - А класусередньої школи № 96Коркуна Дмитро1. Ненасичені вуглеводні –
- Атомизаторы и источники возбуждения в аналитической химии
Сдано на химфаке ДГУ на ''5''Источники возбуждения и атомизации в спектральном анализе Атомизацию, как источник возбуждения, используют в
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

