Синтез этилового спирта
1 Литературный обзор
1.1 Методы получения
1.1.1 Получение этилового спирта сбраживанием пищевого сырья
1.1.2 Гидролиз древесины с последующим брожением
1.1.3 Получение этилового спирта из сульфитных щёлоков
1.1.4 Сернокислотный способ гидратации этилена
1.2 Направления использования
1.3 Источники сырья
2 Физико-химические основы процесса
2.1 Механизм процесса
2.2 Кинетика и термодинамика процесса
2.3 Влияние основных параметров на скорость процесса
2.3.1 Температура
2.3.2 Влияние давления
2.3.3 Концентрация исходных веществ (реагентов)
2.3.4 Влияние мольного соотношения воды и этилена
2.3.5 Катализаторы
2.4 Методы выделения продукта из реакционной смеси
3 Технологическая часть
3.1 Описание принципиальной технологической схемы производства
3.1.1 Отделение гидратации этилена
3.1.2 Отделение ректификации водно-спиртового конденсата
3.1.3 Катализаторное отделение
3.2 Основное и вспомогательное оборудование, его характеристика и обслуживание
3.2.1 Реактор и колонные аппараты
3.2.2 Теплообменная аппаратура
3.2.3 Емкостное оборудование
3.2.4 Оборудование катализаторного отделения
3.2.5 Компрессоры и насосы
3.2.6 Вспомогательное оборудование
3.3 Характеристика сырья и продукта
4 Расчётная часть
4.1 Материальные расчёты и составление материального баланса процесса
4.2 Тепловые расчёты и составление теплового баланса процесса
4.3 Термодинамический расчёт
5 Отходы и их обезвреживание
6 Мероприятия по технике безопасности, промсанитарии, пожарной безопасности и охране труда
6.1 Характеристика производства по взрыво- и пожароопасности
6.2 Свойства сырья и вспомогательных материалов
6.3 Основные правила работы с токсичными газами и едкими веществами
6.4 Основные правила пожарной безопасности
Заключение
Список использованных источников
Приложения
Произвести технологический расчёт процесса производства синтетического этилового спирта.
Данные
производительность – 12 тонн в час;
состав этиленовой фракции: этилен – 75%, этан – 25%;
соотношение Н2О : С2Н4 = 0,65 :1 ,
степень превращения по этилену - 94%;
в побочные продукты – 6%.
Введение
Этилен СН2=СН2, пропилен СН2=СН=СН2, бутилен СН3-СН2-СН=СН2, бутадиен (дивинил) СН2=СН-СН-СН2 будучи очень реакционноспособными соединениями, играют важную роль в промышленности органического синтеза. Из многочисленных реакций, в которые вступают олефины, наибольшее практическое значение имеют процессы полимеризации (полиэтилен, полипропилен, полиизобутилен, и др.), гидратации (спирты), хлорирования (дихлорэтан, хлористый аллил и т.п.), окисления (окись этилена),оксосинтеза и некоторые другие реакции. Широкое распространение получили процессы гидратации олефиновых углеводородов. Таким способом получаются этиловый, изопропиловый, и другие спирты. Этиловый спирт (этанол, метилкарбинол, винный спирт) С2Н5ОН, мол.в. 46,07 - важнейший представитель предельных одноатомных спиртов. Этиловый спирт - бесцветная, легко подвижная жидкость со жгучим вкусом и характерным запахом;т. кип. 78,3° С; т. затв. —112°С; плотность 0,789 г/см3; границы взрывоопасных концентраций этилового спирта в воздухе 3,28 - 18,95 об.%; предельно допустимая концентрация паров этилового спирта в воздухе 1000 мг/м. Этиловый спирт смешивается в любых соотношениях с водой, спиртами, эфиром, глицерином, бензином и др. Органическими растворителями, горит бесцветным пламенем.
Этиловый спирт по объему производства занимает первое место среди всех других органических продуктов. Он широко применяется как растворитель и как исходное соединение для различных синтезов. Особенно большие количества этилового спирта расходуются в производстве синтетического каучука. Этиловый спирт используется также как исходный продукт для производства хлораля, этилацетата, диэтилового эфира и многих других продуктов органического синтеза.
1 Литературный обзор
1.1 Методы получения
Этиловый спирт может быть получен одним из следующих методов: брожением пищевого сырья (зерна, картофеля и др.), а также отходов сахарного производства – мелассы; гидролизом растительных материалов, переработкой сульфитного щелока, гидратацией этилена. Наибольшее значение имеют получение этилового спирта гидратацией этилена и сбраживанием сельскохозяйственного сырья и продуктов его переработки.
1.1.1 Получение этилового спирта сбраживанием пищевого сырья
Сущность спиртового брожения состоит в том, что виноградный сахар (глюкоза) С6Н1206 в присутствии вещества, вызывающего брожение, через ряд стадий превращается вэтиловый спирт и двуокись углерода:
зимаза (дрожжи)
С6Н1206 2С2Н5ОН + 2С02
В промышленности для получения спирта пользуются не природным виноградным сахаром, а крахмалом картофеля, хлебных злаков, отходами сахарных заводов. Крахмал предварительно осахаривают под действием особого энзима — диастаза, находящегося в солоде (проросших зернах ячменя или ржи). Осахаривание идет с присоединением воды к крахмалу; при этом образуется дисахарид — мальтоза С12Н22О11:
диастаз (солод)
![]() m(С6Н10О6) + 0,5mН2О 0,5m(C12H22O11)
m(С6Н10О6) + 0,5mН2О 0,5m(C12H22O11)
В процессе брожения под влиянием энзима мальтоза гидролизуется в глюкозу:
мальгаза (дрожжи)
С12Н22О11 + Н20 2С6Н12Ов
мальтоза глюкоза
Глюкозу потом подвергают спиртовому брожению. Мальтаза, как и зимаза, вырабатывается быстроразмножающимися дрожжевыми грибками.
Основными видами пищевого сырья для получения этилового спирта являются картофель и зерновые культуры.
Пищевое сырье вначале очищают от пыли, грязи и механических примесей, оболочку толстокожурного зерна разрушают на вальцах, жерновах или других приспособлениях, после чего очищенный материал разваривают острым паром под давлением в течение 45-110 мин (в зависимости от вида сырья); при этом к зерну прибавляют воду. После разваривания массу выпускают через выдувное отверстие разваривающего аппарата; при этом происходит перепад давления от 4-5 ат до 0,2-0,5 ат (избыточных), вследствие чего оболочки клеток разрываются и сырье превращается в однородную жидкую массу, поступающую в заторный чан. В этот же чан для осахаривания крахмала вводят ферментативный препарат - солод, который получают из проращенного в особых условиях зерна (ячменя, ржи, проса). После добавления солода массу выдерживают 10-15 мин при 61 для ее стерилизации, а также растворения и осахаривания крахмала. По окончании осахаривания массу охлаждают до 30, после чего в нее вводят дрожжи. Полученную массу охлаждают до 22-26 град. (двухсуточное брожение) или 15-18 град. (трехсуточное брожение) и перекачивают в бродильные чаны. Кроме этилового спирта при брожении образуются: глицерин, янтарная кислота, метиловый спирт, сивушные масла, сложные эфиры и др. Длительность брожения при непрерывном методе составляет 60-65 часов, содержание э.с. в зрелой бражке 8-10об.%. Бражка поступает в брагоперегонный аппарат, из которого отгоняют этиловый спирт и летучие примеси. Остающийся в аппарате твердый продукт - барда (4,5-7,4%), используется на корм скоту. Крепость получаемого при перегонке спирта-сырца должна быть не менее 88% (объемн.) Из спирта-сырца очисткой его от примесей получают спирт-ректификат (95,5%). На рис.1 приведена схема производства этилового спирта из пищевого сырья, включающая процессы разваривания и осахаривания крахмала.
1.1.2 Гидролиз древесины с последующим брожением
Древесина состоит из целлюлозы, гемипеллюлозы (пентозаны и гексозаны) и лигнина. В составдревесины входят также минеральные вещества (зола), смолы и жиры, дубильные вещества и т. д. На целлюлозу приходится около половины массы древесины.
Для получения спирта древесину обрабатывают (гидролизуют) серной или соляной кислотой. При этом из целлюлозы образуется глюкоза
(С6Н10О5)х + хН2О хС6Н12О6
целлюлоза глюкоза
которая затем проходит стадию спиртового брожения. При гидролизе концентрированной (41%-ной) соляной кислотой получается раствор, содержащий до 30% сахаров. Однако этот способ из-за сильной коррозии оборудования, а также трудностей при получении и регенерации 41%-ной соляной кислоты не нашел широкого развития.J
Распространение в промышленности получил гидролиз древесины разбавленной серной кислотой. По этому методу древесные опилки обрабатывают в соединенных последовательно аппаратах (перколяторах) 0,1— 0,4%-ной H2S04 при 7—15 кгс/см2 и 150—170°С. Получаемый 4%-ный раствор сахара выпаривают, нейтрализуют гашеной известью и после фильтрования сбраживают. Внедрен также гидролиз 0,4%-ной серной кислотой в трубчатых аппаратах непрерывного действия при нагревании паром под давлением 25—30 кгс/см2.
Наряду с этиловым спиртом на гидролизных заводах получают ценные побочные продукты — фурфурол, метиловый спирт, уксусную кислоту, скипидар, белковые дрожжи, лигнин и т. д. Из 1 т древесных опилок можно получить до 200 кг гидролизного спирта (в расчете на 100%-ный).
1.1.3 Получение этилового спирта из сульфитных щёлоков
Этиловый спирт, получаемый на предприятиях целлюлозно-бумажной промышленности при сульфитной варке целлюлозы, принято называть сульфитным спиртом.
При сульфитном способе выделения чистой целлюлозы большие количества древесной щепы обрабатывают при повышенной температуре раствором бисульфита кальция или магния, содержащим некоторый избыток свободного сернистого ангидрида. Жидкость, оставшуюся после обработки щепы, называют сульфитными щелоками. Это — отход целлюлозно-бумажного производства. На каждую тонну вырабатываемой целлюлозы получается 8—12 кг сульфитных щелоков, содержащих 10— 12% сухого вещества (лигнин, углеводороды, белки, смолы, жиры, окись кальция и др.). Примерно 25% сухого. вещества относится к сахарам, причем 2/3 из них способны сбраживаться, давая этиловый спирт.
Из щелоков острым паром отгоняют сернистый ангидрид и другие летучие вещества, затем нейтрализуют щелок известковым молоком и направляют его в батарею бродильных чанов, где щелок последовательно перетекает из одного чана в другой. Брожение проводят при 30 °С в течение примерно 20 ч при .интенсивном перемешивании щелока с дрожжами. По окончании брожения дрожжи отделяют в сепараторах от сахарного раствора (бражки). Бражка получается слабой (около 1% спирта). Ее подвергают ректификации с получением 95%-ного этанола.
1.1.4 Сернокислотный способ гидратации этилена.
В 1873 г. А.М. Бутлеров и В. Горяинов детально изучили сернокислотную гидратацию этилена и предсказали техническое значение этого процесса. В начале 30-х годов в Советском Союзе М. А. Далиным с сотр. были проведены исследования сернокислотной гидратации олефинов, а в 1936 г. в г. Баку была создана первая в СССР промышленная установка по получению этанола из нефтяных газов.
Концентрированная серная кислота способна реагировать с этиленом, образуя моно- и диалкилсульфат:
С2H4 + H2S04 С2H5OSO2OH
моноалкилсульфат
2С2Н4 + H2S04 (C2H6О)2SО2
Диалкилсульфат
Эти эфиры при взаимодействии с водой превращаются в этиловый спирт, выделяя кислоту:
С2H5OSO2OH + Н2О C2H5OH + H2SО4
(С2H5О)2SO2 + 2H2О 2С2H5OH + H2SО4
При этом методе можно использовать достаточно разбавленные газы (содержащие всего 30—40% этилена), что позволяет упростить процессы газоразделения. Содержание высших олефинов в газе должно быть минимально, так как они под действием серной кислоты полимеризуются с образованием нежелательных смолистых веществ.
Ниже приводится описание принципиальной технологической схемы процесса. Газ при 25 кгс/см2 и 80 °С подают в нижнюю часть колонны (абсорбера), орошаемой 96—98%-ной серной кислотой. Абсорбер представляет собой освинцованную и футерованную изнутри колонну; в ней имеется 15—20 ферросилидовых тарелок с колпачками для барботирования газа и с трубами для перелива жидкости. Температура абсорбции поддерживается 70°С за счет снятия реакционного тепла трубчатыми холодильниками, имеющимися на каждой тарелке. По трубкам холодильников пропускают холодную воду. Отходящие из абсорбера газы, содержащие примерно 90% этана и 4—6% этилена, дросселируют до 10 кгс/см2, отмывают водой от унесенной кислоты, нейтрализуют 5—10%-ным раствором щелочи, вновь промывают и направляют на пиролиз этана в этилен. Из нижней части абсорбера выводится смесь моно- и диэтилсульфата с непрореагировавшей серной кислотой. Смесь охлаждают до 50 °С и после дросселирования до 5— 6 кгс/см2 направляют в специальный аппарат (гидролизер) для гидролиза водой, отделенной при ректификации этилового спирта.
При гидролизе кроме этилового спирта образуются диэтиловый эфир, полимеры и т. д. Газы, выделяющиеся при дросселировании жидкости, отмывают, нейтрализуют и присоединяют к газам, идущим на пиролиз этана. Гидролиз проводят при 4,5—5 кгс/см2 и 92—96 °С. Вытекающая из нижней части гидролизера жидкость состоит из этилового спирта, воды, серной кислоты, диэтилового эфира и негидролизованного этилсульфата. Эта смесь поступает в отпарную колонну, в нижнюю часть которой вводят острый пар для завершения гидролиза и отгонки спирта и эфира. Отпарку в кубе ведут при 125 °С и —1,5 кгс/см2. Из куба отпарной колонны отводят 47%-ную серную кислоту, которую после очистки от смолистых веществ направляют на концентрирование.
Парогазовая смесь из верхней части отпарной колонны, содержащая пары воды, этилового спирта, диэтиловогоэфира и кислоты, этан и этилен, поступает в нейтрализационно-отпарную колонну. Барботируя через щелочной раствор, смесь нейтрализуется и далее промывается водой; поступающей с верха колонны. В куб этой колонны подают острый пар для отгонки паров спирта из стекающего в куб щелочного раствора. Нейтрализованные пары, отходящие из верхней части колонны, конденсируются в холодильниках и направляются на ректификацию в очистную колонну. В этой колонне происходит разделение эфира и спирто-водного конденсата. Эфир дополнительно отмывают водой от спирта и направляют в ректификационную колонну. С верха этой колонны отводится товарный эфир. Количество его составляет ^10% от количества спирта-ректификата.
Кубовый продукт колонны разделяют на следующей ректификационной колонне на спирт и воду, используемую на стадии гидролиза. Кубовый продукт очистной колонны также проходит ректификацию; в результате получают товарный спирт-ректификат.
Экономичность данного процесса определяется в первую очередь методом концентрирования серной кислоты. Обычно концентрирование проводят в две стадии: упаривание до 88—93%-ной концентрации дымовыми газами в барабанных концентраторах и добавление олеума с доведением концентрации кислоты до требуемой. Для уменьшения потерь кислоты при упаривании и для предотвращения выделения ее паров в окружающий воздух из газов, выходящих из концентрационных аппаратов, улавливают тумансерной кислоты на мокрых электрофильтрах в электрическом поле высокого напряжения. Сернокислотный конденсат из электрофильтров вновь поступает в производство. Недостатками метода являются большой расход серной кислоты, необходимость применения кислотостойкого оборудования и недостаточная селективность процесса.
В то же время был разработан новый способ получения этанола – прямая гидратация этилена, который не требовал использования серной кислоты, что позволяло исключить одну из стадий процесса, сделав его тем самым более экономичным. Более того, прямая гидратация позволяет получить более высокий выход продукта и отличается высокой экологичностью.
Прямая гидратация этилена имеет ряд преимуществ перед сернокислотным методом: исключение расхода серной кислоты и минимальные потребности в других реагентах, кроме этилена и водяного пара, одностадийность процесса, более высокий выход спирта. Недостатками прямой гидратации является частая замена катализатора и использование более дорогих концентрированных этиленовых фракций. Процесс синтеза этилового спирта прямой гидратацией этилена технически более прогрессивен, чем сернокислотной гидратацией, поэтому он получил значительно большее распространение в промышленности. Характерной особенностью процесса прямой гидратацией этилена является низкая конверсия исходного сырья – порядка 5% за один проход. Таким образом, для полного использования этилена он должен быть пропущен через систему 18-20 раз.
1.2 Направления использования.
Этиловый спирт широко применяется в различных отраслях промышленности:
Пищеваяпромышленность (главный потребитель спирта).
· ликероводочная промышленность
· производство бальзамов, настоек
· консервная промышленность
· виноделие
· производство уксусной кислоты
· кондитерская промышленность.
Парфюмерная промышленность (более 85% парфюмерной продукции содержит раствор спирта).
Фармацевтическая промышленность (40% всех лекарственных препаратов приготовлено с использованием этилового спирта).
Медицина
· дезинфекция инструментария
· процедуры
Химическая промышленность
· производство синтетического спирта
· производство эфиров, этилена, этила
· производство растворителей, политуры
· производство искусственного волокна
· производство лаков и красок
· производство стекла
· производство антифриза
· производство носителей информации (аудио-,видео-фотопленка)
· производство синтетического каучука, ацетальдегида, хлороформа, этилацетата и др. органических продуктов
· производство взрывчатых веществ
· производство топлива для реактивных двигателей и др.
Радиоэлектронная промышленность
· обслуживание приборов
· производство микросхем
Кожевеннаяпромышленность
· дубление кожи
Таким образом, спиртовое производство тесно связано, с одной стороны, со многими отраслями, в которых спирт служит сырьем, основным и вспомогательным материалом, с другой - с сельским хозяйством. Оно является единственным производством, способным превращать дефектные (порченые) зерно и картофель и другие материалы в доброкачественные продукты.
1.3 Источники сырья
Исходным сырьем при получении спирта из пищевых материалов являются
растительные продукты, содержащие углеводы: моно- или дисахариды, главным образом глюкозу и сахарозу, а также полисахариды – крахмал. Позже стали применять древесную целлюлозу, которая гидролизом превращается в глюкозу.
Непосредственно сбраживанию с образованием этилового спирта подвергаются только моносахариды, поэтому сахар или крахмал под влиянием ферментов, содержащихся в дрожжах, превращаются в моносахариды:
![]() С12Н22О11 + 2 Н2О С6Н12О6 + С6Н12О6
С12Н22О11 + 2 Н2О С6Н12О6 + С6Н12О6
сахар глюкоза фруктоза
2(С6Н10О5) + 2x Н2О →xС12Н22О11 2x С6Н12О6
![]() крахмал дисахарид глюкоза
крахмал дисахарид глюкоза
Процесс брожения с образованием этилового спирта
![]() С6Н12О6 2С2Н5ОН + 2 СО2
С6Н12О6 2С2Н5ОН + 2 СО2
происходит под влиянием бактерий. Наряду с этиловым спиртом в небольшом количестве получаются высшие спирты.
Глюкоза может быть получена и из древесной целлюлозы гидролизом. Гидролиз осуществляется при действии концентрированной соляной кислоты (41% -ной) или разбавленной серной кислоты (0,4 % -ной) при 150-170º С и 15-30 ат:
![]() (С6Н10О5) + x Н2О x С6Н12О6
(С6Н10О5) + x Н2О x С6Н12О6
Таким образом, сырьем для производства технического этилового спирта могут быть крахмалосодержащие вещества ( различные виды зерна, картофель) или сахаросодержащие продукты (сахарная свекла, сахарный тростник и отходы от производств сахара). При производстве гидролизного этилового спирта исходным сырьем являются отходы деревообрабатывающих заводов – опилки.
При производстве синтетического этилового спирта сырьем служит этилен, который получается при пиролизе газового сырья или нефтяных дистилляторов. Для получения этилового спирта этилен подвергается сернокислотной или прямой гидратации на твердых фосфорнокислых катализаторах:
+H2SO4 +H2O
C2Н5OSO3 H C2H5OH + H2 О
СН2 =СН2 — +H2O
C2H5OH
H3PO4
Трудовые затраты при производстве этилового спирта из пищевых продуктов или древесных опилок очень велики, поэтому значительно выгоднее исходить из дешевого углеводородного сырья и получать спирт гидратацией этилена.
2 Физико-химические основы процесса.
2.1 Механизм процесса.
Присоединение воды к олефинам всегда происходит по правилу Марковникова. Поэтому первичный спирт можно получить только из этилена; из других олефинов получаются вторичные или третичные спирты.
Прямой гидратацией этилена называется обратимый экзотермический процесс непосредственного (без образования промежуточных продуктов) присоединения воды к этилену в присутствии катализатора с образованием этилового спирта:
СН2=СН2 + Н2 С2H5OH + 10,55 ккал
Катализатором процесса служит ортофосфорная кислота на шариковом носителе — силикагеле. Реакция предположительно протекает в четыре стадии:
1) физическое растворение этилена в пленке кислоты;
2) образование иона карбония:
![]()
![]() С2Н4 + H+ C2H5+
С2Н4 + H+ C2H5+
3) взаимодействие иона карбония с водой с образованием иона алкоксония:
![]()
![]() C2H5+ + Н2О C2H5О+Н2
C2H5+ + Н2О C2H5О+Н2
4) разложение иона алкоксония на спирт и протон:
![]()
![]() C2H5О+Н2 C2H5ОН+ Н+
C2H5О+Н2 C2H5ОН+ Н+
Активность катализатора в течение цикла его пробега постепенно снижается из-за уноса ортофосфорной кислоты с проходящим через реактор потоком продуктов. Во избежание коррозии оборудования унесенной кислотой ее нейтрализуют; с этой целью в парогазовый поток после реактора впрыскивают подщелоченный водно-спиртовый конденсат.
Степень превращения этилена за один проход через реактор составляет 3,5—4,8%. Непрореагировавший этилен возвращается в реактор (рециркулирует), пары воды и спирта конденсируются в системе теплообменников и холодильников, а циркулирующий газ при этом охлаждается. Водно-спиртовый конденсат отделяют от циркулирующего газа в сепараторах и направляют на ректификацию. Из всего количества этилена, вступившего вреакцию, только 95—98,5% превращается в спирт, а остальное — в диэтиловый эфир, ацетальдегид, полимеры. С целью повышения степени превращения этилена в спирт поддерживают высокую концентрацию этилена в циркулирующем газе (90% масс, и более). При этом необходимо, чтобы концентрация этилена в свежей этиленовой фракции, поступающей с газоразделительной установки, была равна 99% (масс).
При ректификации водно-спиртового конденсата из него получают 93—94%-ный спирт. Из выделенного концентрированного спирта удаляют небольшие количества ацетилена.
2.2 Кинетика и термодинамика процесса.
Рассмотрим равновесие основной реакции: гидратации - внутримолекулярной дегидратации:
![]()
![]() Н2С=СН2 + Н2О Н2СОН – СН3
Н2С=СН2 + Н2О Н2СОН – СН3
Она протекает с выделением тепла, следовательно ее равновесие смещается вправо при понижении температуры. Дегидратации, наоборот, способствует нагревание. Равновесие невыгодно для гидратации олефинов, так как при 150-300о С, когда катализаторы процесса достаточно активны, DGо имеет большую положительную величину и равновесие смещено в сторону дегидратации. При этом для олефинов разного строения различия в термодинамике рассматриваемых реакций незначительны. Как показывает стехиометрия реакций, на их равновесие можно влиять, изменяя давление. Внутримолекулярной дегидратации, идущей с увеличением числа молей веществ, способствует пониженное или обычное давление. Наоборот, гидратации олефинов (в том числе и этилена) благоприятствует высокое давление, увеличивающее равновесную степень конверсии олефина. Так, последняя при 250-300о С и атмосферном давлении составляет всего 0,1-0,2%, что совершенно неприемлемо для практических целей, но при 7-8 Мпа и тех же температурах она возрастает до 12-20 %. Зависимость равновесной степени конверсии этилена при его гидратации от давления и температуры изображена на рис.2, причем аналогичные кривые характерны и для других олефинов. Очевидно, что гидратации способствует одновременное снижение температуры и повышение давления.
Рассмотрим теперь равновесие в системемежмолекулярная дегидратация спиртов - гидролиз простых эфиров:
![]()
![]() 2ROH ROR + Н2О
2ROH ROR + Н2О
В случае этанола ее равновесие описывается уравнением
![]()
показывающим, что оно смещается вправо при снижении температуры. Следовательно, при 200-400о С внутри- и межмолекулярная дегидратация конкурируют друг с другом. Термодинамическим методом регулирования направления этих реакций является изменение давления: на образование простого эфира оно не влияет, но получению олефина его снижение благоприятствует.
В ряде случаев роль воды более сложная. Так, фосфорная кислота, нанесенная на пористый носитель, образует на его поверхности жидкую пленку, которая абсорбирует воду из газовой фазы. При каждых данных температуре и парциальном давлении водяных паров в газовой фазе устанавливается фазовое равновесие, и фосфорная кислота в пленке имеет определенную концентрацию и соответствующую ей каталитическую активность. Последняя падает при снижении температуры и росте парциального давления воды, что ограничивает выбор этих параметров для каждого случая определенными рамками.
2.3 Влияние основных параметров на скорость процесса.
2.3.1 Температура.
Реакцию прямой гидратации этилена желательно проводить при невысоких температурах. Однако практически выбор температуры лимитируется скоростью реакции и активностью применяемых катализаторов.С повышением температуры, при прочих равных условиях, равновесная степень превращения этилена в спирт снижается. Однако при низких температурах активность фосфорнокислотного катализатора очень мала. Так, степень конверсии этилена при 280-290о С достигает лишь 4-5%, а при более низких температурах она еще меньше.На практике процесс прямой гидратации в паровой фазе в присутствии фосфорнокислотного катализатора ведут в интервале 260-300о С.
С повышением температуры до 290 °С скорость гидратации этилена возрастает. Дальнейшее повышение температуры до 320 °С сопровождается незначительным снижением степени конверсии этилена в этиловый спирт; кроме того, при этом резко возрастает выход побочных продуктов. Зависимость текущей производительности реактора по спирту (Gcп) оттемпературы (Т, К) в верхней части аппарата описывается эмпирическим уравнением:
![]()
где а,, с– коэффициенты, зависящие от активности катализатора и от технологических параметров процесса. Каждому моменту времени соответствует оптимальная температура, обеспечивающая максимальные текущую и суммарную производительность аппарата при минимальной себестоимости спирта. Отклонение температуры от оптимальной на 5°С приводит к снижению производительности реактора на 5%; при этом соответсвенно возрастает расход пара, электроэнергии и катализатора на 1 т спирта. Оптимальная температура (Т, К) верха реактора, в соответствии с литературными данными, определяется по формуле:
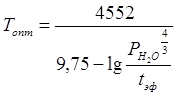
где Рн2о — парциальное давление паров воды в реакторе, кгс/см2; tэф - эффективное время реакции, с. Использование этого уравнения для регулирования температуры верха аппарата осложняется трудностью определения tэфдлякаждого момента работы реактора.
2.3.2 Влияние давления.
Повышение давления благоприятствует реакции гидратации, причем оптимальное давление составляет 6,7-8 Мпа . Это давление связано с процессом абсорбции этилена фосфорной кислотой. Оптимальное парциальное давление водяных паров равно 2,7-3 Мпа ; оно и определяет мольное соотношение водяных паров и этилена. Оптимальное парциальное давление этилена составляет 3,5-3,7 Мпа. Общее давление складывается из парциальных давлений воды, этилена и примесей. При концентрации этилена в циркулирующем газе 80-85% общее давление системы получается равным 7-8 Мпа.
2.3.3 Концентрация исходных веществ (реагентов).
Повышение концентрации этилена в циркулирующем газе при постоянной циркуляции способствует повышению производительности реактора и снижению расхода пара, электроэнергии и катализатора на 1 т спирта. В то же время для поддержания более высокой концентрации этилена в газе необходимо увеличивать долю газа, выводимого из системы для удаления инертных примесей, а это отрицательно влияет на себестоимость спирта. Оптимальной концентрацией этилена в циркулирующем газе является 90-92% (об.). повышение концентрации этилена сверх 93% (об.) нецелесообразно, так как это значительно увеличивает себестоимость спирта.
![]()
2.3.4 Влияние мольного соотношения воды и этилена.
Согласно термодинамическим данным, с увеличением отношения Н2О : С2Н4 c 0,5 :1 до 1 : 1 значительно повышается степень конверсии олефина. Однако экспериментальные данные отличаются от термодинамических: с увеличением отношения Н2О : С2Н4 до 0,7-0,75 степень конверсии этилена действительно возрастает, но при дальнейшем его увеличении она снижается.
Установлено также, что от соотношения Н20 : С2Н4 зависит и активность катализатора гидратации. Оптимальная концентрация фосфорной кислоты в жидкостной пленке на пористом носителе составляет 83-85%. Эта величина зависит от парциального давления водяного пара, которое определяется общим давлением в системе и мольным отношением вода : этилен. Оптимальная концентрация Н3РО4 наблюдается при соотношении Н2О : С2Н4 = 0,75:1. С дальнейшим ростом этого соотношения возрастает количество воды в пленке, уменьшается концентрация кислоты и снижается степень конверсии этилена. Поэтому в промышленных условиях принято мольное соотношение Н2О : С2Н4=(0,6-0,7) : 1.
2.3.5 Катализаторы
Промышленные катализаторы должны удовлетворять ряду требований, предъявляемых технологией. Катализаторы должны быть активными к данной реакции, возможно более стойкими к действию контактных ядов, сравнительно дешевыми, обладать высокой механической прочностью, термостойкостью, определенной теплопроводностью и т.п. Поэтому применяемые на практике катализаторы редко являются индивидуальными веществами и, как правило, представляют собой сложные механические смеси, называемые контактными массами. В состав контактной массы входят в основном три составные части: собственно катализатор, активаторы и носители.
Носителями называются термостойкие инертные пористые вещества, на которые тем или иным способом наносят катализатор. Использование носителей преследует как технологические, так и экономические цели. Во-первых, при этом создается пористая контактная масса с богато развитой внутренней активной поверхностью, увеличивается ее механическая прочность и термостойкость, во-вторых экономится дорогой катализатор (платина, никель, пятиокись ванадия и т.п.). В некоторых случаях сами носители могут быть активаторами. К типичным носителям катализаторов относятся силикагель, алюмосиликат, асбест, пемза, кизельгур, уголь, каолин, некоторые соли.
Поскольку любой каталитический процесс протекает на поверхности контактной массы, скорость и глубина такого процесса во многом определяется величиной поверхности катализатора. Одной из основных характеристик контактных масс является величина удельной поверхности Sуд. ,т.е. поверхность единицы веса или объема катализатора. Для большинства промышленных катализаторов Sуд составляет от нескольких десятков до нескольких сотен м2 / г. Чтобы обеспечить столь высокую удельную поверхность, контактные массы должны быть материалами с высокой пористостью. Мелкие поры, пронизывая зерно контактной массы, создают внутреннюю поверхность, которая, как правило, в несколько сотен раз больше ее наружной поверхности.
В производстве этанола прямой гидратацией этилена наиболее широкое применение получил фосфорнокислотный катализатор на твердом носителе.
Катализаторы прямой гидратации не должны разрушаться под действием влаги, поэтому такой катализатор, как фосфорная кислота на кизельгуре, неприменим - он не имеет скелета и легко разрушается. В качестве носителя для фосфорной кислоты применяют силикагель или алюмосиликат. Чаще всего используют шариковый широкопористый силикагель, обработанный водяным паром с целью снижения удельной поверхности и подавления побочных реакций уплотнения.
Носитель пропитывают 65 %-ной фосфорной кислотой и сушат при 100о С. Готовый катализатор содержит 35-40% Н3РО4 85 %-ной концентрации.
В условиях реакции фосфорная кислота, осажденная на носителе, растворена в пленке воды, адсорбированной на поверхности пор, и реакция фактически протекает в жидкой пленке фосфорной кислоты. Кислотный катализ, таким образом ,сводится к гомогенному катализу в жидкостной пленке катализатора.
Существенными недостатками фосфорнокислотного катализатора являются его коррозионная агрессивность и постепенный унос кислоты с поверхности носителя. Эти недостатки могут быть полностью устранены при использовании нейтральных катализаторов - вольфрамовых и кремневольфрамовых.
Разработаны процессы гидратации этилена на нейтральном катализаторе в жидкой фазе при 250-300о С и 30 Мпа и при 300о С и 14 Мпа. В этих случаях процесс ведут в колонне высокого давления, где на тарелках помещен катализатор - оксиды вольфрама на силикагеле (15-20 % WO3 ). Этилен и воду подают в верхнюю часть колонны, а снизу отводят 10 %-ный спирт. В этом процессе не требуется расходовать большое количество тепла на испарение воды и перегрев водяного пара.
Разработаны и другие активные вольфрамовые катализаторы, содержащие 40-60% триоксида вольфрама на широкопористом силикагеле типа SiO2·12WO3·7Н2О с добавкой борной кислоты. Катализаторы этого типа готовят, пропитывая силикагель раствором вольфрамата аммония и прокаливая затем при 400о С . Они не нуждаются в последующем восстановлении. Добавление в состав катализатора 5-10% борной кислоты существенно повышает его активность. Наиболее активный катализатор, содержащий 60% WO3 и 5% В2О3 на силикагеле, применяется в интервале 200-240о С и 1,5-2,5Мпа, т.е. в более мягких условиях- при конверсии 5,5%.
Вольфрамовые катализаторы более активны, чем фосфорнокислотные, и могут работать в более мягких условиях. Однако они значительно дороже, ибо вольфрам - дефицитный материал, поэтому такие катализаторы не нашли широкого промышленного прим
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Синтез этилового эфира 4-бромбенозойной кислоты
Цель работы состоит в составление литературного обзора по спиртам и синтеза этилового эфира 4-бромбензойной кислоты.Спиртами называютс
- Синтез, свойства и применение дифениламина. Амины и их свойства
Общие сведенияПрименение дифениламинаОбзор литературы. Амины1. Общие реакции. Образование солей2. Ацилирование и алкилирование аминовА
- Синтетические ювелирные камни
СодержаниеВведение. 2Глава 1. Основные методы выращивания синтетических ювелирных камней. 4Глава 2. Синтетические корунды.. 8Глава 3. Синте
- Скорость химической реакции
- Совершенствование технологии изготовления вкладыш-пустотообразователя на основе полипропилена
1. Технологическая часть1.1 Информационный обзор1.2 Выбор и краткая характеристика основного применяемого оборудования для переработки п
- Совершенствование технологии получения прядильного раствора в производстве ПАН волокон
На рубеже второго и третьего тысячелетий волокна на основе полимеров и сополимеров акрилоннтрила заняли 4-6% в общем балансе текстильно
- Совершенствование технологии получения технического ПАН жгутика
Полиакрилонитрильные волокна и нити в настоящее время представляют наиболее распространенный вид промышленно освоенных карбоцепных с
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

