Анализ биохимических показателей работы печени в норме и патологии
1. Функциональная биохимия печени
1.1 Регуляторно–гомеостатическая функция печени
1.1.1 Углеводный обмен в печени и его регуляция
1.1.2 Регуляция липидного обмена
1.1.3 Регуляция обмена белков
1.1.4 Участие печени в обмене витаминов
1.1.5 Участие печени в водно-минеральном обмене
1.1.6 Участие печени в пигментном обмене
1.2 Мочевинообразовательная функция
1.3 Желчеобразовательная и экскреторная функция
1.4 Биотрансформационная (обезвреживающая) функция
2. Заболевания печени и лабораторная диагностика заболеваний печени
2.1 Основы клинической лабораторной диагностики заболеваний печени
2.2 Основные клинико-лабораторные синдромы при поражениях печени
2.2.1 Синдром цитолиза
2.2.3 Синдром гепатодепрессии (малой недостаточности печени)
2.2.4 Синдром воспаления
2.2.5 Синдром шунтирования печени
2.2.6 Синдром регенерации и опухлевого роста печени
Заключение
Список литературы
Биохимия печени включает как протекание нормальных обменных процессов, так и нарушения метаболизма веществ с развитием патологии. Изучение всех аспектов биохимии печени позволит видеть картину нормально функционирующего органа и его участие в работе всего организма и поддержании гомеостаза. Так же при нормальной работе печени осуществляется интеграция всех основных обменов в организме, причем удается наблюдать начальные этапы метаболизма (например, при первичном всасывании веществ из кишечника) и конечные этапы с последующим выведением продуктов обмена из организма.
При нарушениях работы печени происходит сдвиг метаболизма в определенную сторону, поэтому необходимо изучение патологических состояний органа для дальнейшей диагностики заболеваний. В настоящее время это особенно актуально, так как заболевания печени прогрессируют, а достаточно хороших методов лечения пока не существует. К таким заболеваниям в первую очередь относятся вирусные гепатиты, циррозы печени (часто при систематическом употреблении алкоголя и при прочих вредных внешних воздействиях, связанных с неблагоприятной экологией), сдвиги метаболизма при нерациональном питании, онкологические заболевания печени. Поэтому очень важна ранняя диагностика этих заболеваний, которая может основываться на биохимических показателях.
Целью курсовой работы является рассмотрение функций печени и сравнение биохимических показателей работы этого органа в норме и патологии; также указание основных принципов лабораторной диагностики, краткое описание синдромов гепатитов различной этиологии и приведение примеров.
1. Функциональная биохимия печени
Условно функции печени по биохимическим показателям можно разделить на: регуляторно-гомеостатическую функцию, включающую основные виды обмена (углеводный, липидный, белковый, обмен витаминов, водно-минеральный и пигментный обмены), мочевинообразовательную, желчеобразовательную и обезвреживающую функции. Такие основные функции и их регуляция подробно рассмотрены далее в этой главе.
1.1 Регуляторно–гомеостатическая функция печениПечень – центральный орган химического гомеостаза, где чрезвычайно интенсивно протекают все обменные процессы и где они тесно переплетаются между собой.
1.1.1 Углеводный обмен в печени и его регуляцияМоносахариды (в частности глюкоза) поступают в печень по воротной вене и подвергаются различным преобразованиям. Например, при избыточном поступлении глюкозы из кишечника она депонируется в виде гликогена, так же глюкоза производится печенью в ходе гликогенолиза и глюконеогенеза, поступает в кровь и расходуется большинством тканей. Регуляция углеводного обмена осуществляется благодаря тому, что печень является практически единственным органом, который поддерживает постоянный уровень глюкозы в крови даже в условиях голодания.
Судьба моносахаридов различна в зависимости от природы, их содержания в общем кровотоке, потребностей организма. Часть их отправится в печёночную вену, чтобы поддержать гомеостаз, в первую очередь, глюкозы крови и обеспечить нужды органов. Концентрация глюкозы в крови определяется балансом скоростей ее поступления, с одной стороны, и потребления тканями с другой. В постабсорбтивном состоянии (постабсорбтивное состояние развивается через 1,5—2 часа после приема пищи, так же называется истинным или метаболическим насыщением (1). Типичным постабсорбтивным состоянием считают состояние утром до завтрака, после примерно десятичасового ночного перерыва в приеме пищи) и в норме концентрация глюкозы в крови равна 60-100 мг/дл (3,3-5,5 моль\л). А остальную часть моносахаридов (в основном глюкозы) печень использует для собственных нужд.
В гепатоцитах интенсивно протекает метаболизм глюкозы. Поступившая с пищей глюкоза только в печени с помощью специфических ферментных систем преобразуются в глюкозо-6-фосфат (лишь в такой форме глюкоза используется клетками) (6). Фосфорилирование свободных моносахаридов – обязательная реакция на пути их использования, она приводит к образованию более реакционно-способных соединений и поэтому может рассматриваться как реакция активации. Галактоза и фруктоза, поступающие из кишечного тракта, при участии соответственно галактокиназы и фруктокиназы фосфорилируются по первому углеродному атому:
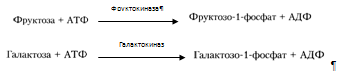
Глюкоза, поступающая в клетки печени, так же подвергается фосфорилированию с использованием АТФ. Эту реакцию катализирует ферменты гексокиназа и глюкокиназа.
печень патология диагностика заболевание
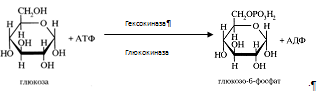
Гексокиназа обладает высоким сродством к глюкозе (Км <0,1 ммоль/л), поэтому максимум скорости реакции достигается при низкой концентрации глюкозы. Глюкозо-6-фосфат ингибирует гексокиназу. Глюкокиназа отличается от гексокиназы высоким значением Км для глюкозы – 10 ммоль/л и не ингибируется глюкозо-6-фосфатом. Это обеспечивает взаимное фунционирование обоих ферментов в печени. В постабсорбтивном состоянии концентрация глюкозы в крови низкая, около 5 ммоль/л и скорость глюкокиназной реакции примерно 1/5 от максимальной скорости. В таких условиях максимально работает гексокиназа. Во время пищеварения в воротную вену и далее в печень поступают большие количества глюкозы, и ее концентрация достигает и превышает 10 ммоль/л. Соответственно увеличивается скорость глюкокиназной реакции, причем если не происходит ингибирование гексокиназы глюкозо-6-фосфатом, то скорость гексокиназной реакции не падает. Что видно из графика:
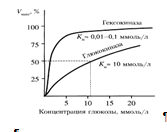
Наряду с другими механизмами это предотвращает черезмерное повышение концентрации глюкозы в периферической крови при пищеварении (7).
Образование глюкозо-6-фосфата в клетке – своеобразная «ловушка» для глюкозы, так как мембрана клетки непроницаема для фосфорилированной глюкозы (нет соответствующих транспортных белков). Кроме того, фосфорилирование уменьшает концентрацию свободной глюкозы в цитоплазме. В результате создаются благоприятные условия для облегченной диффузии глюкозы в клетки печени из крови.
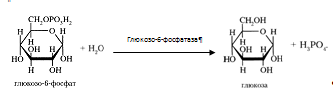
Возможна и обратная реакция превращения глюкозо-6-фосфат в глюкозу при действии глюкозо-6-фосфатазы, которая катализирует отщепление фосфатной группы гидролитическим путем.
Образовавшаяся свободная глюкоза способна диффундировать из печени в кровь. В других органах и тканях (кроме почек и клеток кишечного эпителия) глюкозо-6-фосфатазы нет, и поэтому там проходит только фосфорилирование, без обратной реакции, и выход глюкозы из этих клеток невозможен (3).
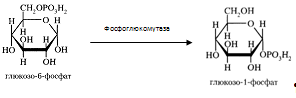
Глюкозо-6-фосфат может превратиться в глюкозо-1-фосфат при участии фосфоглюкомутазы, которая катализирует обратимую реакцию.
Так же глюкозо-6-фосфат может использоваться в различных превращениях, основными из которых являются: синтез гликогена, катаболизм с образованием СО2 и Н2О или лактата, синтез пентоз. Вместе с тем в процессе метаболизма глюкозо-6-фосфата образуются промежуточные продукты, используемые в дальнейшем для синтеза аминокислот, нуклеотидов, глицерина и жирных кислот. Таким образом, глюкозо-6-фосфат – не только субстрат для окисления, но и строительный материал для синтеза новых соединений (приложение 1).
Итак, рассмотрим окисление глюкозы и глюкозо-6-фосфата в печени. Этот процесс идет двумя путями: дихотомическим и апотомическим. Дихотомический путь это гликолиз, который включает «анаэробный гликолиз», завершающийся образованием молочной кислоты (лактата) или этанола и СО2 и «аэробный гликолиз» – распад глюкозы, проходящий через образование глюкозо-6-фосфата, фруктозобисфосфата и пирувата как в отсутствие так и в присутствие кислорода (аэробный метаболизм пирувата выходит за рамки углеводного обмена, однако может рассматриваться как завершающая его стадия: окисление продукта гликолиза – пирувата).
Апотомический путь окисления глюкозы или пентозный цикл заключается в образовании пентоз и возвращению пентоз в гексозы в результате распадается одна молекула глюкозы и образуется СО2 .
Гликолиз в анаэробных условиях - сложный ферментативный процесс распада глюкозы, протекающий без потребления кислорода. Конечным продуктом гликолиза является молочная кислота. В процессе гликолиза образуется АТФ.
Процесс гликолиза протекает в гиалоплазме (цитозоле) клетки и условно делится на одиннадцать этапов, которые соответственно катализируют одиннадцать ферментов:
1. Фосфорилирование глюкозы и образование глюкозо-6-фосфата – перенос остатка ортофосфата на глюкозу за счет энергии АТФ. Катализатором является гексокиназа. Этот процесс был рассмотрен выше.

2. Превращение глюкозо-6-фосфата под действием фермента глюкозо-6-фосфат-изомеразы во фруктозо-6-фосфат:
3. Фруктозо-6-фосфат вновь фосфорилируется за счет второй молекулы АТФ, реакция катализируется фосфофруктокиназой:
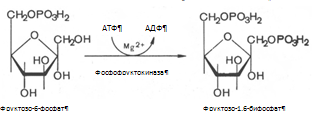
Реакция необратима, протекает в присутствии ионов магния и является наиболее медленно текущей реакцией гликолиза.
4. Под влиянием фермента альдолазы фруктозо-1,6-бифосфат расщепляется на две фосфотриозы:
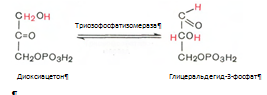
5. Реакция изомеризации триозофосфатов. Катализируеися ферментом триозофосфатизомеразой:
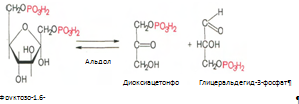
6. Глицеральдегид-3-фосфат в присутствии фермента глицеральдегидфосфатдегидрогеназы, кофермента НАД и неорганического фосфата продвергается своеобразному окислению с образованием 1,3-бифосфоглицериновой кислоты и восстановленой формы НАД – НАД*Н2 :
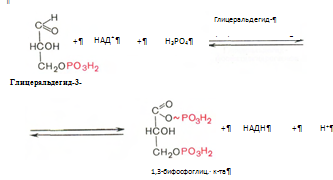
7. Реакция катализируется фосфоглицераткиназой, происходит передача фосфатной группы в положении 1 на АДФ с образованием АТФ и 3-фосфоглицериновой кислоты (3-фосфоглицерат):

8. Внутримолекулярный перенос оставшейся фосфатной группы, и 3-фосфоглицериновая кислота превращается в 2-фосфорлицериновую кислоту (2-фосфоглицерат):

Реакция легкообратима и протекает в присутствии ионов магния.
9. Реакция катализируется ферментом енолазой, 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится макроэргической:
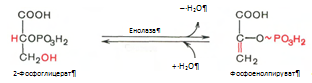
10. Разрыв макроэргической связи и перенос фосфатного остатка от фосфоенолпирувата на АДФ. Кртализируется ферментом пируваткиназой:
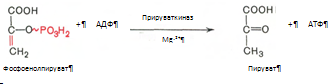
11. Восстановление пировиноградной кислоты и образование молочной кислоты (лактата). Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАД*Н2, образовавшегося в шестой ркакции:

Гликолиз в аэробных условиях. В этом процессе можно выделить три части:
1. специфические для глюкозы превращения, завершающиеся образованием пирувата (аэробный гликолиз);
2. общий путь катаболизма (окислительное декарбоксилирование пирувата и цитратный цикл);
3. митохондриальная цепь переноса электронов.
В результате этих процессов глюкоза в печени распадается до С02 и Н20, а освобождающаяся энергия используется для синтеза АТФ (приложение 2).
К обмену углеводов в печени относятся только специфические для глюкозы превращения, где происходит распад глюкозы до пирувата, который можно разделить на два этапа:
1. От глюкозы до глицеральдегидфосфата. В реакциях происходит включение фосфатных остатков в гексозы и превращение гексозы в триозу (приложение 3). Реакции этого этапа катализируют следующие ферменты: гексокиназа или глюкокиназа (1); фосфоглюкоизомераза (2); фосфофруктокиназа (3); альдолаза фруктозо-1,6-бисфосфата (4) фосфотриозоизомераза (5)
2. От глицеральдегидфосфата до пирувата. Это реакции, связанные с синтезом АТФ. Этап завершается превращением каждой молекулы глюкозы в две молекулы глицеральдегидфосфата (приложение 4). В реакциях участвуют пять ферментов: дегидрогеназа глицеральдегидфосфата (6); фосфоглицераткиназа (7); фосфоглицеромутаза (8); енолаза (9); пируваткиназа (10).
Пентозофосфатный (фосфоглюконатный) путь превращения глюкозы обеспечивает клетку гидрированным НАДФ для восстановительных синтезов и пентозами для синтеза нуклеотидов. В пентозофосфатном пути можно выделить две части — окислительный и неокислительный пути.
1. Окислительный путь включает две реакции дегидрирования, где акцептором водорода служит НАДФ (приложение 5). Во второй реакции одновременно происходит декарбоксилирование, углеродная цепь укорачивается на один атом углерода и получаются пентозы.
2. Неокислительный путь значительно сложнее. Здесь нет реакций дегидрирования, он может служить только для полного распада пентоз (до С02 и Н20) или для превращения пентоз в глюкозу (приложение 6). Исходными веществами являются пять молекул фруктозо-6-фосфата, в сумме содержащие 30 углеродных атомов, конечный продукт реакции — шесть молекул рибозо-5-фосфата, в сумме также содержащие 30 углеродных атомов.
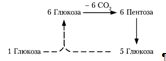
Окислительный путь образования пентоз и путь возращения пентоз в гексозы вместе составляют циклический процесс:
В этом цикле за один оборот полностью распадается одна молекула глюкозы, все шесть углеродных атомов которой превращаются в С02 (7).
Так же в печени идет обратный гликолизу процесс – глюконеогенез. Глюконеогенез — процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Глюконеогенез обеспечивает синтез 80-100 г глюкозы в сутки. Первичные субстраты глюконеогенеза — лактат, аминокислоты и глицерол. Включение этих субстратов в глюконеогенез зависит от физиологического состояния организма. Лактат — продукт анаэробного гликолиза. Он образуется при любых состояниях организма в эритроцитах и работающих мышцах. Таким образом, лактат используется в глюконеогенезе постоянно. Глицерол высвобождается при гидролизе жиров в жировой ткани в период голодания или при длительной физической нагрузке. Аминокислоты образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе. Необходимо отметить, что гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях (3).
Глюконеогенез в основном протекает по тому же пути, что и гликолиз, но в обратном направлении (приложение 7). Однако три реакции гликолиза необратимы, и на этих стадиях реакции глюконеогенеза отличаются от реакций гликолиза.
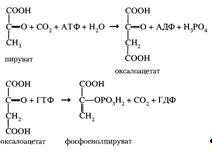
Превращение пирувата в фосфоенолпируват (необратимая стадия I) осуществляется при участии двух ферментов: пируваткарбоксилазы и карбоксикиназы фосфоенолпирувата:
![]()
Две другие необратимые стадии катализируются фосфатазой фруктозо-1,6-бисфосфата и фосфатазой глюкозо-6-фосфата:
Каждая из необратимых реакций гликолиза вместе с соответствующей ей реакцией глюконеогенеза образует субстратный цикл (приложение 7, реакции 1, 2, 3).
Синтез глюкозы (глюконеогенез из аминокислот и глицерина). Глюкоза в печени может синтезироваться из аминокислот и глицерина. При катаболизме аминокислот в качестве промежуточных продуктов образуются пируват или оксалоацетат, которые могут включаться в путь глюконеогенеза на стадии первого субстратного цикла (приложение 7, реакция 1). Глицерин образуется при гидролизе жиров и может превращаться в глюкозу (приложение 8). Аминокислоты и глицерин используются для синтеза глюкозы главным образом при голодании или при низком содержании углеводов в рационе (углеводное голодание).
Глюконеогенез может так же происходить из лактата. Молочная кислота не является конечным продуктом обмена, но ее образование — это тупиковый путь метаболизма: единственный способ использования молочной кислоты связан с ее превращением вновь в пируват при участиитой же лактатдегидрогеназы:
![]()
Из клеток, в которых происходит гликолиз, образующаяся молочная кислота поступает в кровь и улавливается в основном печенью, где и превращается в пируват. Пируват в печени частично окисляется, частично превращается в глюкозу — цикл Кори, или глюкозолактатпый цикл:
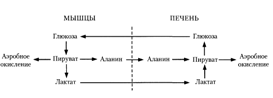
В организме взрослого человека за сутки может синтезироваться около 80 г глюкозы, главным образом в печени. Биологическое значение глюконеогенеза заключается не только в возвращении лактата в метаболический фонд углеводов, но и в обеспечении глюкозой мозга при недостатке углеводов в организме, например, при углеводном или полном голодании (2).
Синтез гликогена (гликогенез). Как уже говорилось выше, часть глюкозы поступившей в печень используется в синтезе гликогена. Гликоген — разветвленный гомополимер глюкозы, в котором остатки глюкозы соединены в линейных участках a-1,4-гликозидной связью. В точках ветвления мономеры соединены a-1,6-гликозидными связями. Эти связи образуются примерно с каждым десятым остатком глюкозы. Так возникает древообразная структура с молекулярной массой >107Д, что соответствует приблизительно 50 000 остатков глюкозы (приложение 9). При полимеризации глюкозы снижается растворимость образующейся молекулы гликогена и, следовательно, ее влияние на осмотическое давление в клетке. Это обстоятельство объясняет, почему в клетке депонируется гликоген, а не свободная глюкоза.
Гликоген хранится в цитозоле клетки в форме гранул диаметром 10—40 нм. После приёма пищи, богатой углеводами, запас гликогена в печени может составлять примерно 5% от её массы.
Распад гликогена печени служит в основном дляподдержания уровня глюкозы в крови в постабсорбтивном периоде. Поэтому содержание гликогена в печени изменяется в зависимости от ритма питания. При длительном голодании оно снижается почти до нуля.
Гликоген синтезируется в период пищеварения (через 1—2 ч после приёма углеводной пищи). Синтез гликогена из глюкозы требует затрат энергии.
Прежде всего глюкоза подвергается фосфорилированию при участии фермента гексокиназы и глюкокиназы. Далее глюкозо-6-фосфат под влиянием фермента фосфоглюкомутазы переходит в глюкозо-1-фосфат.
Образовавшийся глюкозо-1-фосфат уже непосредственно вовлекается в синтез гликогена.
На первой стадии синтеза глюкозо-1-фосфат вступает во взаимодействие с УТФ (уридинтрифосфат), образуя уридиндифосфатглюкозу (УДФ-глюкоза) и пирофосфат. Данная реакция катализируется ферментом глюкозо-1-фосфат-уридилилтрансферазой (УДФГ-пирофосфорилаза) (приложение 10).
На второй стадии — стадии образования гликогена — происходит перенос глюкозного остатка, входящего в состав УДФ-глюкозы, на глюкозидную цепь гликогена («затравочное» количество) (приложение 11). При этом образуется б-1,4-гликозидная связь между первым атомом углерода добавляемого остатка глюкозы и 4-гидроксильной группой остатка глюкозы цепи. Эта реакция катализируется ферментом гликогенсинтазой. Образующийся УДФ затем вновь фосфорилируется в УТФ за счет АТФ, и таким образом весь цикл превращений глюкозо-1-фосфата начинается сначала.
Установлено, что гликогенсинтаза неспособна катализировать образование б-1,6-гликозидную связь, имеющуюся в точках ветвления гликогена. Этот процесс катализирует специальный фермент, получивший название гликогенветвящего фермента, или амило-1,4-1,6-трансглюкозидазы. Последний катализирует перенос концевого олигосахаридного фрагмента, состоящего из 6 или 7 остатков глюкозы, с нередуцирующего конца одной из боковых цепей, насчитывающей не менее 11 остатков, на 6-гидроксиль-ную группу остатка глюкозы той же или другой цепи гликогена. В результате образуется новая боковая цепь. Ветвление увеличивает скорость синтеза и расщепления гликогена (2).
Распад гликогена или его мобилизация происходят в ответ на повышение потребности организма в глюкозе. Гликоген печени распадается в основном в интервалах между приёмами пищи, распад ускоряется во время физической работы. Распад гликогена происходит при участии двух ферментов: гликогенфосфорилазы и фермента с двойной специфичностью — 4:4-трансферазы-б-1,6-гликозидазы. Гликогенфосфорилаза катализирует фосфоролиз 1,4-гликозидной связи нередуцирующих концов гликогена, глюкозные остатки отщепляются один за другим в форме глюкозо-1-фосфата (приложение 12). При этом гликогенфосфорилаза не можетотщеплять глюкозные остатки от коротких ветвей, содержащих менее пяти глюкозных остатков; такие ветви удаляются 4:4-трансферазой-б-1,6-гликозидазой. Этот фермент катализирует перенос фрагмента из трех остатков короткой ветви на концевой глюкозный остаток более длинной ветви; кроме того, он гидролизует 1,6-гликозидную связь и таким образом удаляет последний остаток ветви (приложение 13).
Голодание в течение 24 ч приводит практически к полному исчезновению гликогена в клетках печени. Однако при ритмичном питании каждая молекула гликогена может существовать неопределенно долго: при отсутствии пищеварения и поступления в ткани глюкозы молекулы гликогена уменьшаются за счет расщепления периферических ветвей, а после очередного приема пищи вновь вырастают до прежних размеров.
Глюкозо-1-фосфат, образующийся из гликогена, при участии фосфоглюкомутазы превращается в глюкозо-6-фосфат, дальнейшая судьба которого в печени и в мышцах различна. В печени глюкозо-6-фосфат превращается в глюкозу при участии глюкозо-6-фосфатазы, глюкоза выходит в кровь и используется в других органах и тканях.
Регуляция процессов гликогенеза и гликогенолиза осуществляется гормонами: инсулином, глюкагоном, адреналином. Первичный сигнал для синтеза инсулина и глюкагона — изменение концентрации глюкозы в крови. Инсулин и глюкагон постоянно присутствуют в крови, но при смене абсорбтивного периода на постабсорбтивный изменяется их относительная концентрация, что является главным фактором, переключающим метаболизм гликогена в печени. Отношение концентрации инсулина в крови к концентрации глюкагона называют «инсулин-глюкагоновый индекс». В постабсорбтивном периоде инсулин-глюкагоновый индекс снижается, и решающее значение в регуляции концентрации глюкозы и крови приобретает концентрация глюкагона. В период пищеварения преобладает влияние инсулина, так как инсулин-глюкагоновый индекс в этом случае повышается. В целом инсулин влияет на обмен гликогена противоположно глюкагону. Инсулин снижает концентрацию глюкозы в крови в период пищеварения.
Гормон адреналин стимулирует выведение глюкозы из печени в кровь, для того чтобы снабдить ткани (в основном мозг и мышцы) «топливом» в экстремальной ситуации.
Регуляторным фактором в метаболизме гликогена является также величина Кмглюкокиназы, которая много выше, чем Км гексокиназы - печень не должна потреблять глюкозу для синтеза гликогена, если её количество в крови в пределах нормы.
1.1.2 Регуляция липидного обмена
Липидный обмен в печени включает биосинтез различных липидов (холестерина, триацилглицерина, фосфоглицеридов, сфингомиелина и др.) которые поступают в кровь и распределяются по другим тканям и сгорание (окисление) жирных кислот с образованием кетоновых тел, которые используются как источник энергии для внепеченочных тканей.
Доставка жирных кислот к месту окисления – к митохондриям клеток печени – происходит сложным путем: при участии альбумина осуществляется транспорт жирных кислот в клетку; при участии специальных белков – транспорт в пределах цитозоля; при участии карнитина – транспорт жирной кислоты из цитозоля в митохондрии.
Процесс окисления жирных кислот складывается из следующих основных этапов.
1. Активация жирных кислот. Активация протекает на наружной поверхности мембраны митохондрии при участии АТФ, коэнзима А (HS-KoA) и ионов Mg2+. Реакция катализируется ферментом ацил-КоА-синтетазой:
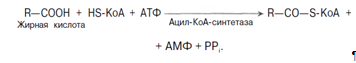
Активация протекает в 2 этапа. Сначала жирная кислота реагирует с АТФ с образованием ациладенилата, далее сульфгидрильная группа КоА действует на прочно связанный с ферментом ациладенилат с образованием ацил-КоА и АМФ.
Затем следует транспорт жирных кислот внутрь митохондрий. Переносчиком активированных жирных кислот с длинной цепью через внутреннюю митохондриальную мембрану служит карнитин. Ацильная группа переносится с атома серы КоА на гидроксильную группу карнитина.
2. Образуется ацилкарнитин, который диффундирует через внутреннюю митохондриальную мембрану:
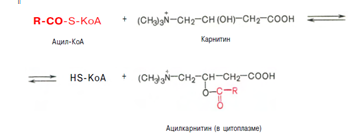
Реакция протекает при участии спецефического цитоплазматического фермента карнитин-ацилтрансферазы. После прохождения ацилкарнитина через мембрану митохондрий происходит обратная реакция – расщепление ацилкарнитина при участии HS-KoA и митохондриальной карнитин-ацилтрансферазы:
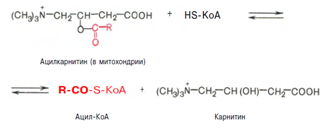
3. Внутримитохондриальное окисление жирных кислот. Процесс окисления жирной кислоты в митохондриях клетки включает несколько последовательных реакций.
Первая стадия дегидрирования. Ацил-КоА в митохондриях подвергается ферментативному дегидрированию, при этом ацил-КоА теряет 2 атома водорода в б- и в-положениях, превращаясь в КоА-эфир ненасыщенной кислоты. Реакцию катализирует ацил-КоА-дегидрогеназа, продуктом является еноил-КоА :
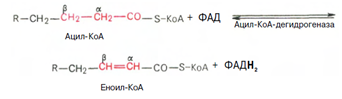
Стадия гидратации. Ненасыщенный ацил-КоА (еноил-КоА) при участии фермента еноил-КоА-гидратазы присоединяет молекулу воды. В результате образуется в-оксиацил-КоА (или 3-гидроксиацил-КоА):
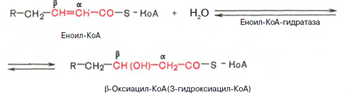
Вторая стадия дегидрирования. Образовавшийся в-оксиацил-КоА (3-гидроксиацил-КоА) затем дегидрируется. Эту реакцию катализируют НАД-зависимые дегидрогеназы:
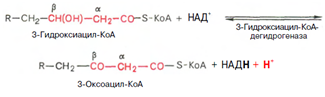
Тиолазная реакция. Расщепление 3-оксоацил-КоА с помощью тиоловой группы второй молекулы КоА. В результате образуется укороченный на два углеродных атома ацил-КоА и двууглеродный фрагмент в виде ацетил-КоА. Данная реакция катализируется ацетил-КоА-ацилтрансферазой (в-ке-тотиолазой):
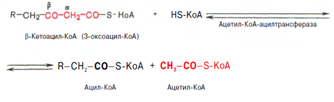
Образовавшийся ацетил-КоА подвергается окислению в цикле трикарбоновых кислот, а ацил-КоА, укоротившийся на два углеродных атома, снова многократно проходит весь путь в-окисления вплоть до образования бутирил-КоА (4-углеродное соединение), который в свою очередь окисляется до 2 молекул ацетил-КоА (2).
Биосинтез жирных кислот. Синтез жирных кислот протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот. Установлено, что в цитоплазме печеночных клеток синтезируется пальмитиновая кислота (16 углеродных атомов), а в митохондриях этих клеток из этой пальмитиновой кислоты или из жирных кислот экзогенного происхождения, т.е. поступающих из кишечника, образуются жирные кислоты, содержащие 18, 20 и 22 углеродных атома.
Митохондриальная система биосинтеза жирных кислот, включает несколько модифицированную последовательность реакций в-окисления, и осуществляет только удлинение существующих в организме среднецепочечных жирных кислот, в то время как полный биосинтез пальмитиновой кислоты из ацетил-КоА активно протекает в цитозоле, т.е. вне митохондрий, по совершенно другому пути.
Внемитохондриальная система биосинтеза жирных кислот (липогенез) находится в растворимой (цитозольной) фракции клеток печени. Биосинтез жирных кислот протекает с участием НАДФН, АТФ, Мn2+ и НСО3– (в качестве источника СО2); субстратом является ацетил-КоА, конечным продуктом – пальмитиновая кислота.
Образование ненасыщенных жирных кислот. Элонгация жирных кислот.
Две наиболее распространенные мононенасыщенные жирные кислоты – пальмитоолеиновая и олеиновая – синтезируются из пальмитиновой и стеариновой кислот. Эти превращения протекают в микросомах клеток печени. Превращению подвергаются только активированные формы пальмитиновой и стеариновой кислот. Ферменты, участвующие в этих превращениях, получили название десатураз. Наряду с десатурацией жирных кислот (образование двойных связей) в микросомах происходит и их удлинение (элонгация), причем оба эти процесса могут сочетаться и повторяться. Удлинение цепи жирной кислоты происходит путем последовательного присоединения к соответствующему ацил-КоА двууглеродных фрагментов при участии малонил-КоА и НАДФН. Ферментная система, катализирующая удлинение жирных кислот, получила название элонгазы. Пути превращения пальмитиновой кислоты в реакциях десатурации и элонгации представлены в приложении 14.
Биосинтез триглицеридов. Синтез триглицеридов происходит из глицерина и жирных кислот (главным образом стеариновой, пальмитиновой и олеиновой). Первый путь биосинтеза триглицеридов в печени протекает через образование б-глицерофосфата (глицерол-3-фосфата) как промежуточного соединения, глицерин фосфорилируется за счет АТФ с образованием глицерол-3-фосфата:

Второй путь в основном связан с процессами гликолиза и гликогенолиза. Известно, что в процессе гликолитического распада глюкозы образуется дигидроксиацетонфосфат, который в присутствии цитоплазматической глицерол-3-фосфатдегидрогеназы способен превращаться в глицерол-3-фосфат:

Образовавшийся тем или иным путем глицерол-3-фосфат последовательно ацилируется двумя молекулами КоА-производного жирной кислоты. В результате образуется фосфатидная кислота (фосфатидат):
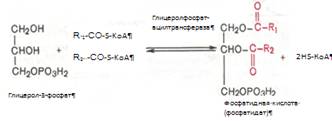
Ацилирование глицерол-3-фосфата протекает последовательно, т.е. в 2 этапа. Сначала глицерол-3-фосфат-ацилтрансфераза катализирует образование лизофосфатидата. Далее фосфатидная кислота гидролизуется фосфатидат-фосфогидролазой до 1,2-диглицерида (1,2-диацилглицерола):

Затем 1,2-диглицерид ацилируется третьей молекулой ацил-КоА и превращается в триглицерид (триацилглицерол). Эта реакция катализируется диацилглицерол-ацилтрансферазой:

Установлено, что большинство ферментов, участвующих в биосинтезе триглицеридов, находятся в эндоплазматическом ретикулуме, и только некоторые, например глицерол-3-фосфат-ацилтрансфераза,– в митохондриях.
Метаболизм фосфолипидов. Фосфолипиды играют важную роль в структуре и функции клеточных мембран, активации мембранных и лизосомальных ферментов, в проведении нервных импульсов, свертывании крови, иммунологических реакциях, процессах клеточной пролиферации и регенерации тканей, в переносе электронов в цепи дыхательных ферментов. Особая роль фосфолипидам отводится в формировании липопротеидных комплексов. Наиболее важные фосфолипиды синтезируются главным образом в эндоплазматической сети клетки.
Центральную роль в биосинтезе фосфолипидов играют 1,2-диглицериды (в синтезе фосфатидилхолинов и фосфатидилэтаноламинов), фосфатидная кислота (в синтезе фосфатидилинозитов) и сфингозин (в синтезе сфингомиелинов). Цитидинтрифосфат (ЦТФ) участвует в синтезе практически всех фосфолипидов.
Биосинтез холестерина. В синтезе холестерина можно выделить три основные стадии: I – превращение активного ацетата в мевалоновую кислоту, II – образование сквалена из мевалоновой кислоты, III – циклизация сквалена в холестерин.
Рассмотрим стадию превращения активного ацетата в мевалоновую кислоту. Начальным этапом синтеза мевалоновой кислоты из ацетил-КоА является образование ацетоацетил-КоА посредством обратимой тиолазной реакции. Затем при последующей конденсации ацетоацетил-КоА с 3-й молекулой ацетил-КоА при участии гидроксиметилглутарил-КоА-синтазы (ГМГ-КоА-синтаза) образуется в-гидрокси-в-метилглутарил-КоА. Далее в-гидрокси-в-метилглутарил-КоА под действием регуляторного фермента НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктаза) в результате восстановления одной из карбоксильных групп и отщепления HS-KoA превращается в мевалоновую кислоту.
Наряду с классическим путем биосинтеза мевалоновой кислоты имеется второй путь, в котором в качестве промежуточного субстрата образуется в-гидрокси-в-метилглутарил-S-АПБ. Реакции этого пути идентичны начальным стадиям биосинтеза жирных кислот вплоть до образования ацетоацетил-S-АПБ. В образовании мевалоновой кислоты по этому пути принимает участие ацетил-КоА-карбоксилаза – фермент, осуществляющий превращение ацетил-КоА в малонил-КоА.
На II стадии синтеза холестерина мевалоновая кислота превращается в сквален. Реакции II стадии начинаются с фосфорилирования мевалоновой кислоты с помощью АТФ. В результате образуется 5-фосфорный эфир, а затем 5-пирофосфорный эфир мевалоновой кислоты 5-пирофосфомевалоновая кислота в результате последующего фосфорилирования третичной гидроксильн
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Грибковые заболевания кожи
Федеральное агентство по здравоохранению и социальному развитиюСанкт-Петербургская государственная медицинскаяакадемия им. И.И. Мечн
- Дисфункциональные маточные кровотечения
- Лечение кандидоза
- Истмико-цервикальная недостаточность
- Лептоспиры. Лабораторная диагностика лептоспироза
- Повреждения от механических факторов, причины, течение и распознавание психических болезней
Судебная медицина изучает и разрабатывает различные проблемы биологии применительно к требованиям юридической и медицинской науки, п
- Понятие и классификация витаминов
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

