Лептоспиры. Лабораторная диагностика лептоспироза
КУРСОВАЯ РАБОТА
На тему:
"Лептоспиры. Диагностика лептоспироза"
Нижний Новгород 2010 г.
1. Историческая справка
Лептоспироз (лат. – Leptospirosis; болезнь Вейля, тиф собак) – в основном остро протекающая природно-очаговая болезнь животных многих видов и человека, проявляющаяся кратковременной лихорадкой, гемоглобинурией или гематурией, геморрагиями, желтушным окрашиванием и очаговыми некрозами слизистых оболочек и кожи, атонией желудочно-кишечного тракта, абортами, маститами, рождением нежизнеспособного потомства, периодической офтальмией и менингоэнцефалитами, снижением продуктивности животных.
80-е годы 19 века являются чрезвычайно насыщенным периодом микробиологических исследований и открытий. Вейн – врач-клиницист, описал первый реакцию агглютинации при риккетсиозе, сыпном тифе. Он подчеркнул, что это заболевание имеет выраженную вариабельность симптомов, оно может протекать в форме ОПН, с выраженным геморрагическим синдромом, всегда сопровождается желтухой.
В 1888 году Васильев независимо от Вейна описал лептоспироз как самостоятельную желтуху ничего общего не имеющую с болезнью Боткина.
Возбудитель поселяется в желчи, и может закупоривать желчные протоки.
Также лептоспироз называется иктерогеморрагическая лихорадка.
В 1928 году В.А. Башенин описал безжелтушную форму лептоспироза, и назвал ее водной лихорадкой. В 1972 году предложено разделить лептоспироз на две группы: желтушный лептоспироз и безжелтушный лептоспироз.
Возбудитель лептоспироза был обнаружен в 1914 году японскими учеными Инардо и Идо (в 1915 году), они независимо друг от друга выделили возбудителя.
Возбудитель лептоспироза – это спирохета, имеющая закругленный конец, очень тоненькая, со спиралевидным крючком. Назвали микроорганизм по его структуре – «лепто» – тонкий, «спира» – крючок. Таким образом, и всему роду возбудителей было дано название.
2. Распространение в природе
лептоспироз заболевание лечение диагностирование
Лептоспирозы относятся к группе заболеваний, которые являются не только зоонозами, но и природно-очагововыми заболеваниями. Основными резервуарами инфекции являются стоячие водоемы, в которых, как правило, сохраняются лептоспиры годами, а дикие грызуны (мыши-полевки, тушканчики и др.) являясь чрезвычайно чувствительными объектами для воспроизведения данной инфекции, поддерживают патологический процесс, болея лептоспирозом, который может протекать у них в различных формах – от бессимптомного носительства до тяжелых генерализованных форм.
Природные очаги лептоспирозов, обусловленные наличием инфекции среди диких животных, имеют ландшафтную стациальную приуроченность. Они располагаются преимущественно в лесной, лесотундровой зонах, а по долинам рек и ирригационным каналам проникают в лесостепную, степную и полупустынные зоны. В пределах своего ареала они встречаются не повсеместно, а в понижениях рельефа, где приурочены главным образом к сырым заболоченным и чрезмерно увлажненным местам. Наивысшей интенсивности лептоспирозного эпизоотического процесса и наибольшего эпидемического потенциала природные очаги достигают в летне-осенний период (июль – октябрь), что связано с пиком численности мелких млекопитающих.
Антропургические очаги, в противоположность природным очагам, не имеют определенной ландшафтной приуроченности и могут возникать повсеместно как в сельской местности, так и в городах. Антропургические очаги имеют важнейшее эпидемиологическое значение, особенно в условиях формирования крупных животноводческих хозяйств. Активность эпизоотического процесса возрастает летом. Манифестность инфекции при этом увеличивается. После острой инфекции через 10 – 20 дней у ряда особей развивается лептоспироносительство, которое продолжается в течение нескольких месяцев и до 1–2 лет, у свиней практически в течение жизни. Все вышеизложенное свидетельствует о том, что для эпизоотического процесса лептоспироза в природных и антропургических очагах характерна саморегулирующаяся смена фаз резервации и эпизоотического распространения возбудителя.
Грызуны выделяют возбудителя с мочой в окружающую среду: почву, инфицируя растения, что приводит к формированию природных очагов, но сформированных дикими животными, которые поедают растения, пьют инфицированную воду. В природе постоянно поддерживается циркуляция лептоспироз. Массивность инфицирования лептоспирами водоема зависит от количества рядом обитающих грызунов, которые являются основными поставщиками инфекции.
Таким образом, можно сказать, что любой район, любая сельская местность, может быть районом обитания грызуном, то есть любая местность может быть опасна с точки зрения формирования очага.
3. Эпизоотология
Механизм развития и проявления эпизоотического процесса (резервуар возбудителя).
Хозяевами лептоспир являются мелкие млекопитающие в природных очагах, синантропные грызуны, а также свиньи, крупный рогатый скот и другие домашние животные. Обычно в популяции диких штаммов лептоспир, выделенных от животных, характеризующихся высокой степенью вирулентности, содержатся и невирулентные клетки в 10 7, как и в невирулентной популяции – 107 вирулентных клеток.
У крупного рогатого скота, помимо бессимптомных форм, имеют место проявления иктерогемоглобинурии и желтухи. У супоросных свиноматок и реже у коров заболевание сопровождается абортами. Популяция каждого отдельного серовара лептоспир поражает главным образом популяции определенного вида животных. Этой особенностью определяются основные источники лептоспирозной инфекции. Но у совместно обитающих видов животных наблюдаются и перекрестные заражения.
С экологической точки зрения отдельные серогруппы имеют видовые свойства. Однако по официальной классификации все патогенные лептоспиры объединены пока в один вид L. interrogan в отличие от сапрофитного вида L. biflеха.
Эпидемические лептоспиры в популяции или стаде млекопитающих передаются от особи к особи водным путем.
Наибольшую опасность представляют свиньи, которые бывают поголовно инфицированы. Чрезвычайно опасны собаки как резервуар лептоспир и источник инфекции. Собакам не отводилось должной роли примерно до 1992–93 года, когда резко повысилась роль собачьей лептоспиры в возникновении лептоспироза. Этот лепоспироз, как правило, безжелтушный, протекает не так тяжело, без выраженных геморрагического синдрома, ОПН, но явления менингита есть. К 1995 году эта лептоспира опять стала занимать малый удельный вес в заболевании лептоспирозом. В 1996 года эта лептоспира занимала в структуре 8%.
Особую эпизоотологическую и эпидемиологическую опасность представляют бессимптомно больные животные-лептоспироносители. Количество лептоспироносителей на неблагополучной по лептоспирозу ферме среди крупного и мелкого рогатого скота колеблется от 1–5 до 10–20%; среди свиней – 30–80%. Срок лептоспироносительства после переболевания или скрытого инфицирования довольно продолжительный: у крупного рогатого скота 1,5–6 месяцев; у овец, коз – 6–9 месяцев; у свиней – от 15 дней до 2 лет; у собак – от 110 дней до 3 лет; у кошек – от 4 до 119 дней; у кур, уток, гусей – от 108 до 158 дней.
Выделяющиеся из организма больных животных и микробоносителей лептоспиры инфицируют воду, корма, пастбища, почву, подстилку, и другие объекты внешней среды, через которые заражаются здоровые животные. Среди указанных факторов передачи возбудителя водный путь является основным. Особую опасность представляют невысыхающие лужи, пруды, болота, медленно текущие речки, влажная почва.
Животные заражаются лептоспирозом чаще при водопое, при поедании трупов грызунов – лептоспироносителей или кормов, инфицированных мочей этих грызунов. Промысловые животные при клеточном их содержании инфицируются в основном при поедании продуктов убоя больных лептоспирозом животных; свиньи – во время купания в открытых водоемах, молодняк – при выпойке молока от больных матерей.
Возможно и внутриутробное заражение у крупного рогатого скота, овец и свиней. Доказана возможность передачи возбудителя половым путем.
Лептоспиры проникают в организм животного и человека через поврежденные участки кожи (царапины, порезы, раны, укусы), слизистые оболочки ротовой и носовой полостей, глаз, половых путей и через желудочно-кишечный тракт.
Лептоспироз чаще встречается в местностях, где почва влажная, содержит много гумуса, имеет нейтральную или слабощелочную реакцию.
Болезнь наблюдается в любое время года, но у животных с пастбищным содержанием – преимущественно в летне-осенний период. Так, анализ заболеваемости крупного рогатого скота лептоспирозом в России показывает, что на июнь-сентябрь приходится 77% заболевших животных. Сезонная динамика болезни в различных природно-экономических зонах неодинакова.
Лептоспироз свиней относится к числу болезней без выраженной сезонности, проявляющийся с равной интенсивностью на протяжении всего года. Это объясняется тем, что водный фактор в распространении заболевания среди свиней имеет значительно меньшее значение, чем для животных других видов.
Лептоспироз проявляется в виде небольших эпизоотий и спорадических случаев. Характерная особенность эпизоотии состоит в том, что вначале в течение 5–10 дней заболевает небольшая группа животных, затем вспышка затихает, но через несколько дней снова повторяется. Это обстоятельство связано с накоплением возбудителя инфекции во внешней среде, т. к. длительность паузы примерно равна инкубационному периоду.
Главной эпизоотологической особенностью лептоспироза сельскохозяйственных животных в настоящее время является преобладание бессимптомных форм инфекции в виде лептоспироносительства и лептоспирозной иммунизирующей субинфекции.
4. Патогенез
Не смотря на то, что возбудитель выделен, заболевание тяжелое, сопровождается высокой летальностью, патогенез его изучен мало. Очень хорошо знают о том, как лептоспира попадает в организм человека, как она выделяется, а где она размножается и накапливается изучено плохо. Все основано на предположениях. В организм лептоспира проникает через поврежденную кожу, через слизистые оболочки рта, носа, глаз, через ЖКТ. На месте входных ворот не отмечается никаких изменений, и проникновение в организм лептоспир не сопровождается возникновением воспалительной реакции, следовательно, раз нет первичного очага, лептоспира быстро проникает в кровь, и с током крови заносится во все органы и ткани. Некоторые авторы считают, что размножение лептоспир происходит в лимфатических узлах, в клетках РЭС. Некоторые полагают, что лептоспиры с током крови поступают в печень, и там происходит накопление лептоспир для формирования инфектомы – минимальной дозы достаточной для соответствующей реакции организма.
Накопившись до патогенных количеств, лептоспира выбрасывается в кровь, что сопровождается повышением температуры и характеризует начальный период заболевания, которое проявляется и как фаза кратковременной первичной бактериемией, с первичной диссеминацией возбудителя в организме. В инкубационном периоде возбудитель поступает в кровь и не оставляет следа что говорит о том что наличие иммуногенности у лептоспиры не велика. То есть эта фаза не сопровождается сенсибилизацией, и иммунокомпетентные клетки не имеют иммунной памяти, а следовательно, в эту фазу нет гиперэргического воспалительного ответа. Возникает лихорадка, которая длится 5–7 дней. Далее возбудитель с током крови проникает в различные органы, в том числе костный мозг, проявляя свое гематотоксическое воздействие, в почки оказывая нефротоксическое действие, в печень, спинной мозг, серозные оболочки головного мозга (вызывает серозный менингит). Часть возбудителей оседает в тканях, часть погибает вследствие бактерицидного действия крови. При гибели возбудителя высвобождается токсин, который оказывает токсическое влияние на эндотелий капилляров – повышение проницаемости, повреждение сосудистой стенки, а следовательно, и побуждает к формированию тромбов, которые могут служить первой фаза начинающегося ДВС-синдрома. В органах и тканях лептоспиры опять размножаются и накапливаются, а следовательно, после недельной лихорадки, температура понижается. Но в этом периоде самочувствие не улучшается, а напротив в этом периоде будет продолжаться токсемия и лептоспирозный токсин оказывает эффект, что может проявляться развивающимися мышечными болями, вследствие того, что повреждается капилляры мышц (пропотевание крови рядом с нервными стволами). Эти мышечные боли на фоне нормальной температуры заставляет обратиться пациента к врачу, и ему ставят что угодно, но только не лептоспироз.
Имеющийся конъюнктивит (следствие повреждения сосудов) также расценивается как вирусный. После накопления возбудителя в органах и тканях наступает следующая фаза – фаза вторичной бактериемии. Вновь возбудитель попадает в кровь, происходит повторная диссеминация возбудителя во все органы и ткани. Клинически эта фаза проявляется повышением температуры, таким образом, начинается лихорадка, так как в крови циркулируют лептоспиры, которые очень быстро гибнут. Первичная бактериемия создала условия для выработки и накопления антител, и при вторичной бактериемии происходит быстрая гибель микробов.
Взаимодействие антигена и антитело приводит к образованию комплексов, которые адсорбируются на шоковых органах – почки, печень, сердце, мягкие оболочки головного мозга, что приводит к формированию гипертермической воспалительной реакции (возбудитель в этой реакции уже не участвует).
Вторая фаза – фаза вторичной лептоспиремии, логично переходит в третью фазу патогенеза – фаза наивысшей степени токсинемии с развитием универсального капилляротоксикоза. Не смотря на то что лихорадки нет, симптоматика нарастает как снежный ком, так как заболевание приобретает аутоиммунный характер. Больше всего комплексы адсорбируются на эндотелии капилляров. Комплекс антиген-антитело способствуют выработки гистамина, брадикинина что приводит к некрозу капиллярам – возникает капилляротоксикоз. Если комплексы образовались в клубочково-канальцевом аппарате почек, то у больного развивается ОПН (олигоурия, повышение остаточного азота).
Если эти комплексы образовались преимущественно на эндотелии капилляров, то у больного начинается массивное кровотечение, и больной умирает от ДВС-синдрома. если оседают комплексы на оболочках головного мозга, то возникает менингит (серозный, гнойный). Если комплексы оседают на гепатоцитах, то возникает гепатит. Редко бывает поражение какого-либо одного органа, как правило, поражаются все органы и ткани, но с преимущественным поражением какого-либо одного органа.
Отмечается извращенная реакция костного мозга. Токсин лептоспир сам по себе способствует гемолизу эритроцитов. В крови повышается свободный (непрямой) билирубин. Моча вследствие геморрагического синдрома розовая, на фоне желтухи кожных покровов.
5. Течение и клиническое проявление
Инкубационный период 5–13 дней (по данным больницы Боткина 15–18 дней).
Лихорадочный период 6–7 дней, желтушный период 1–2 недели, рецидив болезни на 2–5 недели. Выздоровление через месяцы. То есть начало лептоспироза острое – лихорадка, с ознобом, интоксикацией, нарушением сна. В первые дни болезни характерным является наличие конъюнктивита, тошноты, рвоты (диспепсических расстройств), появление мышечных болей. Лихорадка всегда носит реммитирующий характер, особенно в первой фазе. После снижения температуры, у больных, как правило, появляется желтуха, которая усиливается появлением новой лихорадочной волны. Поэтому дифференциально – диагностическим признаком желтухи вызванной лептоспирозом и вирусным гепатитом А является этот признак, так как при вирусной гепатите А с появлением желтухи состояние больного, как правило, улучшается. С появлением желтухи появляется геморрагический синдром разной степени выраженности, и вовлекаются в процесс почки (нарастают явления ОПН).
Рецидивы болезни наблюдаются у 30% больных. Иногда при лептоспирозе отмечается появление розеолезной, папулезной, и даже эритематозной сыпи в третий период болезни, когда образуются комплексы, которые могут откладываться в лимфатических сосудах кожи и на лептоспиру будет реакция клеточных элементов. Сыпь может быть такая же, как при брюшном тифе (даже патогенез ее появления).
5.1 Осложнения
1. Серозный менингит, гнойный менингит (40% случаев). Чаще является осложнением безжелтушного варианта. Характерной особенностью является поздняя санация ликвора. Цитоз держится месяцами.
2. Поражение глаз – иридоциклит (7%).
3. Уремия (ОПН).
4. Пневмонии
5. Анемии
6. Геморрагический синдром
7. Инфекционно-токсический шок
8. Гепатит
5.2 Проявления лептоспироза
Безжелтушная форма лептоспироза: инкубационный период – 5–12 суток, резкий подъём температуры тела до 39–40°С, мышечные и головные боли, конъюнктивит, покраснение склер. На 3–5 сутки возможно появление ярко-розовой сыпи на конечностях и туловище. Возможны тошнота, рвота (иногда с кровью), боли в животе. В некоторых случаях отмечают двустадийное течение заболевания – в первой доминируют гриппоподобные проявления; для второй (через несколько суток или недель) характерна типичная клиника безжелтушного лептоспироза. Прогноз безжелтушного лептоспироза благоприятный. Осложнения безжелтушного лептоспироза – воспаление почек, легких, глаз.
Желтушный лептоспироз (болезнь Васильева–Вейля) – наиболее злокачественная форма лептоспироза. Инкубационный период – 2–19 суток (в среднем 7–13 суток). Желтушный лептоспироз начинается остро, температура тела повышается до 39–40°С. Лихорадка держится 5–7 суток и затем снижается до нормальных величин. Одновременно с падением температуры тела (иногда со 2–4 дня заболевания) появляется желтушное окрашивание кожи и слизистых оболочек. Приблизительно у 30% больных животных наблюдают повторный, обычно укороченный, подъём температуры тела (вторая неделя болезни); в начале 2 недели желтуха становится более интенсивной. Присутствуют мышечные и головные боли, конъюнктивит, тошнота, рвота (часто с кровью) и боли в животе. Могут быть герпетические высыпания на безшерстной части туловища животных. Практически у всех больных выявляют увеличение печени и селезёнки. В благоприятных случаях с конца второй недели и в течение последующих 5–6 недель наступает постепенное выздоровление. Осложнения желтушного лептоспироза: поражения органов зрения – парезы наружных мышц глаз, радужки, воспаления глазного нерва. Выздоровление сопровождается выработкой стойкого иммунитета.
6. Патологоанатомические признаки
Патологоанатомические изменения характеризуются анемией, желтухой, геморрагическим диатезом, некрозами кожи и слизистых оболочек, дегенеративно-воспалительными изменениями паренхиматозных органов.
Печень в большинстве случаев увеличена и перерождена. Цвет ее от глинисто-красного до желтого, консистенция упругая, дряблая или ломкая. Иногда в паренхиме обнаруживают мелкие некротические очажки и кровоизлияния. Желчный пузырь растянут и переполнен густой тягучей желчью темно- или буро-зеленого цвета; на слизистой оболочке единичные или множественные кровоизлияния.
Почки также увеличены, дряблые; в зависимости от степени кровенаполнения, дегенеративных изменений и пигментации окрашены в вишнево-глинистый, серовато-красный или темно-коричневый с зеленоватым оттенком цвет. Околопочечная клетчатка отечная. Фиброзная капсула серого цвета, обычно легко снимается. В паренхиме почек обнаруживают единичные или множественные сероватые очажки различной величины. Граница коркового и мозгового слоев сглажена. Корковый слой расширен, бледно окрашен, иногда содержит мелкие кровоизлияния. Лоханка часто заполнена желеобразной массой красноватого цвета.
Морфологическая картина по всем органам характеризуется лимфогистиоцитарными воспалительными инфильтратами, что позволяет считать эти изменения специфическими для лептоспироза.
7. Экономический ущерб
Экономический ущерб обусловливается высокой летальностью крупного рогатого скота и свиней (25–45% и более), снижением удоя (на 22–37%), потерей массы тела (на 18–28%), замедлением роста молодняка, понижением работоспособности у волов и буйволов, гибелью потомства (до 90%), абортами (у 15–20% коров и свиноматок у 100%), снижением товарных качеств кож переболевших животных и выбраковкой продуктов животноводства на мясокомбинатах, нарушением воспроизводительной функции, а также затратой значительных средств на диагностические, профилактические, лечебные и карантинно-ограничительные мероприятия (С.Я. Любашенко, 1948, 1962; М.А. Мусаев, 1959). Общая сумма ущерба, причиняемого лептоспирозом свиноводческим хозяйствам колеблется в пределах 12–47 тыс, рублей в год (в доперестроечных ценах), или в среднем 14,6 руб. на одно заболевшее животное (И.И. Дукачев, 1972).
8. Возбудитель болезни. Диагностика лептоспироза
Спирохеты – извитые подвижные бактерии, относящиеся к порядку Spirochaetales, семейству Spirochaetaceae. Патогенные спирохеты принадлежат к трем родам: Borrelia, Treponema, Leptospira.
8.1 Классификация
Возбудитель лептоспироза относится к группе 1 – спирохеты, семейство Leptospiraceae, род Leptospira, который включает в себя 10 видов:
Типовой вид: L. interrogans
L. biflexa (сапрофит)
L. borgpetersenii
L. inadai
L. meyeri (сапрофит)
L. noguchii
L. parva (сапрофит)
L. santarosai
L. weilii
L. wolbachii (сапрофит)
Наиболее изучен вид L. Interrogans, по антигенным свойствам он разделен на 25 серогрупп, которые включают 180 сероваров. Таксономическим критерием для классификации штаммов Leptospira на внутривидовом уровне служит антигенный состав клеток. Патогенные лептоспиры разделены на 38 серогрупп и 65 сероваров.
Установлена выраженная видовая чувствительность животных к лептоспирам определенных серологических групп и вариантов. Так, основными возбудителями лептоспироза свиней являются Pomona и Tarassovi, крупного рогатого скота – Hebdomadis, Pomona и Grippotyphosa, мелкого рогатого скота – Grippotyphosa, Pomona и Tarassovi. Крупный и мелкий рогатый скот заражаются лептоспирами Grippotyphosa и Hebdomadis преимущественно при выпасании на территории природного очага от полевок и других видов грызунов – основных резервуаров лептоспир данных серогрупп. Основными хозяевами лептоспир серогрупп Pomona и Tarassovi являются чаще свиньи и крупный рогатый скот. В природных очагах лептоспир Pomona у полевых мышей выявляют серовариант mozdok, который вызывает у сельскохозяйственных животных только спорадические случаи инфекции. Природные очаги лептоспир Tarassovi на территории России и стран СНГ не обнаружены.
Лептоспирами Tarassovi и Pomona в большинстве случаев свиньи заражаются только от свиней, а крупный рогатый скот – только от крупного рогатого скота. Может наблюдаться межвидовое заражение. Лептоспирами Icterohaemorrhagiae и Canicola сельскохозяйственные животные инфицируются от основных хозяев этих лептоспир: серых крыс и собак. Лептоспироз, вызванный этими возбудителями, протекает спорадически и не поражает больших групп животных.
У сельскохозяйственных животных в разных местах обнаруживают лептоспиры одних и тех же серологических групп: Pomona, Tarassovi, Hebdomadis, Icterhaemorrhagica, Canicola. У мелких млекопитающих, кроме названных, выделяют лептоспиры Australis, Javanica, Autumnalis, Cynopteri, Batoviae, Pyrogenes. Эти серогруппы у сельскохозяйственных животных не находят.
8.2 Устойчивость к факторам внешней среды
Лептоспиры неустойчивы к воздействиям внешних факторов. Прямые солнечные лучи убивают их в течение 0,5–2 ч. Высушивание на лептоспир действует также губительно. В воде открытых водоемов лептоспиры выживают от нескольких часов до 30 сут.
При кипячении культуры они гибнут моментально, а при нагревании до 56°С – через 30 мин. Очень устойчивы лептоспиры к низким температурам. Выживаемость микроорганизмов в пищевых продуктах зависит от рН среды. Кислая реакция губительно действует на лептоспиры. Так, в кислом молоке они гибнут в течение 10 мин. Мясо от больных животных обеззараживается при содержании в нем соли 4,8% в течение 10 сут. 20%-ный этиловый спирт, 2%-ная хлористоводородная кислота, 0,5%-ный раствор фенола, 0,5%-ный раствор едкого натра, 0,25%-ный формалин убивают лептоспир в течение 5 мин.
8.3 Отбор патматериала
Для прижизненной диагностики, для бакисследования берут кровь из вены (в первые 7 суток при повышении температуры тела больного животного, 5 мл для бактериологического и 5–10 мл для серологического исследований). Для серологической диагностики кровь отбирают не ранее 5–7 суток после начала заболевания. Обязательно нужно брать пробу крови от абортировшего животного. В крови можно обнаружить живые лептоспиры. Можно брать мочу, которую собирают в стерильные емкости во время естественного мочеиспускания утром (во время кормления). Абортированный плод посылают целиком или его желудок с содержимым (перевязывая его с двух сторон), паренхиматозные органы плода (отдельно от желудка).
Для посмертной диагностики – трупы мелких животных целиком, от крупных животных – сердце с перевязанными сосудами, кусочки органов, почку, селезенку, перевязанный мочевой пузырь, транссудаты из грудной и брюшной полостей. Материал должен быть исследован не позднее 6 часов летом, 10–12 часов – зимой, мочу – в течение 3 часов (то есть сроки выживания лептоспир в данных условиях).
Помимо материала от больных (павших) животных, в лабораторию могут быть направлены для исследования пробы воды (редко корм, навоз).
Для бакисследования предварительно готовят материал: мочу – центрифугируют (при 10–15 тыс. об/мин 30 мин) и исследуют осадок и надосадочную жидкость; кровь (цитратную) отстаивают, исследуют плазму; готовят из проб органов суспензию в стерильном физрастворе, исследуют в нативном состоянии или после центрифугирования.
8.4 Диагностика
Бактериологическая диагностика основана на обнаружении лептоспир в исследуемом материале путем микроскопии или выделения культур. Она складывается из следующих этапов: микроскопия в темном поле микроскопа, выделение культур лептоспир путем посева присланного материала от сельскохозяйственных животных или органов, зараженных этим материалом, лабораторных животных (биопроба) на специальные питательные среды, идентификация и дифференциация выделенных культур.
Одним из самых быстрых, простых и доступных для выполнения в практических условиях методов бактериологической диагностики является микроскопическое исследование. Микроскопию свежевыделенной мочи, околосердечной жидкости, грудного и брюшного экссудата, а также крови и суспензий паренхиматозных органов проводят в темном поле микроскопа. Морфология и характер движения лептоспир – настолько типичны, что в случае их обнаружения дается право ставить окончательный диагноз.
– Морфология
Клетка спирохеты имеет цилиндрическую извитую форму, содержит цитоплазму, отграниченную цитоплазматической мембраной, снаружи которой расположена клеточная стенка со слабовыраженным пептидогликановым слоем. Патогенные спирохеты имеют длину 3–20 мкм и толщину 0,1–0,5 мкм. Представители отдельных родов различаются по длине и толщине, числу и характеру завитков (табл. 2; рис. 21). Спирохеты грамотрицательны. Боррелии в отличие от трепо-нем и лептоспир хорошо окрашиваются анилиновыми красителями. Морфологию трепонем и лептоспир изучают путем микроскопии живых микроорганизмов в препаратах «раздавленная» или «висячая» капля в темнопольном или фазово-контрастном микроскопе, а также в мазках, окрашенных по Романовскому–Гимзе или специальными методами, например серебрением.
Лептоспиры различных серологических групп имеют одинаковые морфологические свойства. В препарате «раздавленная капля» в темном поле микроскопа лептоспиры имеют вид тонких серебристо-белых нитей с нежной спиральной структурой. Длина их 5–18 мкм, диаметр 0,05–0,14 мкм. Лептоспира имеет тонкую ригидную центральную осевую нить, вокруг которой равномерными завитками обвита цитопламатическая спираль. Тело лептоспиры, состоящее из правильных, почти соприкасающихся завитков спирали, постепенно утончается к концам, которые в большинстве случаев загнуты под углом и имеют пуговчатые утолщения (рис. 8). Помимо первичных завитков у лептоспир обнаруживают более крупные вторичные завитки, обусловливающие изгибы ее тела, вследствие чего микроорганизмы приобретают форму букв S, С, X. В старых культурах преобладают более длинные особи. Установлено наличие фильтрующихся форм лептоспир. Осевая нить служит органом движения. Характерная подвижность, лептоспир является их диагностическим признаком. Лептоспиры плохо окрашиваются анилиновыми красками, но хорошо импрегнируются серебром по методу Лёвадити.
Живые бактерии в жидких средах способны быстро перемещаться (прямолинейно, по кругу или вращением на месте). В полужидких субстратах их движения приобретают змеевидный характер. Периодически они становятся неподвижными, похожими на петлю веревки.
ЛС проявляют хемотаксис по отношению к веществам с повышенной вязкостью, гемоглобину и т.д. Сахара оказывают противоположный эффект и даже снижают их подвижность
Структура клетки лептоспир.
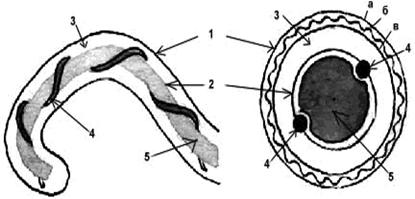
Обозначения: 1-наружная мембрана; 2-периплазматический цилиндр; 3-жгутик: - 1-наружная мембрана (а, б, в-ее слои); - 2-внутренняя мембрана; 3-периплазматическое пространство; 4-жгутики; 5-цитозоль
Структура клеточной стенки лептоспиры аналогична таковой других спирохет. 3–5-слойная наружная мембрана окружает протоплазматический цилиндр, покрытый гибким пептидогликановым слоем, тесно ассоциирванным с внутренней цитоплазматической мембраной, как у грамположительных бактерий. В этих слоях отсутствуют гликолипиды. В пептидогликане преобладает орнитин, а не диаминопимелиновая кислота, как считалось ранее.
Наружная мембрана лептоспиры весьма необычна, поскольку является самой жидкой из известных на сегодняшний день. Находящиеся в ней наружные мембранные протеины при движении всегда (даже при изменении направления) смещаются в задний конец клетки. Скорость дрейфа антигенов в мембранах приблизительно составляет 11 мкм/сек.
Оболочка клетки окружает так называемый «протоплазматический цилиндр». Благодаря укорочению закрученных вокруг него осевых нитей последний имеет винтообразную форму.
Два жгутика (осевые нити) диаметром 20–30 нм локализуются в периплазматическом пространстве между наружной мембраной и пептидогликановым слоем оболочки. Их свободный конец уже внутриклеточного. Аксиальная нить состоит из сердцевины диаметром 11,3 мкм, окруженной 2 мембранными слоями толщиной 21,5 и 42 микрон. Она прикрепляется крючком к базальному тельцу на противоположном конце периплазматического цилиндра и идет вдоль оси клетки приблизительно до ее центра. Аксиальные нити не перекрываются между собой, как это имеет место у других спирохет. Структура базальных телец жгутиков такая же, как и у других грамотрицательных бактерий. Аксиальные нити обеспечивают движение и сохранение лептоспир своей формы. В культурах лептоспиры нередко образуют клубки, а по мере старения в них появляются дегенирирующие формы с атипичной морфологией.
Прохождение на питательных средах более 20 пассажей ведет к изменению морфологии лептоспир – увеличению длины и количества завитков спирали, а также уменьшению количества электронно-прозрачных протоплазматических включений.
– Культуральные свойства
Лептоспиры являются аэробами, их культивируют на средах слабощелочной реакции (рН 7,2–7,4) при 24 – 28 °С. Культивирование лептоспир связано с определенными трудностями, обусловленными их низкой способностью к размножению в жидких, полужидких и особенно на плотных искусственных питательных средах. На простых питательных средах лептоспиры не растут. Для их культивирования наиболее часто используют жидкие среды Любашенко, Терских, Ферворт – Вольфа, содержащие 5–10% сыворотки крови кроликов, а также среду ГНКИ с альбумином. Максимальное накопление биомассы лептоспир отмечается по истечении 5–7 сут. культивирования, при этом вид питательных сред не изменяется.
Патогенные лептоспиры являются аэробными (часто микроаэрофильными) спирохетами. In vitro при хорошей аэрации, pH 7,2–7,4 и оптимальных условиях инкубирования (температуре 28– 30°C для большей части сероваров и 30–32°С для L.canicola) они культивируются намного лучше, чем другие спирохеты. Границы температуры инкубации посевов, в пределах которых возможен рост лептоспир, составляют 22–37°С.
Для нормального роста они нуждаются в липидах и ненасыщенных жирных кислотах, а также витаминах В1 и В12. Наличие белка в питательной среде для лептоспир не обязательно. Из числа аминокислот только аспарагин оказывает на них стимулирующее действие. Его можно заменить полисорбатами. Обработка твина поливинилпирролидоном устраняет его токсичность для лептоспир. В средах без протеина, но с обработанным этим способом твином урожай лептоспир достигает 108 кл/мл. Неплохой альтернативой твину-80 является пируват натрия, который добавляют в среды в концентрации 100 мкг/мл. Наличие в субстрате сахаров угнетает их рост.
Наиболее интенсивно лептоспиры растут на жидких и полужидких питательных средах с 5–10% сыворотки крови кролика или барана (вместо сыворотки часто применяют сывороточный альбумин). Время развития одной генерации лептоспир в логарифмической фазе составляет 58–68 ч, поэтому максимальный рост наблюдают на 5–10 дн.
Классической питательной средой для лептоспир является среда Ногуши-Веньона. Наибольшее распространение в работе с ними получили жидкие (Уленгута, Ферворта-Вольфа в модификации Тарасова, Кортхофа и др.) и полужидкие (Флетчера и др.) агаровые среды (ПРЛ 10:2).
На жидких средах эти спирохеты растут медленно – максимальный урожай бактерий обычно получают на 5–10 дн культивирования. При микроскопировании препаратов культур в этот период в одном поле зрения (окуляр х10, объектив х40) обычно обнаруживают около 100 подвижных бактерий. Культуры лептоспир в жидких средах бесцветны, не имеют запаха, при бурном росте опалесцируют. Опалесценция лучше видна в проходящем свете при легком встряхивании пробирки.
В полужидких средах на 1,5-2 см ниже поверхности появляется помутнение в виде кольца, интенсивность которого усиливается по мере роста лептоспир. В средах с 1% агара эти бактерии формируют преимущественно заглубленные колонии, контуры которых могут быть четкими или размытыми. Тенденция к заглубленному росту (феномен Дингера), обеспечивающая некоторое ограничение доступа кислорода, свидетельствует о микроаэрофильности лептоспир.
В средах с 2% агара лептоспиры образуют поверхностные колонии, имеющие разную степень прозрачности вплоть до трудно различимых при обычном освещении. Пассирование изолятов in vivo повышает частоту образования такого типа колоний, в то время, как многократные пересевы in vitro способствуют усилению заглубленного роста. Чем чаще делают пересевы, тем быстрее получают пышный рост культур.
Фосфомицин (400 мкг/мл) в сочетании с 5-флуорацилом (100 мкг/мл) при добавлении в среду ингибируют размножение посторонней микрофлоры, не влияя на рост лептоспир. Это позволяет использовать их в селективных средах. В качестве селективных компонентов сред применяют также мочевину, соли кобальта и антимикробные препараты (неомицин, рифампицин, фурацилин, фурагин, налидиксовую кислоту, комбинации рифампицина, полимиксина В, бацитрацина и актидиона.
В процессе хранении музейных штаммов лептоспир их пересевают не реже 1 раза в месяц. Для длительного хранения культуры заливают слоем стерильного вазелинового масла или запаивают в ампулы, что предупреждает испарение среды и и
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Повреждения от механических факторов, причины, течение и распознавание психических болезней
Судебная медицина изучает и разрабатывает различные проблемы биологии применительно к требованиям юридической и медицинской науки, п
- Понятие и классификация витаминов
- Распространение месторождений торфяных лечебных грязей России
КУРСОВАЯ РАБОТА"Распространение месторождений торфяных лечебных грязей России"Челябинск 2009АннотацияВ курсовой работе показаны и прос
- Анализ эпизоотологической обстановки и организация противоэпизоотических мероприятий по ликвидации туберкулеза крупного рогатого скота в ОАО "Вараксинское"
- Лечебно-косметические препараты в условиях аптеки
- Запоры: диагностика и лечение
- История женского служения больным
1. ЗАДАНИЕНачиная с первой половины XIX в. и связана история российских общин сестер милосердия, хорошо иллюстрирующая данный процесс: от
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

