Социальное поведение нормальных клеток и антисоциальное поведение опухолевых клеток
Маркович Васильев, доктор медицинских наук
ВВЕДЕНИЕ. МИКРОСРЕДА КЛЕТКИ
Поведение клетки в организме определяется средой, непосредственно окружающей эту клетку. Такая микросреда состоит из компонентов трех типов: а) соседних клеток; б) внеклеточных поверхностей, с которыми контактирует клетка, например, поверхностей коллагеновых волокон и других волокон, выделяемых клеткой (так называемого внеклеточного матрикса), и в) жидкой среды: тканевой жидкости, крови и лимфы. В упрощенных условиях культуры клетки также окружены трехкомпонентной микросредой: жидким компонентом здесь является питательная среда, а среди внеклеточных поверхностей наряду с волокнами матрикса имеется внутренняя поверхность культурального сосуда - подложка культуры. Все поведение нормальной клетки определяется сигналами, получаемыми из микросреды.
В предыдущей статье (5) мы разобрали некоторые механизмы регуляции деления и гибели клеток молекулами жидкого компонента микросреды - факторами роста и гормонами. В этой статье мы рассмотрим реакции клетки на два других компонента микросреды - на контакт с внеклеточным матриксом и поверхностью других клеток. Сложность этих взаимодействий в том, что они двусторонни: при контакте между клетками, разумеется, меняются обе клетки; при контакте с матриксом меняется не только клетка, но и матрикс. В результате множества таких взаимодействий группы клеток обустраивают ту территорию, на которой они живут, строят ткани и органы. Эта деятельность клеток аналогична деятельности людей, обустраивающих свою локальную территорию: дом и участок вокруг дома. При этом и люди и клетки совместно определяют границы между территориями соседей, строят свои дома или заселяют дома, построенные другими, а также организуют связи с ближними и дальними домами.
Изучению механизмов контактных реакций, ведущих к построению тканей (морфогенетических реакций), очень помогает сравнение поведения нормальных и опухолевых клеток. Как мы знаем, у опухолевых клеток реакции на внешние сигналы нарушаются в результате мутаций определенных генов: протоонкогенов и антионкогенов. Рассмотрим нарушения способности к морфогенетическим реакциям, возникающие в результате таких мутаций.
КЛЕТКИ ОБУСТРАИВАЮТ ТЕРРИТОРИЮ КУЛЬТУРЫ
Простейший вариант обустройства своей территории группой клеток - организация многоклеточной структуры, подобной ткани, из изолированных клеток эпителия или соединительной ткани ( фибробластов), высаженных в культуру, где клетки прикрепляются ко дну (подложке) сосуда, заполненного жидкой питательной средой. Одной из важных реакций, возникающих при такой организации, являются выработка и выделение специальных белков внеклеточного матрикса. Эти белки прикрепляются ко дну сосуда, а также полимеризуются вокруг клетки в особые нити, например коллагеновые волокна. Фибробласты в культуре, как и в организме, образуют рыхлую сеть таких волокон, окружающих клетки со всех сторон. Эпителиоциты образуют более густую решетку из особых коллагеновых волокон - так называемую базальную мембрану между клеткой и подложкой.
Клетка, коснувшаяся подложки с сорбированными молекулами белков матрикса или волокон матрикса, сделанных ею самой или другими клетками, начинает тут же реагировать на этот контакт, меняя форму и перестраивая цитоскелет (рис. 1). Мы уже разбирали механизмы таких реакций в предыдущих статьях (4). Повторим коротко суть происходящих при этом процессов. Центральной реакцией здесь является образование подвижных отростков - псевдоподий, наполненных внутри актиновыми филаментами. Поверхность псевдоподий образует затем специальные структуры - фокальные адгезии, где скопления белков-рецепторов прикрепляют мембрану этой клетки к белкам матрикса и через них к подложке. С внутренней стороны мембраны молекулы тех же рецепторов соединяются с актиновыми филаментами цитоскелета. Сокращения этих натянутых и прикрепленных к матриксу филаментов могут вызвать подтягивание всей клетки к фокальной адгезии. Многократное повторение этих реакций - основа движений клетки по подложке.
Клетки реагируют также на контакт с поверхностью другой клетки. Этот сигнал вызывает две реакции: остановку образования псевдоподий в направлении другой клетки (контактное торможение движений (4) и образование адгезионных структур второго типа (межклеточных адгезий).
Таким образом, комплекс морфогенетических реакций в культуре включает секрецию белков матрикса, образование и сокращение псевдоподий, образование адгезий между мембраной псевдоподий и матриксом и мембранами соседних клеток, а также контактное торможение движений. В результате многократного повторения таких реакций клетки организуются в многоклеточные системы, очень похожие на те ткани, которые те же клетки (эпителиоциты и фибробласты) строят в организме.
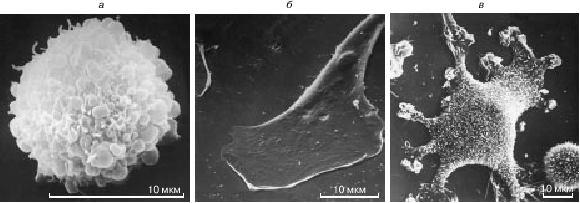
Рис. 1. Топография поверхности нормальных и трансформированных фибробластов в культуре. Сканирующие электронные микрофотографии Ю.А. Ровенского: а - нормальный мышиный фибробласт в жидкой среде. Сферическая клетка с многочисленными пузырчатыми выпячиваниями на поверхности. Увел. 3800; б - нормальный мышиный фибробласт, прикрепившийся к плоскому дну сосуда. Клетка распласталась на подложке, ее поверхность стала гладкой. Впереди - уплощенная ламелла с рядом плоских псевдоподий; сзади - узкое тело клетки. Увел. 1600; в - трансформированный мышиный фибробласт, прикрепившийся к плоскому дну сосуда. Клетка плохо распласталась на подложке, и ее поверхность не стала совершенно плоской. На этой поверхности видны многочисленные короткие ворсинки, а на концах отростков - фестончатые псевдоподии. Увел. 800
Эпителиоциты соединяются друг с другом в пласт из клеток, плотно спаянных адгезиями друг с другом и сидящих на базальной мембране, - организация, очень похожая на однослойный эпителий в организме.
Фибробласты приобретают в культуре вытянутую форму, образование которой зависит от цитоскелетной системы микротрубочек (4). Межклеточные адгезии у фибробластов в отличие от эпителиоцитов непрочны, они легко рвутся при движениях, и контактирующие клетки отделяются друг от друга. Поэтому фибробласты в культуре образуют систему из параллельно расположенных удлиненных клеток, между которыми располагается густая сеть волокон матрикса. В организме соединительные ткани и родственные им хрящевые и костные ткани построены по тому же типу - из клеток, отделенных друг от друга межклеточным матриксом разного состава (рис. 2). Такую систему можно сравнить с селом, где каждый индивидуум или группа индивидуумов отделен друг от друга большими приусадебными участками (структурами матрикса). Эпителий больше похож на коллектив, где индивидуумы более тесно связаны друг с другом, например на марширующую воинскую часть.

Рис. 2. Схема взаимоотношений между клетками (светло-коричневый цвет) и волокнами матрикса (синий цвет) в нормальной соединительной и эпителиальной ткани
КОНТАКТНЫЕ РЕАКЦИИ РЕГУЛИРУЮТ РАЗМНОЖЕНИЕ И ГИБЕЛЬ КЛЕТОК
Реакции с матриксом и подложкой не только приводят к построению тканей, но и участвуют в регуляции внутриклеточных процессов, и прежде всего размножения клеток (рис. 3). Нагляднее всего это видно из опытов, демонстрирующих зависимость размножения нормальных фибробластов от их прикрепления ко дну культуры и волокнам матрикса на этом дне (подложке). Когда мы делаем обычную культуру, то взвесь (суспензия) отделенных друг от друга клеток добавляется в питательную среду культурального сосуда, например чашки Петри. Под влиянием силы тяжести клетки взвеси опускаются на дно сосуда, прикрепляются к этому дну и лишь затем начинают размножаться, то есть вступают в митотический цикл (5). Прикрепление клеток к подложке можно предотвратить, если добавить в среду вязкое вещество (агар или метилцеллюлозу), мешающее клеткам оседать на дно. Клетки остаются взвешенными в таком "студне", размножаться они не начинают. Достаточно, однако, поместить в вязкую среду очень маленькие стеклянные палочки, чтобы клетки, не севшие на дно, но прикрепившиеся к поверхностям таких висящих палочек, немедленно вступили в митотический цикл и образовали через несколько дней колонии клеток вокруг каждой палочки. Очевидно, митотический цикл здесь индуцируется прикреплением клетки к подложке или сходной с ней поверхности палочки.
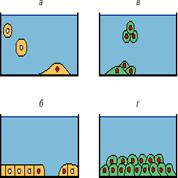
Рис. 3. Регуляция размножения клеток в культуре. Жидкая среда синяя, стенки и дно сосуда черные. У неразмножающихся клеток ядра не окрашены, у клеток в митотическом цикле красные: а, б - нормальные клетки: а - зависимость размножения клетки от подложки: вступила в цикл лишь клетка, прикрепившаяся к поверхности дна сосуда (подложке), но не клетки, взвешенные в жидкой среде, б - зависимость размножения от плотности населения культуры. Среди клеток, прикрепленных к подложке, размножаются лишь те, которые граничат со свободной поверхностью этой подложки, но не клетки, окруженные со всех сторон соседями; в, г - опухолевые клетки размножаются без подложки в жидкой среде (в) и на подложке независимо от числа соседей
В отличие от контактов с подложкой контакты с другими клетками, по-видимому, приводят к торможению размножения (рис. 3). Действительно, когда в результате размножения клеток культура становится густой и на ее дне не остается незанятых клетками мест, то эти клетки перестают делиться, то есть выходят из митотического цикла в так называемую фазу покоя Go (5). Если сделать рану (удалить бритвой со дна сосуда небольшой участок густой культуры), то контактное торможение на краю раны исчезает и клетки начинают мигрировать в рану на свободную подложку. Вскоре такие мигрировавшие клетки начинают в ране активно размножаться и делятся до тех пор, пока не зарастет вся рана, то есть свободная подложка. Эти опыты свидетельствуют о том, что размножение зависит от местной "густоты" населения культуры. Хотя они не доказывают строго, что именно прямые контакты клетка-клетка тормозят размножение, такая возможность представляется очень вероятной.
Контроль размножения с соседними клетками и подложкой в культуре аналогичен процессам, происходящим в организме, Приведем только один пример. Представьте себе царапину, нарушившую целостность эпителия кожи. Клетки эпителия по краю царапины начинают мигрировать на поверхность свободного матрикса и размножаются до тех пор, пока эта поверхность будет полностью закрыта.
Во всех случаях регулируется местное соотношение клеток и территорий, на которых они находятся. Нормальная клетка размножается только тогда, когда у нее есть свободная "площадь для жилья". Благодаря этим регуляциям поддерживается и восстанавливается после повреждений правильная тканевая структура (заживление ран!).
НАРУШЕНИЯ МОРФОГЕНЕТИЧЕСКИХ РЕАКЦИЙ ПРИ ОПУХОЛЕВЫХ ТРАНСФОРМАЦИЯХ
Опыты с культурами показали, что при опухолевых трансформациях эпителиоцитов и фибробластов резко нарушаются все морфогенетические реакции на контакты с другими клетками и подложкой. Такие трансформированные клетки делают меньше матрикса, хуже прикрепляются к матриксу, подложке и другим клеткам. Нарушаются также контактные регуляции размножения. Например, клетки, взвешенные в вязкой среде, продолжают размножаться без прикрепления к подложке. Эти клетки размножаются и в густой культуре независимо от числа соседей. В результате тканевые системы эпителия и соединительной ткани в культуре и организме становятся хуже организованными, а в предельном случае такие системы вообще не образуются, но распадаются на отдельные клетки и группы клеток. В организме такие отделившиеся от ткани клетки начинают двигаться на соседние территории и размножаться там. Например, трансформированные клетки эпителия, отделившись от пласта, начинают мигрировать через дефектную базальную мембрану в окружающую соединительную ткань, а затем проникать в просвет сосудов, откуда они током лимфы или крови могут переноситься в другие органы. Такие крайние изменения способности к морфогенетическим реакциям и построению тканей обусловливают наиболее опасные свойства опухолевых клеток - способность к врастанию в нормальные ткани (инвазия) и к образованию колоний в других органах (метастазирование). Отметим, что способность к инвазии и метастазированию свойственна лишь клеткам опухолей, наиболее резко измененным генетически. Врачи называют такие опухоли злокачественными (рис. 4). Клетки с менее измененными морфогенетическими реакциями образуют доброкачественные опухоли, где имеются различные нарушения организации тканевых структур, но нет инвазии и метастазирования. Анализ генома показал, что клетки злокачественных опухолей человека имеют целую серию мутаций разных онкогенов и антионкогенов, тогда как клетки доброкачественных опухолей обычно имеют меньшее число таких мутаций. Таким образом, степень нарушения морфогенетических реакций и соответственно течение опухоли определяется числом и степенью изменений генома опухолевых клеток, одной мутации для развития рака обычно недостаточно.
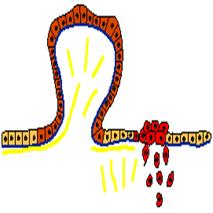
Рис. 4. Два опухолевых клона среди клеток нормального эпителия. Нормальные клетки светло-коричневые. Клетки клона, образующего доброкачественную опухоль - полип (темно-коричневый цвет), дают избыточный рост и образуют выпячивание над поверхностью пласта, но не проникают в соединительную ткань под эпителием. Напротив, клетки злокачественного (ракового) клона (красный цвет) проникают под базальную мембрану в соединительную ткань
МЕХАНИЗМ РЕГУЛЯЦИИ КОНТАКТНЫХ РЕАКЦИЙ
В первой части статьи (5) мы разобрали основы молекулярных механизмов действия специальных сигнальных молекул из жидкой среды, регулирующих размножение клеток. Напомним, что такие молекулы связываются со специальными рецепторами в наружной мембране клетки и активируют эти рецепторы, а те, в свою очередь, активируют цепь промежуточных белков в цитоплазме, что в конце концов приводит к активации синтеза ядерных белков, необходимых для удвоения генома (ДНК) и подготовки деления. Онкогены опухолевых клеток - мутировавшие гены, кодирующие белки разных этапов цепей проведения сигналов. При опухолевых трансформациях онкогены, вызывающие нарушения реакций на гуморальные факторы, индуцируют, как мы видели, и нарушения морфогенетических реакций. Отсюда следует, что многие этапы обеих групп реакций на сигналы контролируют одни и те же белки, в частности специальные ферменты, присоединяющие фосфат к белку (киназы, см. (5)). Конечными этапами цепей активации морфогенетических реакций становятся, вероятно, какие-то белки цитоскелета, например, белки, связывающиеся с актиновыми филаментами (3) и вызывающие изменения сборки и сокращения псевдоподий и образования контактных адгезий. Действительно, у некоторых таких белков присоединение фосфата резко повышено в трансформированных клетках, однако пока еще неясно, каково значение изменений каждого конкретного белка в нарушениях морфогенеза. Другой нерешенный вопрос - какие рецепторы определяют контактную регуляцию размножения нормальных клеток. Вероятное предположение состоит в том, что активация и торможение размножения зависят от тех же белков, которые прикрепляют клетку к подложке и другим клеткам, то есть от белков-рецепторов мембраны адгезионных структур, соединяющихся с белками подложки или соседних клеток. Оказалось, что адгезионные структуры с подложкой (так называемые фокальные контакты, рис. 5) содержат не только белки, необходимые для механического соединения белков матрикса через мембрану с цитоскелетом, но и несколько десятков видов других белков, функции которых неясны. Среди этих "непонятных" белков имеются различные протоонкобелки, участвующие в проведении сигналов, в том числе ферменты-киназы. Зачем они здесь? Естественно предположить, что фокальные адгезии не только механические "склейки", но и "органы осязания" клетки, передающие сигнал от соприкосновения с другой поверхностью с наружной мембраны внутрь клетки и вызывающие активацию размножения. Возможно, что рецепторы адгезий клетка-клетка, наоборот, индуцируют другие сигналы, тормозящие размножение. Все эти гипотезы сейчас активно проверяются в разных лабораториях мира. Взаимодействие системы, проводящей сигналы от мембраны, с цитоскелетом определяет ту разумную организацию движений и изменений формы клеток, тот "разум цитоскелета", о котором говорилось в предыдущей статье (4).
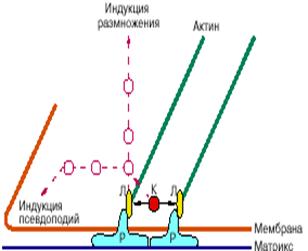
Рис. 5. Упрощенная схема фокального контакта клетки с матриксом. Молекулы - рецепторы белков матрикса (Р) наружной частью прикрепляются к волокнам матрикса, а на внутренней стороне мембраны те же рецепторы через посредство специальных белков - линкеров (Л) соединяются с концами актиновых филаментов цитоскелета (зеленый цвет), которые могут натягивать контакт. В фокальных контактах содержатся также специальные регуляторные белки (киназы - К), которые могут присоединять фосфат к другим белкам, меняя состояние и прочность контакта. Красным пунктиром обозначены гипотетические цепи проведения сигналов от фокальных контактов. Через ряд промежуточных белков (красные круги) такие цепи могут активировать размножение клеток и вызывать образование новых псевдоподий на поверхности клетки
ЗАКЛЮЧЕНИЕ. УНИЧТОЖАТЬ ИЛИ ИСПРАВЛЯТЬ ОПУХОЛЕВЫЕ КЛЕТКИ?
Исследования онкогенов и антионкогенов показали, что в клетке имеется сложнейшая система восприятия окружающего мира и многообразных реакций на этот мир. Мы разбирали реакции на отдельные сигналы (гормоны, контакты), но ведь на деле клетка как-то обобщает разные сигналы и реагирует на весь комплекс таких сигналов комплексом разных реакций (движениями, делением). Поведение клетки не проще, чем поведение человека, каждая реакция которого, например поездка из дома на работу, включает множество сигналов и сложных ответных действий (звон будильника, одевание, выход из квартиры, выбор автобуса нужного маршрута и т.п.). Подобно этому, после создания раны в культуре клетки оценивают целый комплекс факторов (появление свободной подложки, исчезновение контакта с другими клетками, состав жидкой среды) и дают в ответ комплекс реакций: движение в рану, включающее реорганизации цитоскелета и мембраны и почти одновременное вхождение в митотический цикл, включающее синтезы множества белков и РНК, удвоение ДНК, движения хромосом и т.д. Мы уже знаем молекулярные механизмы многих (но далеко не всех!) этапов этих реакций. Мы еще не знаем, однако, как все эти реакции интегрируются в клетке.
Как уже говорилось, биологическая суть опухолевой болезни - разрастание клонов клеток, у которых имеются мутации "генов социального поведения". Такие мутации в опухолях могут возникать последовательно, пока не появятся злокачественные клетки с целой серией мутировавших онкогенов и антионкогенов. Эти клетки реагируют не на внешние сигналы, а лишь на свои внутренние ложные сигналы, вызываемые мутантными белками. Сейчас врач может спасти больного от таких антисоциальных клеток, удалив весь клон хирургически или убив их рентгеновыми лучами и специальными веществами, которые губят делящиеся клетки. Эти методы при надлежащем искусстве врача высокоэффективны и излечивают очень многих. Однако все эти способы лечения не очень избирательны: нередко они не истребляют все опухолевые клетки или, наоборот, убивают не только опухолевые, но и нормальные делящиеся клетки (например, клетки костного мозга) и потому могут погубить организм вместе с опухолью. Кто-то удачно сравнил опухолевые клетки в организме с бандитами в человеческом обществе. Поведение бандита антисоциально, но трудно по внешнему виду отличить его от нормального человека. Столь же трудно придумать яд, который убивал бы только бандитов, но был безвреден для хороших людей.
Чем больше мы знаем о молекулярных механизмах регуляции клеток, тем больше надежда на то, что все же будут разработаны лекарства, убивающие избирательно только клетки-бандиты или, еще лучше, исправляющие поведение этих клеток. Можно представить себе несколько подходов к созданию таких "исправляющих" лекарств:
- генетическая инженерия, то есть введение в геном опухолевой клетки недостающих антионкогенов или, наоборот, разрушение онкогена. Генетики называют такое избирательное разрушение одного гена "нокаутом";
- инактивация патологической функции онкобелков, например избирательное подавление их киназной активности, то есть способности вызывать ложные сигналы путем присоединения фосфата к другим белкам.
Сейчас многие лаборатории и фармакологические фирмы ведут активную работу в этом направлении. Однако пока ни одного эффективного лекарства на основе этих подходов еще не создано.
Тем временем не надо забывать, что если не все, то многие мутации, приводящие к опухолевой трансформации, можно не только пытаться исправить, но и эффективно предотвращать. Для этого необходимо предотвратить контакты нормальных клеток организма с мутагенными агентами: лучами и химическими веществами, которые портят ДНК. Разбор действия таких агентов - задача отдельной статьи, но следует напомнить о самом распространенном мутагене, губящем ежегодно огромное число людей, - о табачном дыме. По подсчетам ученых-эпидемиологов, курение вызывает во многих странах до трети всех злокачественных опухолей. За многие годы в клетках легких у курильщика возникает целая серия мутаций онкогенов и антионкогенов. Обычно нужно накопить около десятка таких мутаций, чтобы измененная клетка дала начало злокачественному клону. Если человек перестает курить на несколько лет раньше, чем появились последние мутации, то рак не возникнет. Попытаемся сохранять наши клетки нормальными, способными правильно строить ткани и правильно вести себя в нашем организме.
Список литературы
1. Ченцов Ю. Общая цитология: (Введение в биологию клетки). 3-е изд. М.: Изд-во МГУ, 1995.
2. Альбертс А., Брей Д., Льюис Р. и др. Молекулярная биология клетки: В 3 т.: Пер. с англ. М.: Мир, 1994.
3. Васильев Ю.М. Клетка как архитектурное чудо. Ч. 1. Живые нити // Соросовский Образовательный Журнал. 1996. N 2. С. 36-43.
4. Васильев Ю.М. Клетка как архитектурное чудо. Ч. 2. Цитоскелет, способный чувствовать и помнить // Там же. N 4. С. 4-10.
5. Васильев Ю.М. Социальное поведение нормальных клеток и антисоциальное поведение опухолевых клеток. I. Сигнальные молекулы, вызывающие размножение и гибель клеток // Там же. 1997. N 4. C. 17-22.
Юрий Маркович Васильев, доктор медицинских наук, профессор, член-корреспондент РАН, профессор кафедры вирусологии МГУ, зав. лабораторией Всероссийского онкологического научного центра. Автор 180 научных работ, включая шесть монографий на русском и английском языках.
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Антиоксиданты: мифы и реальность
Такое ощущение, что мир свихнулся на антиоксидантах. И тем они хороши, и этим... И рак лечат, и жизнь продлевают, и морщины разглаживают. Ни
- О работе мозга в общем виде и о последствиях
Урынбаев Салават Хабибуллаевич, Ст. преп. КазНТУ, г. Алма-АтаНаучные отображения сложных систем представляются нам в виде древовидных ст
- Птицы зимы
- Сущность антропосоциогенеза
- Цепная реакция видообразования
- Изотопный состав человека
Из чего состоит человеческое тело? Помимо того, что как любая материя человеческий организм сложен из кирпичиков - атомов, атомы одного с
- Мимикрия
В процессе эволюции одни организмы начинают подражать другим — либо чтобы отпугнуть возможных хищников, сигнализируя об опасности, либ
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

