Разделение урана и тория с помощью тонкослойных неорганических сорбентов
Уральский Государственный Технический Университет - УПИ
Кафедра Радиохимии
Лабораторная работа № 1:
“Разделение урана и тория с помощью тонкослойных неорганических сорбентов".
2008 г.
1. Теоретическая часть
Цель работы:
Концентрирование микроколичеств тория из водного раствора соли уранила.
Уран и торий являются наиболее распространенными природными радиоактивными элементами. Три естественных, т.е. встречающихся в природе, изотопа урана входят в состав двух радиоактивных семейств: U-234 и U-238 находятся в семействе 4n+2, а U-235 - в семействе 4n+3. Один из самых долгоживущих природных изотопов Th-232 возглавляет семейство 4n+0. Другие природные изотопы тория (Th-234, Th-230) находятся в составе семейства урана-радия (4n+2). Больше естественных изотопов урана и тория не существует. Кларки урана и тория по данным А.П. Виноградова равны соответственно 2,5·10-4% и 1,3 ·10-3%.
В настоящее время основным "ядерным горючим" является уран. Торий можно рассматривать в качестве резервного источника энергии, если с помощью ядерно-химических процессов получать из него отсутствующий в природе U-233:
b- b-
232Th + n ® 233Th ® 233Pa ® 233U.
Период полураспада U-233 1,6·105 лет, поэтому его вполне можно получать и заготавливать впрок. Этот изотоп обладает способностью делиться на тепловых нейтронах с выделением энергии подобно U-235 и Pu-239.
Известны также другие искусственные изотопы урана и тория: от U-230 до U-240 и от Th-226 до Th-231. В подавляющем большинстве это a - и b - излучатели (при этом не следует забывать о сопровождающем g - излучении).
В данной лабораторной работе предлагается разделить уран и торий, часто сопровождающий уран в природных месторождениях. Кроме того, подобная задача (только в этом случае торий будет преобладающим элементом, а уран - на уровне микрокомпонента, или "примеси") встречается как в технологии природного тория, так и в технологии искусственного U-233.
1.1 Очерк химических свойств урана и тория, имеющих значение для гидрометаллургических процессов
Уран обладает более обширным перечнем химических соединений вследствие того, что он (противоположно торию) характеризуется несколькими степенями окисления. Например, в водных растворах существуют достаточно устойчивые его соединения, где уран находится в степенях окисления +3, +4, +5 и +6. А в твердой фазе, расплавах и в газообразном состоянии химические свойства урана еще разнообразнее. В то же время торий в растворах присутствует в составе соединений, где он проявляет единственную степень окисления +4. И уран в различных степенях окисления, и торий образуют большое число растворимых соединений, в том числе комплексных, и плохо растворимых, которые имеют технологическое значение, т.е. могут применяться в процессах обогащения, разделения, выделения, аффинажа.
1.1.1 Уран
В водных растворах наиболее устойчивы соединения, где уран находится в степенях окисления +4, в особенности +6. В степени окисления +3 он проявляет свойства сильного восстановителя, разлагает воду с образованием водорода; при этом уран окисляется:
U (III) ® U (IV).
Уран в степени окисления +5 склонен к диспропорционированию и устойчивых растворов не образует:
U (V) ® U (IV) + U (VI).
Все гидроксиды урана - U (OH) з, U (OH) 4, UO2 (OH) 2 - плохо растворимы. К плохо растворимым солям урана (во всех степенях окисления) относятся фосфаты, средние карбонаты и оксалаты. Среди фторидов плохо растворимы UFз и UF4, а UO2F2 обладает заметной растворимостью. Обладающий большой летучестью гексафторид урана, UF6 и промежуточные фториды (UF5, U2F9, U4F17) гидролизуются при соприкосновении с водой или ее парами с образованием UO2F2 и тетрафторида.
Фториды урана склонны образовывать комплексные соединения. Двойные фториды можно получить не только методами "сухой химии" (например, сплавлением), но и проведением реакций в растворах; часть из них кристаллизуется без воды, например, NH4UF5. Важную роль играют процессы растворения осадков труднорастворимых соединений и не только в кислотах, что в сущности является одним из основных приемов гидрометаллургии (последовательные процессы осаждения и растворения). Например, многие осадки соединений урана, в частности, тетрафторид урана, можно растворить в водных растворах оксалата или карбоната аммония с образованием комплексных соединений, в частности
(UO2 (C2O4) 2) 2 - ; (UO2 (CO3) 3) 4 - .
В согласии с основными принципами равновесий в растворах - непрерывностью и ступенчатостью - возможно существование и других комплексных форм с меньшим и даже большим мольным отношением числа лигандов к атомам комплексообразователя (n). Есть данные об образовании карбонатного комплекса с = 2 и оксалатного с = 3, то есть, типы этих комплексов одинаковы.
В некоторых технологических операциях используют способность урана пребывать в состояниях с различными степенями окисления. Например, U (IV) во многих отношениях напоминает торий, но свойства U (VI) уже совершенно иные, что может в ряде случаев обеспечить либо коллективный, либо селективный процесс.
Восстановителями урана (VI) могут служить различные металлы или их амальгамы (Zn, Cd, Bi, Mg, Al), соли Ti (III), Sn (II) и др. Возможно электрохимическое восстановление с помощью источника постоянного тока. Уран проявляет свойства амфотерности, выступая в роли "кислотообразующего элемента" (в основном, в степени окисления +6). Для удобства при проведении стехиометрических расчетов и для наглядности амфотерность урана (VI) можно проиллюстрировать следующим образом. Рассмотрим процессы, протекающие при титровании растворимой соли щелочью:
UO22+ + 2OH - ® UO2 (OH) 2; UO2 (OH) 2 «H2UO4,поскольку U (VI) амфотерен. (Знак «здесь и дальше обозначает фразу "то же самое, что и").
2NaOH + H2UO4 ® Na2UO4 + 2H2O.
(избыток)
Соединение NaUO4 представляет собой уранат натрия; уран в нем выполняет роль "кислотообразующего элемента". В действительности в данных обстоятельствах образуется не уранат, а полиуранаты, которые можно выразить общей формулой
хNaO · yUO3 · zHO.
Наиболее типичной и представительной формой, которая будет преобладать в достаточно "старом" осадке (а нужно добавить, что абсолютно все полиуранаты - нерастворимые соединения), является димер, диуранат (х = 1; у = 2): Na2U2O7 · zH2O. То же самое можно показать, применяя графы ("структурные формулы") молекул. Нелишне напомнить, что граф молекулы гипотетической "урановой кислоты" такой же, как и у серной:
HO OH HO OH HO O OH
\ / \ / \ / \ /
U + U ® U U + H2O.
// \\ // \\ // \\ // \\
O O O O O O O O
è____________ ø
H2 U2 O7
Поэтому соответствующая натриевая соль имеет состав: NaUO7. В общем случае она гидратирована.
К числу наиболее специфических реакций, приводящих к выделению урана в нерастворимый осадок, можно отнести реакции образования пероксидов. Среди них так называемая "надурановая кислота" UO4 2H2O.
Ее граф:
О = U = O · 2H2O (строение полимерное).
/ \
O - O
Осаждением пероксида часто пользуются при аффинаже соединений урана.
Все термически разлагающиеся соли урана при прокаливании на воздухе образуют так называемую "закись-окись" урана - U3О8 (имеет несколько модификаций).
По-видимому, это соединение не следует рассматривать как соединение оксидов, в которых уран проявляет различные степени окисления, UO2 · 2UOç, а полагать в нем уран, обладающим промежуточной (дробной) степенью окисления (+5,33), так как магнетохимические и структурные исследования показали, что все атомы урана в твердой фазе эквивалентны.
1.1.2 Торий
В водных растворах торий проявляет единственную устойчивую степень окисления +4. Известны важные в технологическом отношении растворимые соли тория: нитрат, хлорид, сульфат. К числу плохо растворимых солей относятся средние - карбонат, оксалат, фторид, фосфаты. В этом торий сходен с ураном (III, IV) и РЗЭ.
Средние - карбонат и оксалат - растворяются в избытке растворителя, образуя комплексные формы по аналогии с РЗЭ и ураном с =3 и =4. Гидроксид тория Th (OH) 4 плохо растворим, амфотерные свойства практически не проявляет. Ионы тория Th4+в водных растворах сильно гидратированы и гидролизованы. Образующиеся многоядерные гидроксокомплексы можно представить в общем виде:
Th ( (OH) 3Th) nn+4, (= 1,2,3).
Комплексы этого типа цепеобразны. Аналогичные цепи найдены и в некоторых кристаллических структурах, например в Th (OH) 4.
Итак, химические свойства тория и урана достаточно различны для того, чтобы без больших затруднений выполнять их разделение и в аналитических (включая радиоаналитические), и в технологических задачах. По классификации Пирсона (5,6) и уран и торий относятся к "жестким кислотам", поэтому они образуют наиболее устойчивые комплексы с лигандами, у которых донорными атомами являются элементы подгруппы N, O или F ("жесткие основания"). Количественные данные о комплексообразовании (константы устойчивости) позволяют утверждать, что тенденция к образованию ацидокомплексов, как правило, убывает в ряду:
M4+ > M3+ > MO22+ > MO2+,
т.е. в порядке уменьшения ионного потенциала. Но ряд специфичности по отношению к оксалат - и ацетат-ионам может содержать инверсию:
M4+ > MO22+ > M3+ > MO2+,
Эти качественные представления помогают ориентироваться в химическом поведении U (IV) и U (VI). В дальнейшем следует помнить и о различии в ионных радиусах U4+ (0,97![]() ) и Th4+ (1,02
) и Th4+ (1,02 ![]() ), так как в понимании химического поведения этих элементов, являющихся "жесткими кислотами", ионный потенциал играет ключевую роль.
), так как в понимании химического поведения этих элементов, являющихся "жесткими кислотами", ионный потенциал играет ключевую роль.
1.2 Многостадийные процессы
Концентрирование (или другие операции) может выполняться не за одну, а за несколько стадий, каждая из которых характеризуется своим значением степени извлечения. Например, в сорбционной технологии применяются последовательные операции сорбции - десорбции, но при этом и первоначальное извлечение компонента из раствора и его последующая десорбция (таких операций может быть несколько) характеризуются не стопроцентным переходом концентрируемого компонента (из раствора и из коллектора в новый раствор). Всегда бывают какие-то потери. В технологии допустимый уровень потерь диктует экономика, а в аналитике большую роль играет скорее хорошая воспроизводимость методики, чем полнота извлечения анализируемого компонента.
Таким образом, в случае многостадийного процесса (сорбция-десорбция и т.д.; экстракция-реэкстракция и т.д.) общее значение степени извлечения можно представить следующим образом:
N
Sобщ = П Si,
i=1
где N - число стадий.
Сорбционное концентрирование компонента или компонентов в колоночном ("динамическом") варианте обычно осуществляется в две стадии. На первой стадии компонент из раствора, пропускаемого с определенной скоростью через сорбционную колонну (или в лабораторных масштабах - колонку), поглощается твердым веществом сорбента. Эту стадию характеризует так называемая "выходная кривая" (см. рис.1), которую обычно строят в координатах "концентрация компонента в вытекающем растворе" (ось ординат) и "пропущенный объем раствора" (ось абсцисс). Таким образом, после проведения всех анализов можно рассчитать степень извлечения компонента на стадии сорбции (S1):
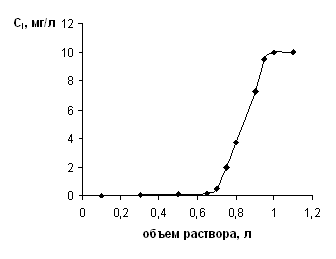
Рис.1 Выходная кривая сорбции урана сорбентом ТГ-Ц из имитата морской воды. С0 = 10 мг/л
S1 = 1 - ( åCiVi) / CoåVi, ,
i=1 i=1
где Co и Ci - концентрации компонента в исходном растворе и в i-й фракции вытекающего раствора соответственно; Vi - объем i-той фракции.
На второй стадии промывают колонку десорбирующим раствором, который по мере его вытекания из колонки также пофракционно анализируют на содержание компонента. По результатам анализа строят выходную кривую (см. рис.2), имеющую другой вид, и вычисляют степень извлечения на этой стадии:
k
S2 = ( åCjVj)/S1CoåVi, ,
j=1 i=1
где Cj - концентрация компонента в j-й фракции элюата (вытекающего десорбента) объемом Vj.
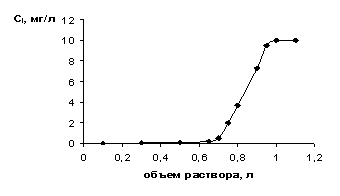
Рис.2. Выходные кривые десорбции урана раствором соляной кислоты
0.1 моль/л. 1 - дифференциальная; 2 - интегральная.
Ход работы:
Исходный раствор - нитрат уранила с концентрацией по урану 1-3 г/л, содержащий 10 - 50 мкг/л тория, рН раствора - 2,5-3,0. Сорбент - гидроксид титана, нанесенный тонким слоем на поверхность клиноптилолита, марка ТГ-Кл (12). Порядок выполнения работы следующий. Отбирают 2 пробы исходного раствора по 0.5 мл, сушат и измеряют на b - радиометре (I0). Через колонку, заполненную сорбентом, пропускают раствор нитрата уранила (50 мл) со скоростью 1 мл/мин·см2, отбирая фракции по 10 мл. Из каждой фракции отбирают 2 пробы по 0,5 мл, сушат и проводят b - метрию. По полученным результатам строят выходную кривую сорбции тория в координатах " П - V " и рассчитывают выход тория на стадии сорбции (В1).
Колонку промывают 10 мл дистиллированной воды и затем проводят десорбцию, пропуская 10 мл 1 моль/л раствора щавелевой кислоты, отбирая фракции по 2 мл. Из каждой фракции отбирают 2 пробы по 0,5 мл, сушат и проводят b - метрию. По полученным результатам строят выходную кривую десорбции тория в координатах "Д - V"
Практическая часть:
1. Проведем сорбцию и десорбцию тория, измерим скорость счета проб на β - радиометре. Так же отберем пробы исходного раствора. Данные измерений и расчетов занесем в таблицу № 1.
Таблица № 1
| Сорбция | Десорбция | ||||||||||
| N | I1 | I2 | Iср | Iср-Iф | П | N | I1 | I2 | Iср | Iср-Iф | Д |
| Фон | 27 | 23 | 25 | - | - | - | - | - | - | - | - |
| 1 | 36 | 36 | 36 | 11 | 0,08 | 1 | 2473 | 2490 | 2482 | 2457 | 0,664 |
| 2 | 30 | 30 | 30 | 5 | 0,04 | 2 | 203 | 198 | 201 | 176 | 0,047 |
| 3 | 36 | 32 | 34 | 9 | 0,07 | 3 | 70 | 75 | 73 | 48 | 0,013 |
| 4 | 40 | 36 | 38 | 13 | 0,10 | 4 | 52 | 51 | 52 | 27 | 0,007 |
| 5 | 40 | 42 | 41 | 16 | 0,12 | 5 | 53 | 54 | 54 | 29 | 0,008 |
| Исх 1 | 178 | 165 | 161 | 136 | - | - | - | - | - | - | - |
| Исх 2 | 152 | 148 | - | - | - | - | - | - | - | ||
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Характеристика химического элемента № 6 Углерод
Южно-Уральский государственный университетКафедра ЕНХарактеристика химического элемента№ 6 УглеродВыполнил:студент группы ММВ-335Ко
- Разложение клетчатки микроорганизмами
- Химико-технологические системы производств кремния высокой чистоты
- Разработка методики определения ультрамикрограммовых количеств тяжелых металлов методом инверсионной вольтамперометрии
Глава 1. Анализ следовых количеств веществ и электрохимические инверсионные методы1.1 Анализ следовых количеств веществ и проблемы,
- Разработка школьного элективного курса "Полимеры вокруг нас"
- Разработка энергосберегающей технологии ректификации циклических углеводородов
Федеральное агентство по образованиюМОСКОВСКАЯ ГОСУДАРСТВЕННАЯ АКАДЕМИЯ ТОНКОЙХИМИЧЕСКОЙ ТЕХНОЛОГИИ ИМЕНИ М.В. ЛОМОНОСОВАна правах р
- Расчет и подбор выпарной установки
Выпаривание - это процесс концентрирования растворов твёрдых веществ при температуре кипения путём частичного удаления растворителя
Copyright © https://www.referat-web.com/. All Rights Reserved
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

