Применение химических веществ группы углеводов в росписи тканей
Содержание
I . Углеводы. 2
II. Классификация всех видов углеводов. 3
III. Важнейшие представители углеводов. 4
1. Моносахариды.. 4
а) Глюкоза. 5
Химические свойства. 7
Получение. 7
Применение. 7
б) Фруктоза. 8
в) Рибоза. 8
2. Дисахариды.. 9
а) Сахароза. 9
б) Мальтозы и лактоза. 12
3. Полисахариды.. 14
а) Крахмал. 14
Химические свойства. 18
б) Целлюлоза. 18
Получение. 19
Применение. 22
Химические свойства. 23
IV. Применение химических веществ группы углеводов в росписи тканей. 24
Свободная роспись. 24
Прием свободной росписи по загустке. 25
Загустки и их приготовление. 25
I . Углеводы.
Углеводы - вещества состава Сn(Н2О)m, имеющие первостепенное биохимическое ёзначение, широко распространены в живой природе и играют большую роль в жизни человека.
Название углеводы возникло на основании данных анализа первых известных представителей этой группы соединения. Вещества этой группы состоят из углерода, водорода и кислорода, причем соотношение чисел атомов водорода и кислорода в них такое же, как и в воде, т.е. на каждые 2 атома водорода приходится один атом кислорода. В прошлом столетии их рассматривали как гидраты углерода. Отсюда и возникло русское название углеводы, предложенное в 1844г. К.Шмидтом. Общая формула углеводов, согласно сказанному, СмН2пОп. При вынесении «n» за скобки получается формула См(Н2О)n, которая очень наглядно отражает название «угле - воды».
Изучение углеводов показало, что существуют соединения, которые по всем свойствам нужно отнести в группу углеводов, хотя они имеют состав не точно соответствующий формуле СмH2пОп. Тем не менее старинное название «углеводы», сохранилось до наших дней, хотя наряду с этим названием для обозначения рассматриваемой группы веществ иногда применяют и более новое название - глициды.
Большой класс углеводов разделяют на две группы: простые и сложные.
Простыми углеводами (моносахаридами и мономинозами) называют углеводы, которые не способны гидролизоваться с образованием более простых углеводов, у них число атомов углерода равно числу атомов кислорода СпН2nОп.
Сложными углеводами (полисахаридами или полиозами) называют такие углеводы, которые способны гидролизоваться с образованием простых углеводов и у них число атомов углерода не равно числу атомов кислорода СмН2пОп.
II. Классификация всех видов углеводов.Углеводы
![]()
![]()
Простые Сложные
МОНОСАХАРИДЫ ДИСАХАРИДЫ
Тетрозы С4Н8О4 сахароза C12H22O11
элитроза лактоза
треоза мальтоза
Пентозы С5Н10О5 целобиоза
арабиноза ПОЛИСАХАРИДЫ
ксилоза (С5Н8О4)n
рибоза пентозаны
ГЕКСОЗЫ С6Н12О6 (С6Н10О5)n
глюкоза целлюлоза
манноза крахмал
галактоза гликоген
фруктоза
Моно- ( 1 молекула) | Олиго- (< 10 молекул) | Поли- (>10 молекул) |
Рибоза Фруктоза Глюкоза C6H12O6 | Сахароза = глюкоза +фруктоза Мальтоза = глюкоза + глюкоза | Крахмал (C6H10O5)n целлюлоза глюкоген – животный сахар |
1. Моносахариды
Моносахариды - это твердые вещества, способные кристаллизоваться. Они гидроскопичны, очень легко растворимы в воде, легко образуют сиропы, из которых выделить их в кристаллическом виде бывает очень трудно
Растворы моносахаридов имеют нейтральную на лакмус реакцию и обладают сладковатым вкусом. Сладость моносахаридов различна: фруктоза в 3 раза слаще глюкозы.
Все моносахориды представляют собой бифункциональные соединения, в состав которых входят неразветвленный угольный скелет, несколько гидроксильных групп и одна карбональная группа. Моносахориды с адельгидной группой называют альдозами, а с некогруппой – кетозами. Ниже приведены структурные формулы важнейших моносахоридов:
Моносахариды, важнейшие представители простых углеводов, в природе находятся как в свободном состоянии, так и в виде своих ангидридов - сложных углеводов.
Все сложные углеводы можно рассматривать как ангидриды простых сахаров, получающиеся путем отнятия одной или нескольких молекул воды от двух или более молекул моносахарида.
К сложным углеводам относятся разнообразные по своим свойствам вещества и их делят по этой причине на две подгруппы.
а) Глюкоза
Общая формула, строение. Глюкоза С6Н12О6 представляет собой белые кристаллы, сладкие на вкус, хорошо растворимые в воде. В линейной формуле молекулы глюкозы содержат одну альдегидную группу и пять гидроксидных групп. В кристаллах молекулы глюкозы находятся в одной из двух циклических форм (α- или β-глюкоза), которые образуются из линейной формы за счет взаимодействия гидроксильной группы при 5-м атоме углерода с карбональной группой.
Глюкозу называют также виноградным сахаром, так как она содержится в большом количестве в виноградном соке. Кроме винограда глюкоза находится и в других сладких плодах и даже в разных частях растений. Распространена глюкоза и в животном мире: 0,1% ее находится в крови. Глюкоза разносится по всему телу и служит источником энергии для организма. Она также входит в состав сахарозы, лактозы, целлюлозы, крахмала.
В растительном мире широко распространена фруктоза или фруктовый (плодовый) сахар. Фруктоза содержится в сладких плодах, меде. Извлекая из цветов сладких плодов соки, пчелы приготавливают мед, который по химическому составу представляет собой в основном смесь глюкозы и фруктозы. Также фруктоза входит в состав сложных сахаров, например тростникового и свекловичного.
В организме человека глюкоза содержится а мышцах, крови, и в небольших количествах во всех клетках.
В природе глюкоза на ряду с другими углеводами образуется в результате реакции фотосинтеза:
6СО2+6Н2О хролофил С6Н12О6+6О2-Q
В процессе этой реакции аккумулируется энергия Солнца.
На производстве глюкозу чаще всего получают гидролизом крахмала в присутствии серной кислоты:
![]() (С6Н10О5)n + nН2О Н2SO4, t nС6Н12О6
(С6Н10О5)n + nН2О Н2SO4, t nС6Н12О6
Физические свойства. Глюкоза — бесцветное кристаллическое вещество со сладким вкусом, хорошо растворимое в воде. Из водного раствора она выделяется в виде кристаллогидрата С6Н12Об*Н2О. По сравнению со свекловичным сахаром она менее сладкая.
Химические свойства.
Глюкоза обладает химическими свойствами, характерными для спиртов и альдегидов. Кроме того, она обладает и некоторыми специфическими свойствами.
Получение.
Первый синтез простейших углеводов из формальдегида в присутствии гидроксида кальция был произведен А. М. Бутлеровым в 1861 г.:

 О
О
![]()
![]() 6Н – С Са(ОН)2 С6Р12О6
6Н – С Са(ОН)2 С6Р12О6
Н
Применение.
Глюкоза является ценным питательным продуктом. В организме она подвергается сложным биохимическим превращениям, в результате которых освобождается энергия, которая накопилась в процессе фотосинтеза. Упрощенно процесс окисления глюкозы в организме можно выразить следующим уравнением:
С6Н12О6 + 6О2 = 6СО2 + 6Н2О + Q
Этот процесс протекает ступенчато, и поэтому энергия выделяется медленно. Так как глюкоза легко усваивается организмом, ее используют в медицине в качестве укрепляющего лечебного средства. Широко применяют глюкозу в кондитерском деле (изготовление мармелада, карамели, пряников и т. д.).
Большое значение имеют процессы брожения глюкозы. Так, например, при квашении капусты, огурцов, молока происходит молочнокислое брожение глюкозы, так же как и при силосовании кормов. Если подвергаемая силосованию масса недостаточно уплотнена, то под влиянием проникшего воздуха происходит маслянокислое брожение и корм становится непригоден к применению.
На практике используется также спиртовое брожение глюкозы, например при производстве пива.
б) Фруктоза
Фруктоза СеН12Об — изомер глюкозы. Как и глюкоза, она может существовать в линейной и циклических формах. В линейной форме фруктоза представляет собой кетоноспирт с пятью гидроксильными группами, а в циклической — кетофуранозу (т.е. пятичленный цикл с атомом кислорода).
Фруктоза вступает во все реакции многоатомных спиртов, но, в отличие от глюкозы, не реагирует с аммиачным раствором оксида серебра.
в) Рибоза
Рибоза и дезоксирибоза. Из пентоз большой интерес представляют рибоза и дезоксирибоза, ибо они входят в состав нуклеиновых кислот. Структурные формулы рибозы и дезоксирибозы с открытой цепью следующие:
Название дезоксирибоза показывает, что по сравнению с рибозой в ее молекуле на одну группу ОН меньше.
Как и глюкоза, молекулы рибозы и дезоксирибозы могут иметь и циклическое строение:
2. Дисахариды
Важнейшие дисахариды — сахароза, мальтоза и лактоза. Все они являются изомерами и имеют формулу С12Н22О11, однако их строение различно.
а) Сахароза
Молекула сахарозы состоит из двух циклов: шестичленного (остатка α-глюкозы в пиранозной форме) и пятичленного (остатка β-фруктозы в фура-нозной форме), соединенных за счет гликозидного гидроксила глюкозы:
Индусы еще за 300 лет до нашей эры умели получать тростниковый сахар из тростника. В наше время получают сахарозу из тростника, произрастающего в тропиках (на о.Куба и в других странах Центральной Америки).
В середине 18 века дисахарид был обнаружен и в сахарной свекле, а в середине 19 века был получен в производственных условиях.
В сахарной свекле содержится 12-15% сахарозы, по другим источникам 16-20% (сахарный тростник содержит 14-26% сахарозы).
Сахарную свеклу измельчают и извлекают из нее сахарозу горячей водой в специальных аппаратах-диффузорах. Полученный раствор обрабатывают известью для осаждения примесей, а перешедший частично в раствор избыточный гидролиз кальция осаждают пропусканием диоксида углерода. Далее после отделения осадка раствор упаривают в вакуум-аппаратах, получая мелкокристаллический песок-сырец. После его дополнительной очистки получают рафинированный (очищенный) сахар. В зависимости от условий кристаллизации он выделяется в виде мелких кристаллов или в виде компактных «сахарных голов», которые раскалывают или распиливают на куски. Быстрорастворимый сахар готовят прессованием мелкоизмельченного сахарного песка.
Тростниковый сахар применяется в медицине для изготовления порошков, сиропов, микстур и т.д.
Свекловичный сахар широко применяется в пищевой промышленности, кулинарии, приготовлении вин, пива и т.д.
Из молока получают молочный сахар - лактозу. В молоке лактоза содержится в довольно значительном количестве: в коровьем молоке 4-5,5% лактозы, женское молоко содержит 5,5-8,4% лактозы.
Лактоза отличается от других сахаров отсутствием гидроскопичности - она не отсыревает. Это свойство имеет большое значение: если нужно приготовить с сахаром какой-либо порошок, содержащий легко гидролизующее лекарство, то берут молочный сахар. Если взять тростниковый или свекловичный сахар, то порошок быстро отсыреет и легко гидролизующее лекарственное вещество быстро разложится.
Значение лактозы очень велико, т.к. она является важным питательным веществом, особенно для растущих организмов человека и млекопитающихся животных.
Солодовый сахар - это промежуточный продукт при гидролизе крахмала. По другому его называют еще мальтоза, т.к. солодовый сахар получается из крахмала при действии солода (по лат. солод - maltum).
Солодовый сахар широко распространен как в растительных, так и в животных организмах. Например, он образуется под влиянием ферментов пищеварительного канала, а также при многих технологических процессах бродильной промышленности: винокурения, пивоварении и т.д.
б) Мальтозы и лактоза
Молекула мальтозы состоит из двух остатков α -глюкозы в пиранозной форме, соединенных через 1-й и 4-й атомы углерода:
Лактоза состоит из остатков (3-галактозы и а-глюкозы в пиранозной форме, соединенных через 1-й и 4-й атомы углерода:
Все эти вещества представляют собой бесцветные кристаллы сладкого вкуса, хорошо растворимые в воде.
Химические свойства дисахаридов определяются их строением. При гидролизе дисахаридов в кислой среде или под действием ферментов связь между двумя циклами разрывается и образуются соответствующие моносахариды, например:
![]() С12Н22О11 + Н2О Н+, t С6Н12О6 + С6Н12О6
С12Н22О11 + Н2О Н+, t С6Н12О6 + С6Н12О6
глюкоза фруктоза
По отношению к окислителям дисахариды делят на два типа: восстанавливающие и невосстанавливающие. К первым относятся мальтоза и лактоза, которые реагируют с аммиачным раствором оксида серебра по упрощенному уравнению:
NH3
C12H22O11 + Ag2O ——— > С12Н22О12 + 2Ag.
Эти дисахариды могут также восстанавливать гидроксид меди (II) до оксида меди (I):
C12H22O11 + 2Сu(ОН)2 —— > С12Н22О12 + Cu2O↓ + 2Н2О.
Восстановительные свойства мальтозы и лактозы обусловлены тем, что их циклические формы содержат гликозидный гидроксил (обозначен звездочкой), и, следовательно, эти дисахариды могут переходить из циклической формы в альдегидную, которая и реагирует с Ag2O и Сu(ОН)2.
В молекуле сахарозы нет гликозидного гидроксила, поэтому ее циклическая форма не может раскрываться и переходить в альдегидную форму. Сахароза — невосстанавливающий дисахарид; она не реагирует с гидро-ксидом меди (II) и аммиачным раствором оксида серебра.
Распространение в природе. Наиболее распространенный дисахарид — сахароза. Это химическое название обычного сахара, который получают экстракцией из сахарной свеклы или сахарного тростника. Сахароза — главный источник углеводов в пище человека.
Лактоза содержится в молоке (от 2 до 8%) и получается из молочной сыворотки. Мальтоза содержится в проросших семенах хлебных злаков. Мальтоза также образуется при неполном гидролизе крахмала.
3. Полисахариды
Молекулы полисахаридов можно рассматривать как продукт поликонденсации моносахаридов. Общая формула полисахаридов (СбН10О5)п. Мы рассмотрим важнейшие природные полисахариды — крахмал и целлюлозу.
а) Крахмал
Крахмал образуется в растениях при фотосинтезе и откладывается в корнях и семенах. Он представляет собой белый порошок, нерастворимый в холодной воде и образующий коллоидный раствор в горячей воде.
Крахмал — это природный полимер, образованный остатками а-глю-козы. Он существует в двух формах: амилоза и амшопектин. Амилоза растворима в воде и представляет собой линейный полимер, в котором остатки ос-глюкозы связаны друг с другом через первый и четвертый атомы углерода.
Крахмал - это первый видимый продукт фотосинтеза. При фотосинтезе крахмал образуется в растениях и откладывается в корнях, клубнях, семенах. Зерна риса, пшеницы, ржи и других злаков содержат 60-80% крахмала, клубни картофеля - 15-20%. Крахмальные зерна растений различаются по внешнему виду, что хорошо видно, когда их рассматриваешь под микроскопом.
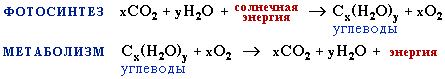
Внешний вид крахмала хорошо всем известен: это белое вещество, состоящее из мельчайших зерен, напоминающих муку, поэтому его второе название «картофельная мука».
Крахмал не растворим в холодной воде, в горячей набухает и постепенно растворяется, образуя вязкий раствор (клейстер).
При быстром нагревании крахмала происходит расщепление гигантской молекулы крахмала на мелкие молекулы полисахаридов, называемых декстринами. Декстрины имеют общую молекулярную формулу с крахмалом (С6Н12О5)х, разница лишь в том, «х» в декстринах меньше «n» в крахмале.
Пищеварительные соки содержат несколько разных ферментов, которые при низкой температуре доводят гидролиз крахмала до глюкозы:
(С6Н10О5) ------- (С6Н10О5)х --------- С12Н22О11 --------- С6Н12О6
крахмал ряд декстрин мальтоза глюкоза
Еще быстрее декстринизация идет в присутствии кислоты:
Н2SО4 t
(С6Н10О5)n ------------ n Н2О --------------- n С6Н12О6
Ферментативный гидролиз (разложение путем брожения) крахмала имеет промышленное значение в производстве этилового спирта из зерна и картофеля. Процесс начинается с превращением крахмала в глюкозу, которую затем сбраживают. Используя специальные культуры дрожжей и изменяя условия, можно направить брожение и в сторону получения бутилового спирта, ацетона, молочной, лимонной и глюконовой кислот.
Подвергая крахмал гидролизу кислотами, можно получить глюкозу в виде чистого кристаллического препарата или в виде патоки - окрашенного нескристаллизирующего сиропа.
Наибольшее значение крахмал имеет в качестве пищевого продукта: в виде хлеба, картофеля, круп, являясь главным источником в нашем рационе питания. Кроме того, чистый крахмал применяется в пищевой промышленности в производстве кондитерских и кулинарных изделий, колбас. Значительное количество крахмала употребляется для проклеивания тканей, бумаги, картона, производства канцелярского клея.
В аналитической химии крахмал служит индикатором в йодометрическом методе титрования. Для этих случаев лучше применять очищенную амилозу, т.к. ее растворы не загустевают, а образуемая с йодом окраска более интенсивна.
В медицине и фармации крахмал применяется для приготовления присыпок, паст (густых мазей), а также при производстве таблеток.
В животном мире роль «запасного крахмала» играет родственный крахмалу полисахарид - гликоген. Гликоген содержится во всех животных тканях. Особенно много его в печени (до 20%) и в мышцах (4%).
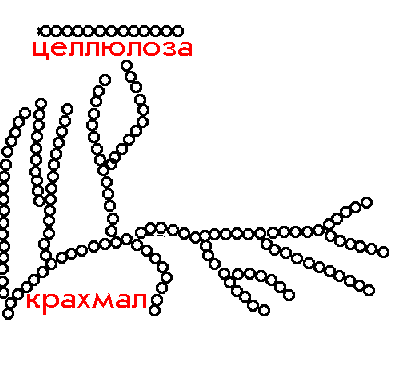
Фрагмент амилозы выглядит следующим образом:
Линейная полимерная цепь в молекуле амилозы свернута в спираль. Внутри спирали находится канал размером 0,5 нм, который может захватывать некоторые молекулы, например молекулу йода. Образующийся комплекс амилозы и йода имеет характерное синее окрашивание. Эта реакция служит для обнаружения йода.
В отличие от амилозы, амилопектин не растворим в воде и имеет разветвленное строение. В его молекуле остатки α-глюкозы связаны не только 1,4-связями, но и 1,6-связями:
Химические свойства.
При нагревании в кислой среде крахмал гидро-лизуется с разрывом связей между остатками a-глюкозы. При этом образуется ряд промежуточных продуктов, в частности мальтоза. Конечным продуктом гидролиза является глюкоза:
Н+, t
(С6Н10О5)n + nН2О ———> nС6Н12О6.
Эта реакция имеет важное промышленное значение, поскольку из глюкозы получают этанол, молочную кислоту и другие ценные продукты.
Крахмал — это ценный питательный продукт. Он входит в состав хлеба, картофеля, круп и наряду с сахарозой является важнейшим источником углеводов в человеческом организме.
б) Целлюлоза
Строение молекул. Молекулярная формула целлюлозы (C6H10O5)n, как и у крахмала. Целлюлоза тоже является природным полимером. Ее макромолекула состоит из многих остатков молекул глюкозы. Может возникнуть вопрос: почему крахмал и целлюлоза — вещества с одинаковой молекулярной формулой — обладают различными свойствами?
При рассмотрении синтетических полимеров мы уже выяснили, что их свойства зависят от числа элементарных звеньев и их структуры. Это же положение относится и к природным полимерам. Оказывается, степень полимеризации у целлюлозы намного больше, чем у крахмала. Кроме того, сравнивая структуры этих природных полимеров, установили, что макромолекулы целлюлозы, в отличие от крахмала, состоят из остатков молекул р-глюкозы и имеют только линейное строение. Макромолекулы целлюлозы располагаются в одном направлении и образуют волокна (лен, хлопок, конопля).
В каждом остатке молекулы глюкозы содержатся три гидроксильные группы.
Нахождение в природе.
Целлюлоза, так же как и крахмал, образуется в растениях при реакции фотосинтеза. Она является основной составной частью оболочки растительных клеток; отсюда происходит ее название — целлюлоза («целлула» — клетка). Волокна хлопка — это почти чистая целлюлоза (до 98%). Волокна льна и конопли тоже состоят главным образом из целлюлозы. В древесине ее содержится примерно 50%.
Получение.
Образцом почти чистой целлюлозы является вата, полученная из очищенного хлопка. Основную массу целлюлозы выделяют из древесины, в которой она содержится вместе с другими веществами. Наиболее распространенным методом получения целлюлозы в нашей стране является так называемый сульфитный. По этому методу измельченную древесину в присутствии раствора гидросульфита кальция Ca(HSO3)2 или «гидросульфита натрия NaHSO3 нагревают в автоклавах при давлении 0,5— 0,6 МПа и температуре 150 "С. При этом все другие вещества разрушаются, а целлюлоза выделяется в сравнительно чистом виде. Ее промывают водой, сушат и направляют на дальнейшую переработку, большей частью на производство бумаги.
Физические свойства. Целлюлоза — волокнистое вещество, нерастворимое ни в воде, ни в обычных органических растворителях. Растворителем ее является реактив Швейцера — раствор гидроксида меди (II) с аммиаком, с которым она одновременно и взаимодействует.
Химические свойства. Одно из наиболее характерных свойств целлюлозы — способность в присутствии кислот подвергаться гидролизу с образованием глюкозы. Аналогично крахмалу гидролиз целлюлозы протекает ступенчато. Суммарно этот процесс можно изобразить так:
![]() (С6Н10О5)n + nН2О Н2SO4 nСбН12О6
(С6Н10О5)n + nН2О Н2SO4 nСбН12О6
Так как в молекулах целлюлозы имеются гидроксиль-ные группы, то для нее характерны реакции этерификации. Из них практическое значение имеют реакции целлюлозы с азотной кислотой и ангидридом уксусной кислоты.
При взаимодействии целлюлозы с азотной кислотой в присутствии концентрированной серной кислоты в зависимости от условий образуются динитроцеллюлоза и три-нитроцеллюлоза, являющиеся сложными эфирами:
При взаимодействии целлюлозы с уксусным ангидридом (в присутствии уксусной и серной кислот) получается триацетилцеллюлоза или диацетилцеллюлоза:
Целлюлоза горит. При этом образуются оксид углерода (IV) и вода.
При нагревании древесины без доступа воздуха происходит разложение целлюлозы и других веществ. При этом получаются древесный уголь, метан, метиловый спирт, уксусная кислота, ацетон и другие продукты.
Применение.
Целлюлоза используется человеком с очень древних времен. Ее применение весьма разнообразно. Основные продукты, получаемые из древесины.
Большое значение имеют продукты этерификации целлюлозы. Так, например, из ацетилцеллюлозы получают ацетатный шелк. Для этого триацетилцеллюлозу растворяют в смеси дихлорметана и этанола. Образовавшийся вязкий раствор продавливают через фильеры — металлические колпачки с многочисленными отверстиями (рис. 36). Тонкие струи раствора опускаются в шахту, через которую противотоком проходит нагретый воздух. В результате растворитель испаряется и триацетил целлюлоза выделяется в виде длинных нитей, из которых прядением изготовляют ацетатный шелк Ацетил целлюлоза идет также на производство негорючей пленки и органического стекла, пропускающего ультрафиолетовые лучи.
Тринитроцеллюлоза (пироксилин) используется как взрывчатое вещество и для производства бездымного пороха. Для этого тринитроцеллюлозу растворяют в этил-ацетате или в ацетоне. После испарения растворителей компактную массу размельчают и получают бездымный порох. Динитроцеллюлоза (коллоксилин) применяется также для получения коллодия. В этих целях ее растворяют в смеси спирта и эфира. После испарения растворителей образуется плотная пленка — коллодий, применяемый в медицине. Динитроцеллюлоза идет также на производство пластмассы целлулоида. Его получают путем сплавления ди-нитроцеллюлозы с камфорой.
Целлюлоза (клетчатка) — основное вещество растительных клеток. Древесина на 50% состоит из целлюлозы, а хлопок и лен — это практически чистая целлюлоза.
Целлюлоза представляет собой твердое волокнистое вещество, нерастворимое в воде, но растворимое в аммиачном растворе гидроксида меди (II) (реактиве Швейцера).
Целлюлоза — природный полимер. В отличие от крахмала, ее молекулы состоят только из линейных цепей, содержащих остатки р-глюкозы, которые связаны через первый и четвертый углеродные атомы. Фрагмент линейной структуры целлюлозы выглядит следующим образом:
Химические свойства.
Гидролиз целлюлозы происходит при нагревании в кислой среде. Конечным продуктом гидролиза является глюкоза.
Для целлюлозы характерны реакции образования сложных эфиров. Каждое структурное звено молекулы целлюлозы содержит по три группы ОН, которые могут реагировать с азотной и уксусной кислотой:
(С6Н7О2(ОН)3)n + 3nHNO3 ——> (C6H7О2(ONO2)3)n + ЗnН2О. (С6Н7О2(ОН)3)n + ЗnСН3СООН ——> (C6H7О2 (ОСОСН3)3)n + ЗnН2О
Тринитрат целлюлозы (пироксилин) — взрывчатое вещество, на его основе готовят бездымный порох. Из триацетата целлюлозы изготавливают лаки, кинопленку и ацетатное волокно.
IV. Применение химических веществ группы углеводов в росписи тканей.Свободная роспись
Родиной этой техники считается Древний Китай. Предания относят возникновение ручной росписи шелковой ткани с помощью кисти еще к Х-ХП векам.
Если в других странах ткани украшенные ручной росписью применялись исключительно для национальной и ритуальной одежды, то в Китае батик применялся и в интерьере. Это были различные настенные панно и ширмы, на которых изображались пейзажи или растительные мотивы Нередко на них присутствовали фигуры людей и животных.
Свободная роспись внешне очень близка к восточным техникам живописи Мягкие живописные переходы, легкое, воздушное исполнение, по характеру похожи на нежный легкий набросок.
Эта техника требовала oт мастеров твердости руки и точности мазка, четкости и размытости пятна одновременно. В древних работах не было буйства красок, и внимание уделялось не столько цвету, сколько оттенкам. Даже очень светлые элементы имели большой диапазон тоновых градаций, оттенков и нюансов.
Подобная роспись была также распространена и в Японии, где применялась как для украшения национальной одежды, так и в качестве декора интерьера. Возникла и развивалась она под очень сильным влиянием Дзен-буддизма и традиционной живописи «суибоку».
В свободной росписи существует несколько различных приемов:
- свободная роспись по сухой ткани
- свободная роспись по увлажненной ткани
Прием свободной росписи по загустке.
В качестве загусток используются: сальвитоза, трагант, декстрин, крахмал и различные клеевые растворы.
Загусткой можно покрывать всю поверхность ткани, а после ее высыхания работать красителями. Такой прием напоминает рисование по бумаге. Можно делать как жесткие очертания, так и размывать их. Также работа с применением загусток дает возможность покрывать ткань не целиком, а частично и сочетать ее с другими видами росписи. Загустку можно добавлять в краситель, который становиться похожим на гуашь по консистенции. И работать им можно как гуашью мазками или перекрывая небольшие плоскости. Таким красителем можно осуществлять печать по трафарету при помощи губки. Такое разнообразие приемов обобщает возможности художника занимающегося искусством батика.
Загустки и их приготовление
1. Сальвитоза. Растворяется в воде при температуре 25 градусов по Цельсию, образуя загустку большой устойчивости. Смесь, 100-120 г сальвитозы с 900-880мл воды оставляют на один-два часа, затем размешивают и процеживают.
2. Трагант — застывший сок кустарника типа каучуконосных Имеет вид роговидных пластинок белого, желтого и коричневого цветов Для получения загустки берут траганта 60-80 гр., воды 940-920 мл. Трагант заливают холодной водой и оставляют на сутки. затем разваривают на кипящей водяной бане в 1ечение трех-четырех часов. Готовую загустку протирают через сито.
3. Декстрин клеящее вещество, хорошо растворяется в воде. Загустку из декстрина готовят так, берут 125-150 г декстрина и 875-850 мл воды, затем размешивают декстрин с небольшим количеством воды, потом разваривают в течение часа при помешивании на кипящей водяной бане до получения прозрачной массы. Готовую загустку процеживают через сито.
4. Крахмал - картофельный пли рисовый, такая загустка готовится как трагант.
В работе можно совмещать вышеперечисленные способы и добиваться, таким образом, разнообразных эффектов.
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Применение экспресс-анализаторов АН-7560, АН-7529 и АС-7932 в аналитической химии
Применение экспресс-анализаторов АН-7560,АН-7529 и АС-7932 в аналитической химии.Содержание. Наименование раздела СтрВведение.I. Экспресс-анал
- Применение электролиза
Доклад ученицы 10 кл. "Б"школы 1257Масоловой Елены по теме:Применение электролиза.Сущность электролиза. Электролиз — это окислительно-восс
- Природные источники углеводородов
- Проблемы государственного регулирования нефтяного комплекса России в условиях рынка
Министерство образования Российской ФедерацииРоссийский государственный университет нефти и газа имени И.М.Губкина.Кафедра управлени
- Программа для поступающих в вузы (ответы)
Программа по химии для абитуриентов 1. Предмет химии. Явления химические и физические.2. Атомно-молекулярное учение. Атомы. Молекулы. М
- Проект реконструкции цеха первичной переработки нефти и получения битума на ОАО «Сургутнефтегаз»
Введение На ОАО «Сургутнефтегаз» производят дорожный битум, дизельное топливо и бензиновую фракцию. Все эти производства на сегодняшни
- Производство метанола
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

