Лечение внебольничной пневмонии
Д.м.н. С.Н. Авдеев, НИИ пульмонологии МЗ РФ, Москва
Современные классификации, в зависимости от условий возникновения заболевания, подразделяют пневмонии на две большие группы: внебольничные и нозокомиальные (госпитальные) пневмонии (3). Отдельно выделяют пневмонии у больных с тяжелыми дефектами иммунитета и аспирационные пневмонии (5). Такой подход обоснован различными причинными факторами пневмоний и различными подходами к выбору антибактериальной терапии.
Внебольничные пневмонии условно можно разделить на 3 группы:
1. Пневмонии, не требующие госпитализации. Данная группа больных – самая многочисленная, на ее долю приходится до 80% всех больных с пневмонией; эти больные имеют легкую пневмонию и могут получать терапию в амбулаторных условиях, летальность не превышает 1–5% (7).
2. Пневмонии, требующие госпитализации больных в стационар. Эта группа составляет около 20% всех пневмоний, больные пневмонией имеют фоновые хронические заболевания и выраженные клинические симптомы, риск летальности госпитализированных больных достигает 12% (7).
3. Пневмонии, требующие госпитализации больных в отделения интенсивной терапии. Такие пациенты определяются как больные с тяжелой внебольничной пневмонией. Летальность при тяжелой пневмонии составляет около 40% (7).
Микробиология внебольничной пневмонии
Микробиологическая идентификация возбудителя возможна лишь в 40–60% случаев всех пневмоний. Структура возбудителей внебольничных пневмоний, основанная на результатах 41–го проспективного исследования (они проводились в Европе), представлена в таблице 1 (23).
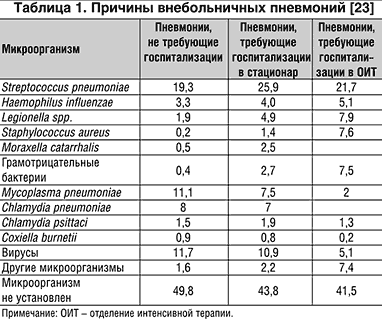
Streptococcus pneumoniae является ведущей причиной внебольничных пневмоний как среди больных с легкой, так и тяжелой пневмонией (около 20%). Среди больных пневмонией с бактериемией, на долю S. pneumoniae приходится до двух третей всех причин заболевания.
Второе место по значению среди причин внебольничных пневмоний занимают «атипичные» микроорганизмы – Mycoplasma pneumoniae и Chlamydophila pneumoniae (до 10–20%), распространенность данных возбудителей зависит от сезона, возраста больных, географического региона.
Staphylococcus aureus, Legionella pneumophila и грамотрицательные бактерии (Klebsiella pneumoniae, Pseudomonas aeuruginosa и др) играют более скромную роль в генезе внебольничных пневмоний, однако их роль возрастает по мере нарастания тяжести заболевания. Инфекции Legionella spp. встречаются, в основном, в регионах с теплым климатом (страны Средиземноморья), и довольно редко – в странах Северной Европы (23).
Роль анаэробных микроорганизмов в генезе внебольничных пневмоний небольшая, но значительно возрастает при аспирационных пневмониях – до 50% всех причин. Вирусные инфекции являются причиной 5–15% всех внебольничных пневмоний, при этом основное значение имеет вирус гриппа, меньшее – вирусы парагриппа, аденовирусы, респираторно–синтициальный вирус. Вирусные пневмонии имеют сезонное преобладание, преимущественно в осенне–зимнее время.
На протяжении последних лет во всем мире наблюдается стремительный рост резистентности возбудителей пневмоний к антибактериальным препаратам. Для некоторых патогенов ситуация резистентности к антимикробным препаратам является сходной во всем мире. Так, например, практически все штаммы Moraxella catarrhalis являются продуцентами b-лактамаз, а атипичные микроорганизмы (микоплазма, хламидия, легионелла) практически не имеют проблем с развитием приобретенной устойчивости к антибиотикам. Однако для S. pneumoniae и H. influenzae пропорция резистентных штаммов значительно варьирует как между странами, так и между регионами одной страны.
Значительно увеличилась доля пневмоний, вызываемых штаммами S. pneumoniae, устойчивыми к пенициллину, и к другим антибиотикам (полирезистентные штаммы). Доля штаммов S. pneumoniae, резистентных к пенициллину, в мире варьирует от < 5% до > 50%, что зависит от географического региона, популяции (чаще у детей), локализации инфекции (чаще в назофарингеальной зоне) и клинического окружения (чаще в стационаре) (18). По данным Российского многоцентрового исследования ПеГАС–1, на долю штаммов S. pneumoniae, устойчивых к пенициллину, приходится 9% (умеренно резистентные – 7%, высоко резистентные – 2%) (2), однако следует учесть, что резистентность штаммов значительно варьирует в каждом регионе. Устойчивость пневмококка к макролидам в России также невелика, в тоже время очень высока резистентность к тетрациклинам (27%) и ко–тримоксазолу (33%). Факторами риска для развития устойчивости пневмококков к антибиотикам являются: возраст больных более 60 лет и менее 7 лет, наличие сопутствующих заболеваний, предшествующая антибиотикотерапия, пребывание в домах ухода.
Оценка тяжести и риска летального исхода при внебольничной пневмонии
Объективная оценка тяжести состояния больного является необходимым инструментом для принятия решения о тактике ведения больного, решения вопросов о его транспортировке, об оптимальном месте терапии больного (специализированное отделение, отделение интенсивной терапии и др.), для сравнения исходов больных в зависимости от методов терапии, качества оказания помощи.
Наиболее актуальной проблемой при первичной оценке больного с пневмонией является вопрос о том, где больной должен получать терапию: в домашних условиях (т.е. госпитализация не требуется), в условиях отделения стационара или в условиях реанимационного отделения.
Показания к госпитализации больных с внебольничной пневмонией в стационар и в отделение интенсивной терапии представлены в таблицах 2, 3.


Более простые алгоритмы также позволяют оценить риска летального исхода при тяжелой внебольничной пневмонии, например, при наличии двух из трех признаков: мочевина крови > 20 мг/дл, частота дыхания і 30 мин-1 и диастолическое артериальное давление Ј 60 мм рт.ст. (правило Британского торакального общества), риск развития смертельного исхода повышается в 21 раз по сравнению с больными, у которых отсутствуют данные показатели (12).
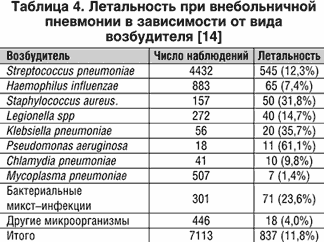
Причинный фактор также оказывает влияние на прогноз заболевания: летальность больных значительно повышена при обнаружении таких микроорганизмов как: S. pneumoniae, Legionella spp., P. aeruginosa (14) (табл. 4).
Антибактериальная терапия при внебольничной пневмонии
Начальный выбор антимикробного препарата производится эмпирически (т.е. до получения результатов микробиологического исследования), так как:
– как минимум, в половине случаев ответственный микроорганизм не удается выявить даже при помощи современных новейших методов исследования, а существующие микробиологические методы довольно неспецифичны и малочувствительны;
– любая задержка этиотропной терапии пневмоний сопровождается повышенным риском развития осложнений и летальности пневмонии, тогда как своевременная правильно выбранная эмпирическая терапия позволяет улучшить исход заболевания;
– оценка клинической картины, рентгенологических изменений, сопутствующих заболеваний, факторов риска и тяжести пневмонии в большинстве случаев позволяет принять правильное решение о выборе адекватной терапии.
В то же время необходимо стремиться к уточнению этиологического диагноза, особенно у больных с тяжелой пневмонией, так как такой подход может оказать влияние на исход заболевания. Кроме того, преимуществами «направленной» терапии являются уменьшение количества назначаемых препаратов, снижение стоимости лечения, снижение числа побочных эффектов терапии и уменьшение потенциала селекции резистентных штаммов микроорганизмов (8).
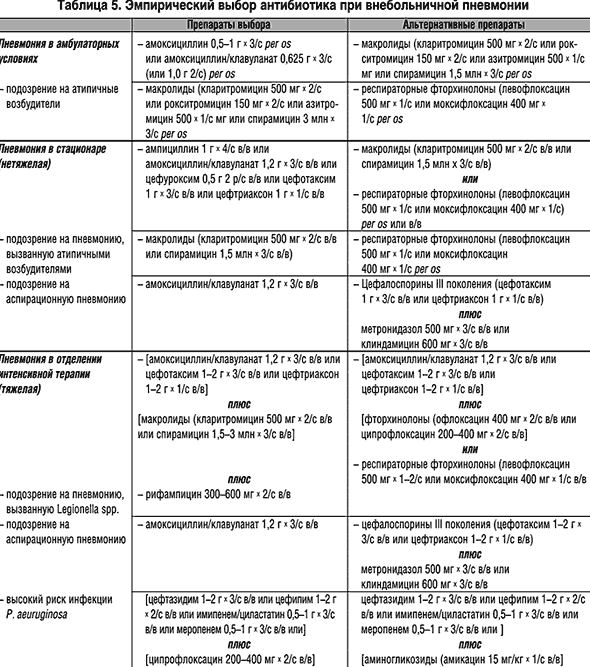
Выбор стартовой терапии зависит от тяжести заболевания, места терапии, клинических и эпидемиологических факторов (табл. 5). Основой терапии легкой пневмонии в амбулаторных условиях являются пероральный амоксициллин 1,0 г каждые 8 часов (4), и амоксициллина/клавуланат 1,0 г каждые 12 часов.
Амоксициллина клавуланат (Амоксиклав) не только оказывает прямое бактерицидное действие на широкий спектр грамположительных, грамотрицательных, аэробных и анаэробных микроорганизмов, включая устойчивые штаммы. В последнее время получены данные о постантибиотическом эффекте и эффекте потенцирования активности полиморфноядерных лейкоцитов и фагоцитоза, выраженных у Амоксиклава достоверно сильнее, чем у амоксициллина. Причем на его примере был впервые описан эффект: клавулановая кислота существенно продлевает постантибиотическое действие амоксициллина.
Амоксиклав хорошо проникает в различные ткани и жидкости организма, достигая в большинстве случаев адекватных антибактериальных концентраций. Период полувыведения для обоих компонентов составляет в среднем около 1 ч. Основная доля препарата выводится через почки.
По сравнению с другими пенициллиновыми антибиотиками Амоксиклав обладает лучшими фармакокинетическими свойствами, в частности, большей биодоступностью при приеме внутрь, возможностью одновременного приема с пищей, молоком, меньшей степенью связывания белками плазмы и др. Эффективность монотерапии (один антибиотик, один курс) в группе Амоксиклава достоверно выше. Необходимо отметить также более низкую антибактериальную нагрузку в группе Амоксиклава, где курс лечения в среднем требует меньших доз.
Также применение орального антибиотика Амоксиклав позволяет получить существенный экономический эффект. Анализ показал, что основное влияние на стоимость лечения оказывают стоимость лечебно–диагностических процедур, инъекций и общая длительность госпитализации больного. Стоимость антибактериальных препаратов играет далеко не ведущую роль. В то же время использование эффективных антибиотиков, наиболее показанных при данной патологии, способствует более быстрой положительной динамике, сокращает длительность антибиотикотерапии и общую продолжительность лечения, что в конечном итоге дает значительный экономический эффект. Относительно более дорогостоящий антибиотик Амоксиклав по сравнению с традиционными препаратами (пенициллин, линкомицин, ампициллин и др.) в итоге оказался более экономичным.
При подозрении на пневмонию, вызванную атипичными возбудителями, назначаются пероральные макролиды. Альтернативой макролидам могут быть респираторные фторхинолоны (лефофлоксацин, моксифлоксацин).
У госпитализированных больных с нетяжелой пневмонией возможно назначение как парентеральных, так и пероральных препаратов. Показаниями к парентеральной терапии являются: тяжелая пневмония, нарушение сознания, нарушение глотательного рефлекса, функциональные или анатомические причины нарушенного всасывания (9). При нетяжелой пневмонии возможно использование амоксициллина/клавуланата, ампициллина, парентеральных цефалоспоринов II и III поколений (цефтриаксон, цефуроксим аксетил, цефатаксим), альтернативными препаратами являются внутривенные макролиды (кларитромицин, спирамицин) или респираторные фторхинолоны. При подозрении на аспирационный генез пневмонии назначают амоксициллина/клавуланат или комбинацию b-лактамов с метронидазолом или клиндамицином.
При тяжелой пневмонии в качестве стартовой терапии назначают комбинацию цефалоспоринов III поколения (или амоксициллина/клавуланата) и макролидов. По данным нескольких ретроспективных исследований, такой режим терапии может сопровождаться снижением летальности, что объясняется не только активностью комбинации препаратов к типичным и атипичным микроорганизмам, но и способностью макролидов уменьшать противовоспалительный эффект бактериальных продуктов (19). Альтернативным режимом является комбинация цефалоспоринов III поколения и фторхинолонов (офлоксацин, ципрофлоксацин). При подозрении на инфекцию Legionella spp. к указанным препаратам добавляют парентеральный рифампицин. При высоком риске инфекции P. aeuruginosa (муковисцидоз, бронхоэктазы), эмпирическая антимикробная терапия должна включать цефалоспорины III поколения с антисинегнойной активностью (цефтазидим, цефипим) или карбапенемы (имипенем, меропенем) в комбинации с ципрофлоксацином или аминогликозидами (табл. 5).
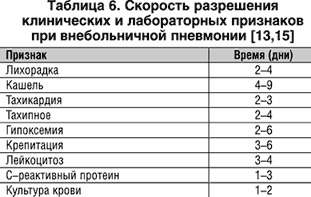
Ответ на антимикробную терапию зависит от иммунной реактивности организма, тяжести заболевания, причинного патогена, протяженности пневмонии по данным рентгенографической картины. Субъективный ответ на антибиотики обычно наблюдают в течение 1–3 суток от начала терапии. Объективный ответ включает оценку лихорадки, других симптомов, лабораторных показателей и рентгенографических изменений. Средняя динамика объективных параметров показана в таблице 6.
После получения адекватного ответа на парентеральное введение антимикробных препаратов возможен переход на пероральные препараты. Такой подход определяют как «ступенчатая» терапия, если используется один и тот же антибиотик, или как «последовательная» терапия, если производится замена одного парентерального антибиотика на другой пероральный препарат. Использование ступенчатой или последовательной терапии позволяет значительно уменьшить расходы на лечение и сократить длительность пребывания больных в стационаре. Пероральный антибиотик при последовательной терапии должен обладать высокой биодоступностью. Для ступенчатой терапии чаще используют макролиды, фторхинолоны, амоксициллин/клавуланат, цефуроксим. При последовательной терапии возможен переход от в/в ампициллина на амоксициллин, от в/в цефалоспоринов на амоксициллин/клавуланат или другие пероральные цефалоспорины (цефподоксим, цефиксим).
Критериями перехода от в/в к пероральной терапии являются:
Разрешение лихорадки > 24 часов
Пульс < 100 мин-1
Разрешение тахипное (ЧД < 20 мин-1)
Хорошая гидратация, способность к приему жидкости per os
Отсутствие гипотензии
Отсутствие гипоксемии
Снижение лейкоцитоза периферической крови
Отсутствие бактериемии
Отсутствие микробиологических данных за инфекции Legionella spp., Staphylococcus aureus и грамотрицательные бактерии
Адекватная абсорбция из желудочно–кишечного тракта
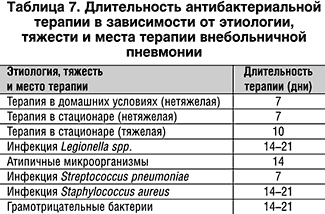
Длительность антимикробной терапии зависит от тяжести заболевания, этиологического фактора, наличия или отсутствия осложнений. Средняя длительность терапии представлена в таблице 7.
Терапия осложнений внебольничной пневмонии
Антибактериальные препараты являются основой терапии больных с пневмонией, однако в ситуации ведения больных с тяжелой пневмонией, важнейшее значение играет терапия, направленная на терапию осложнений пневмонии (острая дыхательная недостаточность, септический шок, абсцесс и др.) (1).
При умеренной гипоксемии (SpO2 85–90%), при условии достаточного респираторного усилия больного, сохраненного сознании и быстрой обратной динамики инфекционного процесса, возможна коррекция гипоксемии при помощи простой носовой маски (FiO2 до 45–50%) или маски с расходным мешком (FiO2 до 90%). Показания в респираторной поддержке рассматриваются на основании клинической картины с учетом газометрических показателей:
нарушение сознания (сопор, кома);
нестабильная гемодинамика;
признаки дисфункции дыхательной мускулатуры;
частота дыхания > 35 мин-1;
рН артериальной крови < 7,3;
РаО2/FiO2< 250 мм рт.ст.
Альтернативой традиционной респираторной поддержке является неинвазивная вентиляция легких (НВЛ) с помощью лицевых масок, НВЛ позволяет улучшить газообмен у 75% больных и избежать интубации трахеи у 60% больных с тяжелой пневмонией. Применение НВЛ при тяжелой пневмонии обосновано у больных с фоновым заболеванием ХОБЛ, при условии хорошего дренирования дыхательных путей и на ранних этапах развития ОДН (1)
Особую сложность представляет проблема проведения вентиляционного пособия больным с ОДН на фоне унилатерального (несимметричного) поражения легких. Предложено несколько подходов для улучшения оксигенации у больного с односторонней пневмонией: использование фармакологических препаратов (альмитрин, ингаляционный оксид азота NO); периодическое придание больному положения на здоровом боку (decubitus lateralis); раздельная вентиляция легких с учетом разного комплаенса и различной потребности РЕЕР в здоровом и «больном» легком (11).
У больных с тяжелым сепсисом и септическим шоком на первом этапе терапии назначают растворы для восполнения объема циркулирующей жидкости (чаще коллоиды). В ряде случаев введения растворов может быть достаточно для коррекции циркуляторных нарушений, в случае их неэффективности назначают допамин, а затем при неэффективности – вазоконстрикторы (норадреналин, адреналин) и инотропные препараты (добутамин) (22). При «рефрактерном» септическом шоке, при подозрении на недостаточность надпочечников (больные с предшествующим приемом стероидов) возможно использование низких доз глюкокортикостероидов (гидрокортизон 100 мг 3 раза в сутки в течение 5–10 дней).
Абсцесс легкого определяется, как локализованный участок некроза ткани легких, приводящий к образованию одиночных или множественных полостей размерами более 2 см (10). Причиной развития большинства абсцессов легких является смешанная флора, причем анаэробная инфекция встречается до 90% случаев, либо как первичный патоген, либо в комбинации с аэробами. Терапия абсцесса легкого слагается из антимикробной терапии и (редко) бронхоскопических и хирургических методов лечения. К основным антибактериальным препаратам, назначаемым при абсцессах легких, относятся: клиндамицин, «защищенные» пенициллины: амоксициллин/клавуланат (Амоксиклав), ампициллин/сульбактам, тикарциллин/клавуланат, клиндамицин. Рекомендуемая длительность антибактериальной терапии больных с абсцессом легких составляет 1–3 месяца.
Дренирование абсцессов часто достигается путем обеспечения хорошей экспекторации мокроты и использования физиотерапевтических процедур (перкуссия, вибрационный массаж), бронхоскопических методов. Хирургическое вмешательство может понадобиться при больших размерах абсцесса (более 6 см) и при осложнениях абсцесса (легочное кровотечение, формирование бронхоплевральной фистулы).
Парапневмонические плевральные выпоты могут значительно различаться по тяжести течения, варьируя от неосложненного выпота до развития эмпиемы плевры. Некоторые формы парапневмонического выпота не требуют специальной терапии, кроме антибактериальной терапии, в то время, как при эмпиеме может потребоваться хирургическое вмешательство. Биохимический анализ плеврального выпота позволяет разграничить три стадии парапневмонического плеврального выпота на основании трех параметров: рН, ЛДГ и глюкозы (16) (табл. 8).

Терапия парапневмонического плеврального выпота прежде всего зависит от его стадии и риска неблагоприятного исхода (13) (рис. 1). При неосложненном выпоте показано наблюдение и антимикробная терапия. При осложненном плевральном выпоте показано проведение торакоцентезов при помощи повторных пункций или установка дренажной трубки. При эмпиеме методом выбора является дренирование плевральной полости. При наличии спаечного процесса в плевральной полости и осумкованных полостей адекватное дренирование плевральной полости может быть достигнуто при введении в нее фибринолитиков, которые позволяют растворить фибриновые сгустки и мембраны. Торакоскопия является альтернативным методом фибринолитикам для терапии осумкованных плевральных выпотов (13).
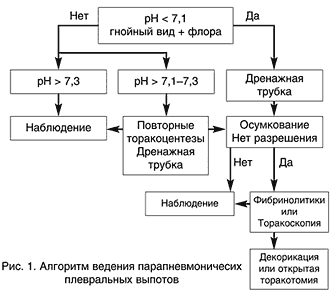
Рис. 1. Алгоритм ведения парапневмоничесих плевральных выпотов
Поддерживающая терапия при внебольничной пневмонии
Больные с пневмонией, госпитализированные в стационар, особенно, в отделения интенсивной терапии, как правило, нуждаются в проведении поддерживающей терапии, которая включает растворы, электролиты, питание, бронхолитики, отхаркивающие препараты. Тяжелым больным, особенно с ОДН, дегидратацией, наличием в анамнезе тромбоэмболий и не имеющим противопоказаний к терапии прямыми антикоагулянтами, для профилактики венозных тромбозов назначают низкие дозы нефракционированного гепарина (п/к 5.000 ед 2–3 р/сут) или, предпочтительнее, низкомолекулярные гепарины (эноксапарин п/к 40 мг/сут) (20).
1. Авдеев СН. Осложнения внебольничной пневмонии. В книге: Пневмония. Под редакцией АГ Чучалина, АИ Синопальникова, НЕ Чернеховской. Москва, Экономика и информатика, 2002: 134–181.
2. Козлов РС, Кречикова ОИ, Сивая ОВ, и кол. Антимикробная резистентность Streptococcus pneumoniae в России: результаты проспективного многоцентрового исследования (фаза А проекта ПеГАС–I). Клин Микробиол Антимикр Химиотер 2002; №3: 267– 277.
3. Навашин СМ, Чучалин АГ, Белоусов ЮБ, и др. Антибактериальная терапия пневмоний у взрослых. Клин Фармакол Терапия 1999; 8(1): 41– 50.
4. Страчунский ЛС. Антимикробная терапия внебольничной пневмонии в условиях поликлиники. С. 341– 363. В книге: Пневмония. Под редакцией АГ Чучалина, АИ Синопальникова, НЕ Чернеховской. Москва, Экономика и информатика, 2002.
5. Чучалин АГ, Синопальников АИ, Яковлев СВ, и др. Внебольничная пневмония у взрослых: практические рекомендации по диагностике, лечению и профилактике. Пособие для врачей. Смоленск 2003, 53с.
6. American Thoracic Society. Guidelines for the initial management of adults with community–acquired pneumonia: diagnosis, assessment of severity, and initial antimicrobial therapy. Am Rev Respir Dis 1993; 148: 1418– 1426.
7. American Thoracic Society. Guidelines for the management of adults with community–acquired pneumonia. Diagnosis, assessment of severity, antimicrobial therapy, and prevention. Am J Respir Crit Care Med 2001; 163: 1730– 1754.
8. Bartlett JG, Dowell SF, Mandell LA, et al. Pracice guidelines for the management of community–acquired pneumonia in adults. Clin Infect Dis 2000; 31: 347– 382.
9. British Thoracic Society. British Thoracic Society guidelines for the management of community–acquired pneumonia in adults. Thorax 2001; 56(suppl IV): iv1– iv64.
10. Cassire HA, Niederman MS. Aspiration pneumonia, lipoid pneumonia, and lung abscess. In: Pulmonary diseases. Ed: Baum GL, Crapo JD, Celli BR, Karlinsky JB. Lippincot–Raven, Philadelphia, New York, 1998: 645– 655.
11. Dreyfuss D, Djedaini K, Lanore JJ, et al. A comparative study of the effects of almitrine bismesylate and lateral position during unilateral bacterial pneumonia with severe hypoxemia. Am Rev Respir Dis 1992; 146: 295– 299.
12. Farr BM, Sloman AJ, Fisch MJ. Predicting death in patients hospitalized for community acquired pneumonia. Ann Intern Med 1991; 115: 428– 436.
13. Fein A, Grossman R, Ost D, Farber B, Cassiere H. Daignosis and management of pneumonia and other respiratory infections. Professional Communications, Inc., 1999: 288p.
14. Fine MJ, Smith MA, Carson CA, et al. Prognosis and outcome of patients with community–acquired pneumonia: a meta–analysis. JAMA 1996; 275: 134– 141.
15. Halm EA, Fine MJ, Marrie TJ, et al. Time to clinical stability in patients hospitalized with community–acquired pneumonia: implications for practice guidelines. JAMA 1998; 279: 452– 1457.
16. Heffner JE. Infection of the pleural space. Clinics Chest Med 1999; 20: 607– 622.
17. Huchon G, Woodhead M. Management of adult community–acquired lower respiratory tract infections. Eur Respir Rev 1998; 8: 391– 426.
18. Ortqvist A. Treatment of community–acquired lower respiratory tract infections in adults. Eur Respir J 2002; 20(Suppl.36): 40s–53s.
19. Rello J, Catalan M, Diaz E, et al. Associations between empirical antimicrobial therapy at the hospital and mortality in patients with severe community–acquired pneumonia. Intensive Care Med 2002; 28: 1030– 1035.
20. Samama MM, Cohen AT, Darmon J–Y et al., A comparison of enoxaparin with placebo for the treatment of venous thromboembolism in acutely ill medical patients. N Engl J Med 1999; 341: 793– 800.
21. Sitbon O, Mercat A, Petitretz P. Pneumopathies aiguёs infectieuses. Salmeron S, Duroux P, Valeyre D (Ed). Pneumologie. Medecine–Sciences. Flammarion, Paris, 1997: p 232– 247.
22. Wheeler AP, Bernard GR. Treating patients with severe sepsis. N Engl J Med 1999; 340: 207– 214.
23. Woodhead M. Community acquired pneumonia in Europe: causative pathogens and resistance patterns. Eur Respir J 2002; 20: 20s– 27s.
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Новые данные иммунных реакций при туберкулезе
- Современные средства патогенетической и симптоматической терапии гриппа и ОРЗ
- Антигипоксанты и антиоксиданты в кардиологической практике
Профессор А.М. Шилов ММА имени И.М. СеченоваКлючевая роль тромбоза артерий сердца в формировании острого коронарного синдрома, вплоть д
- Антибактериальная терапия при острых инфекциях ЛОР-органов
- Постменопаузальный остеопороз - новые подходы к оценке эффективности антирезорбтивной терапии Миакальциком
К.м.н. Н.В. Торопцова, профессор Л.И. БеневоленскаяГУ Институт ревматологии РАМН, МоскваОстеопороз является одной из важнейших проблем з
- Cиндром Марфана в практике терапевта и семейного врача: диагностика, тактика ведения, лечение, беременность и роды
- Диагноз и лечение при болях в спине
Профессор В.А. Парфенов ММА имени И.М. СеченоваБоли в спине – одна из наиболее частых жалоб пациентов в общемедицинской практике. Они за
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

