Коррозия металла
Коррозия стали и цветных металлов принципиально отличается от коррозионных процессов в неметаллических строительных материалах. Большинство так называемых драгоценных металлов, особенно сталь, в большей степени подвержены коррозии, чем неметаллические материалы. Средняя скорость коррозии основных металлов в условиях средне европейского климата представлена в табл. 2.1 Из таблицы видно, что наибольшие потери наблюдаются для обычных сталей. Приведённые данные являются усредненными. Загрязнение, воздуха, особенно вблизи химических заводов, приводит к значительному ускорению процессов коррозии. В результате коррозии происходят необратимые изменения - уменьшение площади сечения и снижение прочности, а также часто изменение внешнего вида поверхности металла.
Химическая коррозия
Химическую коррозию стали вызывают сухие газы и жидкости, не имеющие характера электролитов, например органические соединения или растворы неорганических веществ в органических растворителях, Химическая коррозия не сопровождается возникновением электрического тока. Она основана на реакции между металлом и агрессивным реагентом. Этот вид коррозии протекает в основном равномерно по всей поверхности металла. В связи с этим химическая коррозия менее опасна, чем электрохимическая.
Продукты коррозии могут образовывать на поверхности металла плотный защитный слой, затормаживающий её дальнейшее развитие, или же пористый слой, не защищающий поверхность от разрушающего воздействия среды. В этом случае процесс коррозии продолжается до полного разрушения материала или период времени пока будет действовать агрессивная среда. Наиболее часто на практике встречается газовая коррозия
стали, вызванная воздействием О2 , SO2 , H2S, CI, НС1,
NO3 ,CO2 ,CO и H2 .
Электрохимическая коррозия
Электрохимическая коррозия происходит при взаимодействии металлов с жидкими электролитами, в основном растворами кислот, оснований и солей. Механизм процесса коррозии зависит от структуры металла, а так же от типа электролита. Сталь, как всякий металл, имеет кристаллическое строение, при котором атомы располагаются в соответствующем порядке, образуя характерную пространственную решетку. Кристаллы железа имеют строение, значительно отличающиеся от идеальной схемы, так как имеются пустоты, не занятые атомами металла, трещины, включения примесей к газов .
Металлы обладают хорошей электропроводностью, что обусловлено наличием свободных электронов, движение которых создает электрический ток. Числу свободных электронов соответствует эквивалентное число ион-атомов, т.е. атомов, утративших один или более электрон. В случае возникновения на концах металлического стержня разности потенциалов электроны движутся от полюса с высшим потенциалом к противоположному полюсу. Металлы, обладающие электронной проводимостью, являются проводниками первого рода, а электролиты которые имеют ионную проводимость проводниками второго рода.
Каждый металл имеет так называемую термодинамическую устойчивость, т е. способность ион-атомов переходить в раствор электролита. При погружении какого-либо металла в чистую воду определенное число положительных ионов отрывается от металла и переходит в раствор, оставляя на поверхности металла соответствующее число электронов. В результате этого металл, погруженный в воду, имея избыток свободных электронов, получает отрицательный электрический заряд, а на границе раздела фаз образуется двойной электрический слой.
Положительные ионы (благодаря притяжению зарядов с противоположным знаком) удерживаются вблизи поверхности металла. Возникает поле электрических сил, которое притягивает к металлу ионы, находящиеся в растворе. Однако накопление ионов металла приводит к затормаживанию его дальнейшего растворения. Через некоторое время при определенном потенциале наступает подвижное равновесие.
Если металл погружается не в чистую волу, а в раствор, могут быть следующие случаи:
1. Энергия гидратации раствора недостаточна для нарушения связи между ион-атомами и электронами, При этом на поверхности металла будут накапливаться катионы из раствора, а поверхность приобретает положительный заряд. На границе металл - раствор устанавливается равновесие, а процесс коррозии прекращается.
2. Возможен переход ион-атомов в раствор, так как энергия гидратации больше чем энергия связи в металла. При этом коррозионный процесс протекает беспрепятственно.
Металл, погруженный в электролит, является единичным электродом. Однако абсолютная величина разности потенциалов поверхности металла и соприкасающегося с ним слоя раствора (а следовательно, и склонность металла, из которого выполнен электрод, к коррозии) не поддается измерению. Поэтому за электрод с условным нулевым потенциалом принимается водородный электрод, относительно которого определяются потенциалы всех металлов. Это так называемые нормальные потенциалы. Водородный электрод состоит из пластины, покрытой платиновой чернью, погруженной в раствор НС1 и омываемой водородом.
Нормальный потенциал может быть положительным или отрицательным. Он определяется при составлении элемента, одним электродом которого является водородный электрод, а другим - металл, погруженный в раствор соли этого металла при температуре 25' С и нормальном давлении. Величина потенциала зависит не только от типа металла, но и от концентрации раствора, температуры и давления. Все металлы в соответствии с их нормальными потенциалами, определенными по отношению к водородному электроду, образуют определенный ряд. Этот ряд позволяет определить разность потенциалов, которая возникает между двумя металлами, погруженными н абсолютно чистую, дистиллированную воду.
По положению металла в ряду потенциалов можно сделать вывод о том, что, например, железо при Контакте с медью будет подвергаться ускоренной коррозии. В присутствии же цинка коррозии будет подвергаться не железо, а цинк. Электролитом в этих случаях служить даже следы влаги.
Величина потенциалов, возникающих на электроде зависит не только от металла, из которого выполнен электрод, по в еще большей степени от процессов, имеющих место на электроде.
Как можно видеть, в зависимости от типа и содержания растворённых в воде солей изменению подвергаются не только нормальные потенциалы, но даже положение металла в ряду потенциалов.
Коррозия при действии вод, не содержащих кислород.
Коррозия стали в воде зависит от количества кислорода, имеющего доступ к поверхности металла.
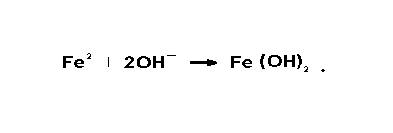
В воде, не содержащей кислорода, коррозия протекает следующим образом : ион-атомы железа переходят в раствор, в результате чего на аноде происходит потеря металла, а его поверхность приобретает отрицательный заряд: Fе, Fе2++2е. Электроды от анода движутся к катоду, В воде носителями тока являются водородные ионы Н+ и гидроокисные ионы ОН- , появляющиеся в результате диссоциации воды. Ионы железа, которые перешли в раствор, соединяются с гидроокисными анионами, образуя плохо растворимый гидрат закиси железа:
Водородные катионы соединяются с электронами, и на катоде выделяется атомарный водород Н++е=Н. 0н образует на поверхности металла защитный слой, уменьшающий скорость коррозии стали (так называемая водородная деполяризация).
В некоторых случаях атомарный водород соединяется в молекулы газа Н+Н — Н2. Пузырьки водорода растут и отрываются от электрода, как только достигнут такой величины, чтобы преодолеть поверхностное натяжение. В этом случае эффект защитного слоя исчезает.
Если сталь соприкасается с раствором с рН>7, водород выделяется в атомарном виде, а следовательно, создаются условия, способствующие образованию защитного слоя. Из растворов же с рН<7 водород выделяется в виде газа.
Интенсивность процесса коррозии н воде, не содержащей кислорода, зависит таким образом от величины pH.
Коррозия при действии вод, содержащих кислород.
В случае когда сталь соприкасается с водой, содержащей кислород, коррозия происходит иначе.
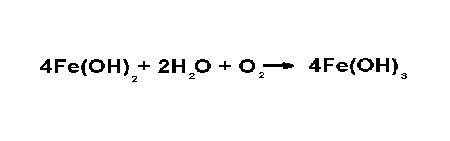
Содержащийся в воде кислород связывает водород, образующий защитный слой на поверхности железа (кислородная деполяризация). А двухвалентное железо подвергается окислению в трехвалентное
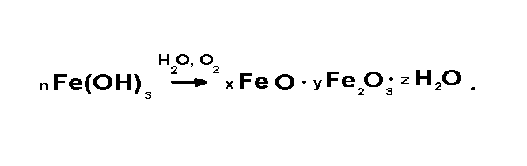
Гидроокись железа в дальнейшем может переходить в гидра тированные окиси (обычно называемые - пучиной)
Продукты коррозии не образуют плотно прилегающего к поверхности металла защитного слоя. Это обусловлено, по-видимому, более чем двукратным увеличением объема которое имеет место при переходе гидроокиси железа в гидрат закиси железа.
Наличие кислорода в воде ускоряет коррозию стали, причем увеличение концентрации кислорода до определенного предела приводит к резкому увеличению коррозионной активности среды. При дальнейшем повышении содержания кислорода скорость коррозии уменьшается в результате пассивации.
Влияние рН на коррозию стали.
Показатель концентрации водородных ионов является вместе с тем показателем активности этих ионов. Низкие значения рН (0 - 7) соответствуют высокой концентрации ионов водорода, которая имеет место в кислых растворах. Значения рН (7 - 14) соответствуют основным растворам с малой активностыо водородных ионов. Следует учитывать, что во всем диапазоне шкалы рН от 0 до 14 потенциал Fе/Fe2+ ниже потенциала водородного электрода. Следовательно, сталь всегда может подвергаться растворению на аноде при одновременном образовании водорода на катоде. При низких значениях рН, т. е. при высокой концентрации водородных ионов, растворы интенсивно разрушают сталь. При значениях рН больше 9 процесс коррозии затормаживается.
Атмосферная коррозия стали.
Наиболее часто встречающимся на практике типом коррозии стали является образование ржавчины под влиянием атмосферных воздействий (чаще всего кислорода и влажности), В сухом атмосферном воздухе сталь практически не подвергается коррозии. Атмосферная коррозия носит электрохимический характер, причем электролитом является слой влаги, имеющийся на поверхности металла.
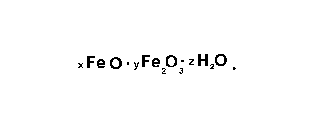
Протекание процессов коррозии в атмосферных условиях аналогично коррозии стали в воде, содержащей кислород. Продукты коррозии, покрывающие металл, представляют собой гидра тированные окиси железа с составом, определяемым формулой
Скорость атмосферной коррозии зависит от содержания влаги в воздухе. Повышение относительной влажности воздуха до 70-75% приводит к сравнительно небольшим потерям стали. При влажности, превышающей эти значения, наблюдается интенсивное ускорение процессов коррозии .
Загрязнение воздуха агрессивными продуктами такими, как СО2, SО2, CI2, H2S, дым и сажа, усиливает коррозию. Сталь, в течение нескольких лет подвергавшаяся воздействию промышленной атмосферы, имеет значительно большие потери, чем сталь в условиях сельской местности .
Ингибиторы
Ингибиторы представляют собой вещества, замедляющие процесс коррозии. Ингибирующее воздействие на металлы, прежде всего на сталь, оказывает целый ряд неорганических и органических веществ, которые часто добавляются в среду, вызывающую коррозию. Ингибиторы имеют свойство создавать на поверхности металла очень тонкую пленку, защищающую металл от коррозии.
Ингибиторы в соответствии с Х. Фишером можно сгруппировать следующим образом:
экранирующие, покрывающие поверхность металла тонкой пленкой. Пленка образуется в результате поверхностной адсорбции. При воздействии физических ингибиторов химических реакций не происходит;
окислители (пассиваторы) типа хроматов, вызывающие образование на поверхности металла плотно прилегающего защитного слоя окисей, которые замедляют протекание анодного процесса. Эти слои не очень стойки и при определенных
условиях могут подвергаться восстановлению. Эффективность пассива торов зависит от толщины образующегося защитного слоя и его проводимости;
катодные, повышающие перенапряжение катодного процесса. Они замедляют коррозию в растворах неокисляющих кислот. К таким ингибиторам относятся соли или окислы мышьяка и висмута.
Эффективность действия ингибиторов зависит в основном от условий среды, поэтому универсальных ингибиторов нет. Для их выбора требуется проведение исследований н испытаний.
Наиболее часто применяются следующие ингибиторы: нитрит натрия, добавляемый, например, к холодильным соляным растворам, фосфаты и силикаты натрия, бихромат натрия, различные органические амины, сульфоокись бензила, крахмал, танин и т. п. Поскольку ингибиторы со временем расходуются, они должны добавляться в агрессивную среду периодически. Количество ингибитора, добавляемого в агрессивные среды, невелико. Например, нитрита натрия добавляют в воду в количестве 0,01 - 0,05%.
Ингибиторы подбираются в зависимости от кислого или щелочного характера среды. Например, часто применяемый в качестве ингибитора нитрит натрия может использоваться в основном в щелочной среде и перестает быть эффективным даже в слабокислых средах.
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Коррозия металлов - проблема химии?
- Крахмал (Доклад)
Министерство Образования Российской Федерации Доклад по Химии на тему Крахмал Выполнил: Ученик 10 кл. Б Нечин Евгений Красноярск, 1998Крах
- Крашение натурального шелка бромакриламидными красителями
- Круговорот веществ в природе
- Курсовая работа по органической химии
Министерство образования российской федерацииСамарский государственный университетХимический факультетКафедра органической химииС
- Курсовая работа по химии. Медь
- Лабораторная работа по химии 1-3 (NPI)
КафедраИнженернойэкологииГИДРОЛИЗ СОЛЕЙ№5Цель работы: изучить условия протекания процессов гидролиза солей и влияние факторов, обусл
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

