Изучение возможности применения магнитных жидкостей для синтеза магнитных сорбентов
1. Обзор литературы
1.1.Магнитные сорбенты
1.1.1. Синтез пористых ферритов с применением выгорающих добавок
1.1.2. Неорганические магнитонаполненные адсорбенты
1.1.3. Углеминеральные магнитные сорбенты
Изотермы адсорбции
1.2.Магнитная жидкость как коллоидная система
1.2.1.Устойчивость магнитных жидкостей
1.2.2.Обзор методов получения магнитных жидкостей
1.2.2.1.Дисперсионные методы получения MЖ
1.2.2.2.Методы конденсации
2. Методика эксперимента
2.1. Синтез магнитного материала
2.1.1. Синтез магнетита
2.1.2. синтез магнетита
2.1.3. Синтез магнитной жидкости с водной дисперсионной средой и стабилизатором олеатом ТЭА
2.1.4.Синтез магнитной жидкости с водной дисперсионной средой и стабилизатором олеатом аммония
2.1.5. Синтез магнитной жидкости с водной дисперсионной средой и минеральными кислотами в качестве стабилизатора
2.1.6. Синтез магнитной жидкости с деканом в качестве дисперсионной среды и стабилизатором олеиновой кислотой
2.1.7. Синтез магнитной жидкости с керосином в качестве дисперсионной среды и стабилизатором олеиновой кислотой
2.2. Синтез магнитного сорбента
2.2.1. Синтез намагниченного сорбента 1
2.2.2. Синтез намагниченного сорбента 2
2.2.3. Синтез намагниченного сорбента 3
2.2.4. Синтез намагниченного сорбента 4
2.2.5. Синтез намагниченного сорбента 5
2.2.6. Синтез намагниченного сорбента 6
2.2.7. Синтез намагниченного сорбента 7
2.3. Методики анализа
2.3.1. Определение содержания Fe(II) при помощи количественного анализа..
2.3.2. Определение содержания Fe(III) при помощи количественного анализа
2.3.3. Определение содержания Fe(II) и Fe(III) в осадке, образующемся при соосаждении гидроксидов при помощи количественного анализа
2.3.4. Упрощенный метод определения поверхности по адсорбции воздуха
2.3.5.Эктронномикроскопическое исследование
2.3.6. Рентгенографическое исследование
2.3.7. Дериватографичеекое исследование
3. Результаты и их обсуждение
3.1. Рентгенофазовое исследование
3.2. Количественный анализ
3.3. Изотермы адсорбции
3.4. Электронная микроскопия
3.5. Удельная поверхность
3.6. Намагниченность
3.7. Дериватографическое исследование
Выводы
Литература
Резюме
Приложение
Введение
Данная дипломная работа посвящена синтезу и изучению магнитных сорбентов, представляющих собой магнитный (либо намагниченный) материал с высокими адсорбционными свойствами.
Преимущество таких адсорбентов по сравнению с обыкновенными (не магнитными) состоит в том, что обладая высокой сорбционной емкостью они могут управляться при помощи магнитного поля. Адсорбенты с магнитными свойствами применяются для контактной очистки веществ, что существенно упрощает адсорбционный процесс и полноту отработки адсорбента, исключает стадию отделения отработанного адсорбента от раствора, являющуюся одной из трудоемких, заменив ее магнитной сепарацией. Магнитные сорбенты уже широко используются для очистки сточных вод, сбора нефти с поверхности водоемов и в медицине (очищают костный мозг и др.) (1-8).
Придание сорбентам магнитных свойств может обеспечить значительное повышение эффективности их использования, поскольку открывается возможность вводить сорбенты в очищаемую среду в виде дисперсной фазы при контролируемой поверхности межфазного контакта и извлекать из среды физическим методом. Известно (8), что придание сорбентам магнитных свойств обычно не снижает емкости и селективности сорбции, а в ряде случаев улучшает эти характеристики, повышая также скорость процесса сорбции – десорбции. Известно также, что магнитные сорбенты способны улучшать ионообменные свойства почв, что указывает на возможность использования материалов данного типа для направленного изменения свойств биологических систем.
Использование данных адсорбентов не ограничивается указанными областями их применения, тем более что они с технологической точки зрения во многих адсорбционных процессах наиболее предпочтительны.
Есть много способов их получения, принципиально отличающихся друг от друга. Большинство из них являются трудоемкими и влекут за собой большие энергетические затраты, что существенно сужает диапазон возможного применения магнитных сорбентов.
На кафедре неорганической химии Белгосуниверситета им. В.И. Ленина в течение нескольких десятков лет проводятся исследования по применению коллоидных систем на основе олова, вольфрама, ванадия, железа и некоторых других металлов для получения пленок и тонких покрытий.
Целью настоящей работы является разработка способа синтеза магнитоуправляемых сорбентов при использовании магнитной жидкости и изучение некоторых их свойств.
Актуальность поставленной в работе задачи подчеркивается потребностью различных областей науки и техники в недорогих магнитоуправляемых сорбентах. Так, магнитоуправляемые сорбенты, используемые для сбора нефти с поверхности водоемов, в медицине и других областях представляют собой дорогостоящие материалы, изготовление которых требует использования сложных технологических процессов и не менее сложного и дорогого оборудования.
Использование именно жидкого материала для пропитки сорбента (и придания ему тем самым магнитных свойств) выгодно отличает предложенный нами способ получения магнитных сорбентов от описанных в литературе (1-7). Применение различных магнитных жидкостей (в отличие от магнетита определенного состава) позволяет в широких пределах варьировать свойства получаемого сорбента.
Автор считает необходимым выразить признательность к.х.н., научному сотруднику Макс Планк института угольных исследований, Мюлхайм ан дер Рур, Германия, Матусевич Н.П. и к.х.н., научному сотруднику Академии Наук Беларуси Самускевичу В.В. за помощь в выполнении физико-химических исследований а также за ценные замечания и пожелания высказанные в ходе обсуждения результатов.
1. Обзор литературы.
1.1.Магнитные сорбенты
1.1.1. Синтез пористых ферритов с применением выгорающих добавок.
Среди большого числа адсорбентов, отличающихся друг от друга структурными параметрами, природой поверхности и соответственно областью применения, особое место занимают пористые тела с магнитными свойствами.
Для решения большинства сорбционных задач требуются адсорбенты с различной пористой структурой, среди которых минеральные пористые вещества занимают основное положение. Во-первых, они во много раз дешевле, доступны и синтез их не требует специального оборудования и дефицитного сырья. Во-вторых, методы получения данных адсорбентов, в том числе и с магнитными свойствами, позволяют в широких пределах регулироватьих структуру. Это свидетельствует о необходимости расширения исследований по синтезу адсорбентов, выявлению закономерностей механизма их структурообразования, природы поверхности, магнитных и адсорбционно-структурных свойств.
Способы получения указанных пористых материалов в зависимости от температуры их синтеза методически могут быть подразделены на две группы. В первой группе они реализованы путем наращивания компонентов шпинельного состава на поверхности коллоидных частиц термостойкого носителя (Т= 700— 750°С) (9), во второй — (Т>750°С) путем применения различного рода выгорающих добавок (10).
Отличие минеральных магнитных адсорбентов от угольных ферромагнитных, как следует из анализа литературы (11-15), состоит в следующем: во-первых, ферромагнитные угольные адсорбенты обладают мелкопористой структурой, что существенно ограничивает область их применения, во-вторых, магнитные свойства высокодисперсных ферромагнетиков вследствие значительной анизотропии формы частиц железа в данных системах, степени их упаковки как в объеме, так и в поверхностном слое, а также при наличии на поверхности частиц хемосорбированных поверхностно-активных веществ снижают магнитные характеристики получаемых адсорбентов (12, 13). В работе (16) показано, что магнитные свойства веществ сильно зависят от упорядоченности активных магнитных частиц, которая для систем с низкой степенью упаковки Р удлиненных частиц сфероидальной формы может быть рассчитана по уравнению (17):
![]()
где Nа и б — размагничивающие факторы вдоль короткой и длинной оси частиц. Оценка Р0 для железных частиц дает величину ~ 0,2 (18).
В-третьих, например, в металополимере для достижения необходимой магнитной индукции насыщения Вs и остаточной индукции Вr, как показано в работах (13, 19), требуется до 30% электролитического железа в. В-четвертых, несмотря на относительно высокое содержание Fe3O4 в образце, в силу вышеупомянутых факторов, достичь предельной величины магнитных свойств, присущих индивидуальному оксиду Fe3O4, не удается. При этом следует отметить, что магнитные свойства массивного индивидуального Fe3O4 по сравнению с другими магнитными материалами не столь высоки.
В отличие от угольных ферромагнитных адсорбентов, синтезированных на основе дорогостоящих синтетических или природных полимеров, минеральные ферриты как по своим магнитным характеристикам, так и по доступности, стоимости исходных компонентов, экологичности процесса имеют ряд преимуществ: наличие высоких магнитных свойств, отсутствие вредных газовых выбросов при их синтезе, компактное расположение магнитных частиц получаемого вещества и т.д. Действие выгорающей добавки (20) заметно сказывается на росте сорбционной емкости, которая по сравнению с исходными образцами увеличилась в два раза.
Влияние исходной структуры гидрогеля с нанесенной шпинельной фазой проявляется в том, что более крупнопористые гидрогели при температуре синтеза ферритов 650°С подвержены меньшим структурным изменениям, чем мелкопористые. Безусловно, степень изменения Vs и Sуд сильно зависит от термостабильности носителя. Одна картина будет иметь место при наращивании гидроксида магния на носитель — коллоидные частицы гидроксида железа и другая — при наращивании Fе(ОН)3 на частицы Mg(OH)2, емкость поглощения и термостабильность которого по сравнению с Vs гидроксида железа примерно в 2 раза выше. Это уже само по себе, не прибегая к применению структурирующих добавок, позволит в определенных пределах варьировать структуру, а соответственно и сорбционные свойства синтезируемых ферритсодержащих адсорбентов.
1.1.2. Неорганические магнитонаполненные адсорбенты
Наряду с изучением адсорбентов-ферритов с развитой пористой структурой представляют интерес адсорбенты с магнитными свойствами, полученные путем механического смешивания или совместного осаждения магнитных порошков с гидроксидами металлов. Этот метод синтеза по сравнению с другими имеет ряд преимуществ. Во-первых, использование магнитных порошков позволяет за счет структуры матрицы регулировать пористость и удельную поверхность синтезируемых магнитных адсорбентов в желаемом направлении. Во-вторых, в зависимости от процентного содержания магнитного порошка в составе образца и величины его намагниченности можно изменять структурные и физико-химические свойства получаемых адсорбентов в достаточно широких пределах.
Кроме того, данный метод получения адсорбентов с магнитными свойствами дает возможность в достаточно широких пределах регулировать структуру матрицы, а соответственно и структурные параметры синтезированных образцов (21, 22). Все это наряду со специфическими свойствами указанных адсорбентов расширяет возможность их использования в разных сорбционных процессах.
Существует расхождение между теоретическими расчетами и экспериментальными данными. По теории с возрастанием концентрации (20-50%) магнитной компоненты Vs и Sуд должна уменьшаться, на практике же наблюдается обратное. Причина таких расхождений обусловлена участием твердых частиц порошка в формировании структуры адсорбентов. Механизм их действия связан с образованием жесткого каркаса, препятствующего сжатию гидроксида во время сушки. Аналогично изменяется и удельная поверхность синтезируемых адсорбентов, которые из-за наличия более открытой структуры несколько выше теоретически рассчитанной.
Условия получения адсорбентов оказывают существенное влияние на их адсорбционно-структурные характеристики. Одна картина наблюдается при внесении магнитного порошка в отмытый гель с последующим механическим перемешиванием и другая — при внесении порошка в солевой раствор, т.е. перед осаждением гидроксида. Разница заключается в том, что образцы, полученные по второму методу, имеют на 10—12% более высокие значения Vs и удельные поверхности. Причина данных расхождений состоит в том, что при механическом перемешивании гидроксида вследствие нарушения гидратных оболочек коллоидных частиц происходит неполная стабилизация системы, сопровождающаяся снятием фактора устойчивости отдельных участков поверхности частиц, в результате чего частицы, слипаясь в этих местах, образуют пространственную сетку, в петлях которой будет находиться дисперсионная среда. При сильном падении агрегативной устойчивости между частицами в местах их соприкосновения может происходить полное вытеснение прослоек дисперсионной среды и осуществляться непосредственный контакт между частицами. Причем с повышением частичной концентрации количество контактов, приходящихся на единицу объема системы, и скорость взаимодействия частиц возрастают.
Увеличение числа контактов между частицами — результат их более плотной объемной упаковки, сопровождающейся, как правило, уменьшением сорбционной емкости и сокращением удельной поверхности образцов за счет недоступности поверхности частиц гидроксида для молекул адсорбата. При совместном осаждении гидрогеля с магнитным порошком протекание указанных процессов весьма ограничено вследствие резкого уменьшения дисперсной фазы и концентрации вещества, а также из-за отсутствия интенсивного механического перемешивания, способствующего образованию коагуляционных структур и т.д.
Все это вызывает формирование пестропористой структуры образцов в результате упаковки первичных частиц и вторичных агрегатов частиц, ответственных за образование мезо- и макропор.
Природа магнитного порошка определяет как магнитные, так и сорбционные свойства получаемых адсорбентов. Если первое из них очевидно, то второе имеет неявные очертания. Дело в том, что удельная поверхность получаемых магнитных адсорбентов практически находится в прямой зависимости от процентного содержания в их составе порошка. Отклонения от этой зависимости могут быть обусловлены некоторым действием порошка на структуру гидроксидов.
Отсюда очевидно, что излишнее содержание магнитного порошка в составе адсорбента ухудшает его структурные параметры и сорбционные характеристики. Основную ответственность за изменение указанных структурных параметров по сравнению с исходными образцами несет магнитный порошок, собственный вклад которого в структуру шпинельсодержащего адсорбента составляет величину, практически приближающуюся к нулю.
С ростом содержания шпинельного порошка в составе адсорбента тенденция сокращения удельной поверхности и сорбционной емкости получаемых образцов по отношению к носителю увеличивается.
Кроме того, адсорбционно-структурные свойства магнитнаполненных адсорбентов, так же, как и других пористых материалов, в значительной степени зависят от структуры носителя, обеспечивающей эффективность очистки жидких сред, содержащих примеси с различным размером молекул.
1.1.3. Углеминеральные магнитные сорбенты
Многообразие задач, решаемых сорбционными методами, требует и разнообразия адсорбентов, отличающихся по структуре, химической природе поверхности и другим эксплуатационным характеристикам.
Синтез таких адсорбентов может быть осуществлен путем наполнения гидроксида магнитным компонентом (10) и модифицирующей органической добавкой (23). Сочетание этих двух операций позволяет, с одной стороны, придать получаемым адсорбентам магнитные свойства, а с другой — гидрофобные и тем самым приблизить их к углеродным адсорбентам со специфическими способностями.
Степень гидрофобизации поверхности таких адсорбентов определяется процентным содержанием и природой органической углеобразующей добавки: с ростом ее молекулярной массы зауглероженность образца увеличивается. Одна из причин этого — более высокая энергия взаимодействия добавки с поверхностью модифицируемого вещества и минимальная ее улетучиваемость в процессе термической обработки.
Гидрофобные адсорбенты с магнитными свойствами расширяют их возможности при решении многих производственных и экологических задач, где использование обычных адсорбентов создает некоторые технологические затруднения. Так, например, аварийные разливы нефти или тяжелых нефтепродуктов на поверхности воды могут быть удалены магнитными углеродными адсорбентами. Для этого достаточно покрыть пятна адсорбентом с последующим удалением его вместе с поглощенным веществом путем магнитной сепарации.
Сопоставление сорбционных данных гидрофильных (10) и гидрофобных магнитнаполненных образцов показывает, что по своим структурным параметрам они отличаются друг от друга. Так, например, сорбционная емкость гидрофобных магнитных адсорбентов выше, чем в аналогичных гидрофильных образцах.
Максимальное внесение органической углеобразующей добавки вызвано требованиями, предъявляемыми к получаемому адсорбенту: среди них необходимая механическая прочность, степень гидрофобизации поверхности и экономический фактор. Каждое требование имеет определенные ограничения, соблюдение которых является неотъемлемой частью синтеза адсорбентов с заданными эксплуатационными характеристиками. Так, например, для получения механически прочных пористых материалов излишнее содержание угля сопровождается потерей механической прочности. Для избежания этого количество органической добавки, адсорбированной на поверхности коллоидных частиц, должно обеспечивать непосредственный контакт между частицами гидроксида, а не через углеродные оболочки. Таким образом, адсорбированный слой модифицирующей добавки в зависимости от ее природы не должен превышать одного или двух молекулярных слоев. В противном случае образуются порошкообразные адсорбенты с сокращенным объемом микро- и мезопор, которые, как было отмечено, полностью или частично закупорены образующимся углем. Данное обстоятельство вынуждает придерживаться золотой середины, которая, помимо сказанного, в некоторой степени определяется и стоимостью модифицирующего агента. Однако трудно предсказать количественное содержание органического модифицирующего агента, необходимого для удовлетворения упомянутых выше требований.
Решение этой задачи обычно осуществляли опытным путем и, как показала практика, содержание модифицирующего вещества в зависимости от его природы, молекулярной массы и дисперсности частиц гидроксида колеблется от 2 до 5 мас.%.
Магнитные характеристики адсорбентов одного и того же состава практически не отличаются между собой. Незначительное присутствие в их составе углеродной компоненты не оказывает заметного изменения ни на магнитную индукцию насыщения, ни на остаточную индукцию.
Иначе говоря, по магнитным параметрам, кроме поверхностных, а соответственно и сорбционных свойств, рассматриваемые пористые материалы не отличаются друг от друга. Поэтому с целью увеличения их разнообразия по структурным параметрам и для повышения эффективности в различных процессах, связанных с очисткой и разделением органических сред, синтез адсорбентов данного типа может быть осуществлен как с использованием структурно отличающихся индивидуальных гидроксидов, так и бинарных систем разного состава.
Для гидрофобных магнитных адсорбентов в отличие от гидрофильных на первый план выступает их структура и ее стабильность при температуре зауглероживания поверхности.
В связи с этим одно из основных требований синтеза магнитных гидрофобных адсорбентов — подбор высокопористых термостабильных носителей. Дело в том, что малоактивные носители, как и аналогичные адсорбенты, не представляют практического интереса, тем более что зауглероживание их поверхности направлено не на развитие, а на сокращение удельной поверхности.
Вторым необходимым условием получения гидрофобных адсорбентов является выбор высокомолекулярного водорастворимого органического вещества — модификатора, обладающего высокой энергией связи с поверхностью коллоидных частиц, и определение его процентного содержания, необходимого для полной гидрофобизации поверхности адсорбента. Это минимальные, но необходимые требования, соблюдение которых — успех синтеза гидрофобных, активных адсорбентов.
Привлекательность данного направления исследований состоит еще и в том, что оно требует разработки принципиально новых методов и нестандартных решений.
Изотермы адсорбции
Изотермы адсорбции являются одной из важнейших характеристик адсорбентов, т.к. при их анализе можно установить многие характеристики сорбента (удельную поверхность, размер пор, предположить их форму, характер сорбции и т.п.).
Для получения изотерм адсорбции очень важен правильный выбор адсорбтива.
Адсорбтив должен быть химически инертным по отношению к поверхности твердого тела; давление насыщенных паров при температуре опыта должно быть достаточно большим, чтобы его можно было точно измерить в соответствующем, довольно широком интервале относительных давлений (~0,001 < р/ро < ~0,5); однако, чтобы удобнее было проводить эксперимент, р0 не должно превышать 1—2 атм. Кроме того, рабочие температуры должны быть такими, чтобы их можно было легко получить при помощи обычных хладагентов, а именно азота (т. кип. 77 К), кислорода (Ткип. 90 К), охлаждающей смеси на основе диоксида углерода (195 К), тающего льда (273 К) или при помощи подходящих термостатов (в интервале от 253 до 323 К). Наконец, желательно, чтобы форма молекул адсорбата не слишком отличалась от сферической, с тем чтобы свести к минимуму неопределенность в величине ат (площадь, занимаемая молекулой адсорбата в плотном монослое)из-за возможной различной ориентации на поверхности. В первое время кислород часто применялся как адсорбат при определении удельной поверхности по методу БЭТ, причем адсорбция измерялась при температуре его кипения. Однако, когда жидкий азот стал вполне доступным, использование кислорода резко сократилось. Помимо того что жидкий кислород как хладагент небезопасен, при температуре 90 К трудно исключить возможность его хемосорбции.
В литературе (26, 83) приводятся десятки тысяч изотерм адсорбции, полученных для самых различных твердых тел.
Существует также несколько теорий, объясняющих вид изотерм адсорбции. Так, например, если происходит хемосорбция (молекулы адсорбтива связываются с частицами адсорбента при помощи химического взаимодействия), то данный вид взаимодействия хорошо описывает теория мономолекулярной адсорбции Ленгмюра. Согласно этой теории, адсорбция молекул адсорбтива происходит на активных центрах, всегда существующих на поверхности адсорбента. Такими центрами могут быть пики и возвышения, имеющиеся на любой, даже самой гладкой поверхности. В результате большой ненасыщенности силового поля около таких пиков и выступов эти участки обладают способностью удерживать налетающие молекулы газа. Вследствие малого радиуса действия адсорбционных сил, имеющих природу, близкую к химической, и способности их к насыщению, каждый активный центр, адсорбируя молекулу адсорбтива, становится уже неспособным к дальнейшей адсорбции. В результате этого на поверхности адсорбента может образоваться только мономолекулярный слой адсорбтива. И изотерма адсорбции примет следующий вид (рис.1).
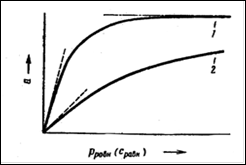
Рис. 1. Обычный вид изотерм адсорбции при различных температурах:
1 — изотерма, отвечающая температуре Т1; 2—изотерма, отвечающая температуре Т2 (Т1< Т2).
Однако, наряду с изотермами адсорбции, вид которых показан на рис. 1, довольно часто на практике встречаются изотермы, не имеющие второго участка, почти параллельного оси давлений и отвечающего насыщению поверхности адсорбента молекулами адсорбтива. Вид таких изотерм изображен на рис.2. Как можно видеть, в точке А изотерма Ленгмюра круто поднимается кверху. Очевидно, связывание адсорбтива адсорбентом не прекращается после образования мономолекулярного слоя, а продолжается дальше. Форму подобных изотерм нельзя объяснить как следствие капиллярной конденсации, так как такая изотерма наблюдается и у непористых адсорбентов, когда капиллярная конденсация невозможна.
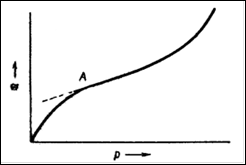
Рис. 2. Вид изотермы, характерной для полимолекулярной адсорбции.
Для объяснения этого явления Поляни предложил теорию полимолекулярной сорбции Рассмотрим кратко исходные положения этой теории, особенно пригодной в случае адсорбции паров на твердом теле:
- Адсорбция обусловливается чисто физическими силами.
- На поверхности адсорбента нет активных центров, а адсорбционные силы действуют вблизи от поверхности адсорбента и образуют около этой поверхности со стороны газовой фазы непрерывное силовое поле.
- Адсорбционные силы действуют на сравнительно большие расстояния, во всяком случае большие, чем размеры отдельных молекул адсорбтива, и поэтому можно говорить о существовании у поверхности адсорбента адсорбционного объема, который заполняется при адсорбции молекулами адсорбтива.
- Действие адсорбционных сил по мере удаления от поверхности уменьшается и на некотором расстоянии практически становится равным нулю.
- Притяжение данной молекулы поверхностью адсорбенга не зависит от наличия в адсорбционном пространстве других молекул, вследствие чего возможна полимолекулярная адсорбция.
- Адсорбционные силы не зависят от температуры, и, следовательно, с изменением температуры адсорбционный объем не изменяется. Это не противоречит тому, что с повышением температуры адсорбция уменьшается; в этом случае снижение адсорбции обусловливается не уменьшением адсорбционных сил, а увеличением в результате нагревания интенсивности теплового движения адсорбированных молекул, что приводит к увеличению десорбции.
Большинство изотерм физической адсорбции можно отнести к одному из пяти типов, от I до V, по классификации, впервые предложенной С. Брунауэром, Л. Демингом, У. Демингом. и Э. Теллером, иногда приписываемой Брунауэру, Эммету и Теллеру (БЭТ) или даже одному Брунауэру . Эти типы изотерм показаны на рис. 3.
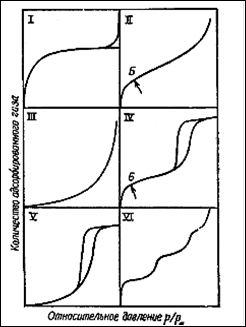
Рис. 3. Пять типов изотерм адсорбции (I—V) по классификации Брунауэра, Деминга, Деминга и Теллера (БДДТ) и ступенчатая изотерма (тип VI).
Как мы уже отмечали, полимолекулярная адсорбция характеризуетея S-образной изотермой адсорбции (тип II). Однако следует иметь в виду, что кривую аналогичной формы можно получить при адсорбции, осложненной капиллярной конденсацией (тип IV).Точка Б, которой соответствует начало прямолинейного участка, соответствует завершению образования монослоя, так что величина адсорбции в точке Б должна быть равна емкости монослоя. Возможность локализации точки Б зависит от формы изгиба изотермы. Если изгиб крутой, точка Б может быть локализована с хорошей точностью, даже если линейный участок изотермы короткий.
Существует много типов пористых систем. И в различных образцах, и в одном и том же образце отдельные поры могут значительно различаться как по форме, так и по размеру. Особый интерес во многих случаях может представлять поперечный размер пор, например диаметр цилиндрических пор или расстояние между стенками щелевидных пор. Удобная классификация пор по размерам принята Международным союзом по теоретической и прикладной химии (IUPAC) :
Таблица 1 ,
Классификация пор по размерам.
| Название пор | Размеры пор, нм |
Микропоры Мезопоры Макропоры | <2 2-50 >50 |
Эта классификация (табл.1.) основана на следующем принципе: каждый интервал размеров пор соответствует характерным адсорбционным свойствам, находящим свое выражение и изотермах адсорбции. В микропорах благодаря близости стенок пор потенциал взаимодействия с адсорбированными молекулами значительно больше, чем в более широких порах, и величина адсорбции при данном относительном давлении соответственно также больше. В мезопорах происходит капиллярная конденсация; на изотермах наблюдается характерная петля гистерезиса. Макропоры настолько широки, что для них невозможно детально изучить изотерму адсорбции из-за ее близости к прямой р/р0 = 1.
Капиллярная конденсация обусловлена наличием у адсорбента мезопор. Пары адсорбтива конденсируются в таких порах при давлениях, меньших давления насыщенного пара над плоской поверхностью вследствие образования в капиллярах вогнутых менисков. Возникновение этих менисков следует представлять как результат слияния жидких слоев, образовавшихся на стенках капилляра вследствие адсорбции паров. Понятно, что возникновение вогнутых менисков возможно только в том случае, если образовавшаяся жидкость смачивает стенки капилляра.
Явление конденсации не следует смешивать с физической адсорбцией. Элементарная теория капиллярной конденсации не учитывает специфического действия поверхностных сил. Доказательством различия капиллярной конденсации и полимолекулярной физической адсорбции служит и тот факт, что полимолекулярная адсорбция может происходить на плоских поверхностях, тогда как капиллярная конденсация в таких условиях невозможна.
При адсорбции, сопровождающейся капиллярной конденсацией, часто наблюдается явление гистерезиса, когда изотермы адсорбции и десорбции не совпадают.
Предварительное тщательное удаление воздуха из пористого адсорбента обычно очень сильно уменьшает гистерезис. Это как будто подтверждает правильность объяснения гистерезиса адсорбцией воздуха на стенках капилляров. Есть, однако, и другие объяснения этого сложного явления. В частности, гистерезис при капиллярной конденсации может быть объяснен, исходя из формы пор адсорбента. Представим, что адсорбент содержит поры, изображенные на рис. 4.
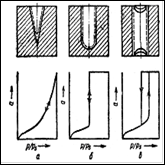
Рис. 4. Схема капиллярной конденсации в порах различной формы: а - конусообразной; б - цилиндрической, закрытой у одного конца; в - цилиндрической, открытой с обоих концов.
При конусообразной форме в порах (см. рис. 4а) oбразуется адсорбционнная пленка с вогнутой поверхностью, причем шаровидная поверхность с максимальной кривизной наблюдается в наиболее узкой части поры. При p = psexp(-2σVмол/(rRT)) пар будет насыщенным по отношению к этой поверхности и начнет конденсироваться. Это приведет к продвижению жидкости и в более широкую часть поры, что, конечно, вызовет увеличение r. Для того чтобы пар продолжал конденсироваться, давление р должно возрастать (см. изотерму на рис. 4а). При уменьшении р жидкость со стен капилляра десорбируется и изотерма пойдет в обратном направлении таким же путем, т. е. капиллярная конденсация в конусообразных порах полностью обратима.
В порах цилиндрической формы, закрытых с одного конца, т. е. имеющих форму пробирки (см. рис. 46), у закрытого конка при адсорбции образуется шаровидный мениск. При p = psexp(-2σVмол/(rRT)) происходит капиллярная конденсация, и в результате этого поры заполняются жидкостью. Однако в отличие от предыдущего случая радиус мениска при этом будет постоянным, и поэтому заполнение пор происходит при постоянном значении р. чему соответствует вертикальная часть изотермы капиллярной конденсации (см. изотерму на рис. 46). Процесс десорбции пойдет в обратном направлении таким же путем, т. е. капиллярная конденсация в цилиндрических капиллярах с одним закрытым концом также вполне обратима. Наконец, в цилиндрических порах, открытых с обоих концов (см. рис. 4в), шаровидный мениск при адсорбции не может образоваться, и конденсация начнется на внутреннем цилиндрическом мениске пленки, покрывающей стенки капилляра, при давлении pц = psexp(-2σVмол/(rRT)). В результате конденсации толщина пленки жидкости увеличивается, а радиус поры уменьшается, и поэтому она заполняет жидкостью при давлении р. Изотерма капиллярной конденсации, как и в предыдущем случае, имеет вертикальный участок (см. изотерму на рис. 4в). Однако вследствие меньшей кривизны цилиндрической поверхности мениска по сравнению с кривизной шаровой поверхности (при одном и том же радиусе капилляра) вертикальный участок на изотерме соответствует большим значениям давления пара. После заполнения поры на обоих ее концах возникнут шаровидные мениски, кривизна которых с повышением давления пара уменьшается. При десорбции процесс вначале пойдет обратимо — при испарении небольших количеств жидкости в устья капилляров будут вдавливаться шаровидные мениски со все возрастающей кривизной.. Однако при p = psexp(-σVмол/(rRT)) эти шаровидные мениски прорваться еще не могут и капилляр при этом давлении останется еще заполненным. Только при снижении давления пара до p = psexp(-2σVмол/(rRT)) радиус шаровидного мениска станет равным радиусу адсорбционной пленки в цилиндрическом капилляре и вся жидкость, заполнявшая капилляр, испарится. Все это обусловит то, что десорбционная ветвь разойдется с адсорбционной, т. е. получится характерная петля капиллярно-конденсационного гистерезиса.
Реальные адсорбенты не обладают порами какого-нибудь одного размера в какой-нибудь одной формы. Их поры заполняются или опустошаются не одновременно. Это является причиной того, что ветви гистерезисной петли обычнонаклонены к оси абсцисс.
1.2. Магнитная жидкость как коллоидная система
Магнитная жидкость представляет собой устойчивую коллоидную систему стабилизированных высокодисперсных частиц магнитного материала в жидкой среде. Обладая одновременно свойствами магнитного материала и жидкости-носителя, она может помочь решить множество научных и технических задач. Диапазон применения индивидуальных магнитных жидкостей необычайно широк. Они используются в космосе и в медицине, для сепарации руд и методов неразрушающего контроля, в магнитожидкостных уплотнениях, демпферах, а теперь и для получения магнитных сорбентов.
Свойства МЖ определяются совокупностью характеристик входящих в нее компонентов (твердой фазы, жидкости-носителя и стабилизатора), варьируя которыми можно в довольно широких пределах изменять физико-химические параметры МЖ в зависимости от конкретных условий их применения.
Процесс синтеза МЖ включает в себя основные стадии: получение высокодисперсных частиц магнитного материала и их стабилизацию в жидкости-носителе. В качестве магнитного материала выбран магнетит. Основное достоинство дисперсии магнетита по сравнению с дисперсиями других ферромагнитных материалов - это технологическая простота и отработанность методик его получения.
1.2.1. Устойчивость магнитных жидкостей.
Магнитную жидкость, включающую в себя в качестве дисперсной фазы высокодисперсные магнитные материалы (железо, кобальт, магнетит, ферриты и т.д.) с размером частиц 50-200 Å, в качестве дисперсионной среды жидкие углеводороды, силиконовые и минеральные масла, воду, фторорганические соединения и т.д., можно отнести к коллоидным растворам или золям.
Устойчивость коллоидных систем - это центральная проблема коллоидной химии, и ее решение имеет огромное практическое значение в геологии, земледелии, биологии, техник
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Изучение кластеров и их свойств в области химии
- Изучение основных закономерностей протекания химических реакций
- ИК-спектральное проявление водородных связей
Литературный обзорСущность и природа водородной связиВодородные связи и свойства органических соединенийМетод инфракрасной спектрос
- Ингибиторы коррозии стали на основе фосфорсодержащих соединений и полиэлектролитов
- Интерполиэлектролитные комплексы
- Использование комплексов полиамфолита этиламнокротонатаакриловой кислоты с поверхностно-активными веществами для извлечения 90Sr
- Использование энергосберегающих технологий для кристаллизации сульфата натрия
Устойчивость объекта в чрезвычайных ситуациях представляет собой способность в условиях чрезвычайной ситуации производить продукцию
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

