Выбор катализатора амидирования и изучение в его присутствии превращения м-толуиловой кислоты в N,N-диэтил-м-толуамид
Проблема получения репеллентов представляет большой интерес, т.к. они отличаются от других пестицидов высокой специфичностью действия, вызывая отрицательный хемотаксис одноклеточных организмов и воздействуя на дистантные или на контактные хеморецепторы животных, преимущественно – насекомых. Потребность в отпугивании москитокровососущих насекомых возрастает в России с каждым годом, а активный антифидинг должен начинаться с ранней весны и продолжаться до наступления холодов, а в странах с тропическим климатом - круглый год.
Используемый арсенал репеллентов (ДЭТА, диметил фталат, бензимин, индалон, дибутилсукцинат, N- бутилацетанилид, бензилбензоат и др.), как правило, представлен азотсодержащими соединениями, из которых высокой эффективностью и изученностью токсилогических свойств выделяется N,N-диэтил-м-толуамид (м-ДЭТА).
Первые сведения об активности этого препарата появились в 1955 году (1), поэтому отечественными учеными он был синтезирован уже в 1956 году (2). Препарат отличался малой токсичностью для теплокровных (ЛД50 для мышей 2500 мг на 1 кг живого веса), но отпугивал клещей, комаров и москитов, причем эффективность его действия против комаров при работе, не связанной с физической нагрузкой, достигала 10ч. Продолжительность защитного действия ДЭТА в 3 раза превосходила таковую диметилфталата и в 1,6 раза – препарат ДИД (смесь, состоящая из 75% диметилфталата, 20% индалона и 5% диметилкарбата).
Впервые ДЭТА был синтезирован в 1929 году (3), и метод базировался на получении хлорангидрида м-толуиловой кислоты, что достигалось при действии на кислоту галоидирующих агентов (PCl5, PCl3 или SOCl2), а реакция сопровождалась выделением агрессивных газов (HCl, SO2). Все последующие синтезы (4-6) также включали стадию получения хлорангидридов и только, по-видимому, в 1960 г. начались первые попытки использовать метиловые эфиры толуиловой кислоты или проводит синтезы с применением традиционных для процессов амидирования алифатических кислот катализаторов (Al2O3, SiO2) (7). Однако стабильность таких катализаторов, несмотря на возможность восстановления их активности после регенерации, не превышала 10-12 ч, хотя селективность могла достигать 80-90%.
Однако, в силу указанной причины, а также трудно на сегодня устанавливаемых факторов, организация производств ДЭТА как в России, так и за рубежом была осуществлена по следующей схеме: м-ксилол – м-толуиловая кислота – хлорангидрид м-толуиловой кислоты – ДЭТА. Однако данный метод является морально устаревшим. Однако до настоящего времени не предложен удовлетворительный катализатор для промышленного синтеза ДЭТА, независимо от природы исходного сырья (м-толуилоая кислота, её сложные эфиры, нитрилы и т.д.).
Несмотря на то, что ДЭТА является ингибитором некоторых полимеризационных процессов (8), катализатором в производстве силиконового каучука (9), растворителей гербицидов (10), основное его назначение, как отмечалось выше, - это бытовая химия (11) и эпидемиология (12). Сказанное диктует жесткие требования к чистоте и цветности продукта, что вынуждает проводить определенные исследования, как по материалу оборудования, так и по поиску эффективных путей отделения м-ДЭТА от параизомеров и м-толуиловой кислоты.
Решение указанной задачи в связи со всеобщим потеплением климата и активизацией, таким образом, насекомых – переносчиком трансмиссивных болезней – является своевременными и актуальными.
Цель работы: выбор катализатора амидирования и изучение в его присутствии превращения м-толуиловой кислоты в N,N-диэтил-м-толуамид.
1. Литературный обзор
Амиды кислот - класс органических соединений, представляющих совершенно определенный интерес как с практической, так и с теоретической точек зрения. Практическая ценность в первую очередь определяется их биологической активностью (гормоны, нейропептиды, антибиотики, токсины, ингибиторы ферментов; вещества, вызывающие хемотаксис микроорганизмов и т.п.) и, во-вторых, наличием пептидной группировки -СО-NH-, присутствующей как в шерсти, так и в некоторых искусственных волокнах в определяющей их теплофизические свойства. Интерес к амидам для фундаментальных химических исследований связан с наличием сопряжения между неподеленной парой электронов атома азота и π-электронами карбонильной группы.
1.1 Общие методы получения амидов органических кислот
Одним из наиболее доступных и в то же время промышленно значимым является метод получения амидов через аммонийные соли карбоновых кислот (13). Последние подвергают сухой перегонке (пиролизу), при этом выход целевого продукта достигает 87-90%.
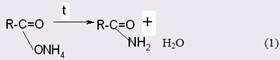
Прямое взаимодействие кислот с аминами в силу обратимости реакции проводят в присутствии избытка одного из реагентов, причем реакция легко протекает только с алифатическими кислотами с неразветвленной цепью, но с трудом - с ароматическими и пространственно затрудненными кислотами или с менее основными аминами (14).
![]()
В реакции принимают участие также вторичные амины, процесс катализируется кислотами. Механизм кислотного катализа относят к типу AAC2 (15) и он близок к перегруппировке Бекмана (16).
Возможность получения замещенных амидов по Бекману в присутствии серной или полифосфорной кислот, PCl5 или других катализаторов характерна для Е-диастереомеров. На примере кетоксимов доказано, что имеет место анти-перегруппировка: группа ОН меняется местами с остатком, находящемся в транс-положении по отношению к ней.
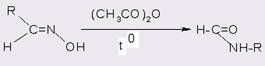
В том случае, когда субстратом выступают сложные эфиры, лактоны или фталиды, в качестве амидирующих агентов можно использовать аммиак или пространственно незатрудненные амины (17). Реакция сложных эфиров с аммиаком катализируется водой, гликолями и другими подобными соединениями (18); аналогичная реакция с аминами промотируется солями, например, NH4Cl (19).
![]()
В зависимости от типа катализатора, используемого при реакции, аминолиз протекает по механизмам AAC2 или BAC2.
Естественно, лактоны и фталиды аналогичным образом превращаются в имиды без раскрытия кольца (20).
В свою очередь действие на ангидриды карбоновых кислот амидирующих агентов (в том числе мочевины и уретанов) протекает обычно без катализаторов
![]()
В случае менее реакционноспособных реагентов (например, дифенил-амина или 2,4-динитроанилина) ацетилирование уксусным ангидридом проводят в присутствии кислотного катализатора (14).
Однако синтезы на основе ангидридов более широко применяются для получения имидов, чем амидов, при этом циклические ангидриды могут давать только имиды, кислые имиды или диимиды в зависимости от реагента и условий эксперимента (21).
Упомянутая несколько выше мочевина может реагировать напрямую с карбоновыми кислотами (синтез по Шербулье (16)).
![]()
Следующий метод - один из наиболее широко применяемых способов получения амидов, по которому выходы последних обычно составляют 80-90%. Отрицательным свойством данной реакции является потеря одного эквивалента амина на связывание высвобождающегося хлористого водорода
![]()
Реакция сильно экзотермична (22), поэтому зачастую ее проводят в растворителях, например, в дихлорэтане (23), четыреххлористом углероде (24), хлороформе (25), толуоле (26) и т.п. Количественному протеканию конденсации способствует присутствие водного раствора гидроксида натрия (27). Механизм ацилирования, как правило, соответствует типу SN2 (28), а реакционная способность агентов симбатна ряду кислотностей соответствующих кислот и убывает в последовательности RCOHal >(RCO)2O ≈ RCOOR > RCONR2 > RCOR. Кроме того, скорость реакция увеличивается с ростом нуклеофильности амина и может осуществляться основной и даже кислотный автокатализ (29).
Целесообразно упомянуть и другие, представляющие синтетический интерес, ацилирующие агенты: кетены, диктены, кетонитрилы, карбамоилхлориды (14). В последнем случае в реакцию могут вступать арены, но в присутствии кислот Льюиса (реакция Гаттермана-Хопфа (16)).
![]()
Представляет интерес путь через нитрилы - вполне доступный класс соединений (16):
![]()
Реакцию проводят с осторожностью, т.к. первичный амид часто подвергается дальнейшему гидролизу до соответствующей карбоновой кислоты и аммиака. Кислоты и щелочи сильно ускоряют реакцию. При кислотном катализе процесс протекает за счет атаки воды на протонированную форму нитрила, в то время как при основном катализе ион гидроксила взаимодействует со свободным нитрилом. В последнем случае в качестве реагента применяют водный раствор NaOH, содержащий 6-12% перекиси водорода, т.к. гидропероксид-анион в несколько тысяч раз активнее гидроксид-иона (14). Ароматические нитрилы дают почти количественные выходы, хотя для о-замещенных нитрилов необходимо применять пергидроль.
Гидролиз до амидов в безводных условиях при комнатной температуре можно проводить в присутствии метилсульфинил метида натрия с выходом 75-95% (30). Альтернативный вариант - это реакция Риттера (31), когда нитрил реагирует с алкенами или спиртами (32):
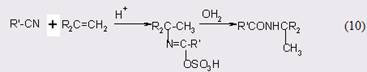
Механизмы реакций превращения нитрилов в амиды достаточно подробно изучены (33), но в данном случае нет необходимости подвергать их анализу.
Таким образом, краткий обзор общих методов получения амидов позволяет сделать некоторые выводы. Все основные методы получения амидов, как правило, могут быть применимы как для алифатических, так и для ароматических членов гомологических рядов. Во всех случаях кроме тех, где реакции принципиально могут протекать чисто термически, процессы катализируют кислотные или основные катализаторы; применяемые гетерогенные контакты также содержат кислотные центры, но преимущественно Льюисовского типа.
1.2 Методы получения N, N-диэтил-м-толуамида
Как указано во введении, до настоящего времени ДЭТА производят по классическому методу, который основан на окислении м-ксилола в м-то-луиловую кислоту, превращении последней в хлорангидрид и последующем ацилировании им N,N-диэтиламина (2).
Из методов модифицирования указанного варианта следует упомянуть работы по совместному получению бензилхлоридов и амидов ароматических кислот (34), когда обрабатывают полностью замещенные бензиламины общей формулы RR’NCH2Ar (R, R’- алкил) хлорангидридом ароматической кислоты ArCOCl, получая при этом ArCONRR’ и ArCH2Cl с выходом 83,5 и 80% соответственно. Преимуществом данного способа является минимальное образование сточных вод и экологически опасных выбросов и получение двух целевых продуктов одновременно. Однако не устранены отрицательные факторы: многостадийность, периодичность и использование хлорпроизводных (фосгена или хлористого тионила).
К новым методам получения ДЭТА относятся следующие: амидирование эфиров м-толуиловой кислоты; совместное с гидролизом амидирование нитрила м-толуиловой кислоты; прямое амидирование м-толуиловой кислоты диэтиламином в жидкой или газообразной фазе.
Амидирование эфиров м-толуиловой кислоты подразумевает предварительную стадию получения эфиров этерификацией кислоты спиртами в присутствии серной, фосфорной или соляной кислот с одновременной отгонкой азеотропа спирт-вода. После нейтрализация кислоты и отмывки полученный катализат подвергают вакуумной ректификации. Таким образом, по сравнению с классическим методом получения ДЭТА, включающим стадию синтеза хлорангидрида м-толуиловой кислоты, синтез алкилового эфира имеет неоспоримое преимущество, но вопросы экологии и очистки сточных вод остаются. Само амидирование диэтиламином проводят в присутствии водоотнимающих катализаторов (35), а в качестве сырья используют метиловый эфир м-толуиловой кислоты в соотношении с диэтиламином 1:3-7 мольн., которые нагревают в автоклаве при температуре 270-280°С в течение 2-8 ч. Избыточное количество амина отгоняют, соль ароматической кислоты с диэтиламином разрушают 30%-ной серной кислотой и после стадии отмывки и нейтрализации извлекают целевой продукт экстракцией толуолом (выход 55%). В тех случаях, когда используют нитрил м-толуиловой кислоты (36). ДЭТА получают с выходом более 90%. Процесс реализуют в автоклаве при температуре 230°С и мольном соотношении реагентов нитрил: алкиламин: вода равном 1:1-1,5:1-2, времени реакции 2-12 ч. В качестве катализаторов используют перекиси, неорганические и органические кислоты и их соли, например, ацетат свинца. В катализатах обнаружены также N-этилтолуамид и м-толуамид при конверсии нитрила 90%, однако процесс многостадиен и не обеспечен сырьевой базой. Наибольшее внимание исследователей посвящено разработке метода синтеза ДЭТА прямым амидированием м-толуиловой кислоты диэтиламином. Действительно, метод прямого амидирования привлекателен уже тем, что это одностадийный процесс, который может быть осуществлен как в периодическом, так и в непрерывном вариантах. Реакция протекает при повышенных температурах в присутствия гомогенного или гетерогенного катализаторов.
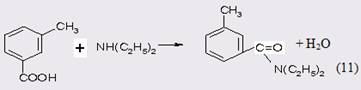
В качестве побочных процессов следует отметить переаминирование и гидролиз:
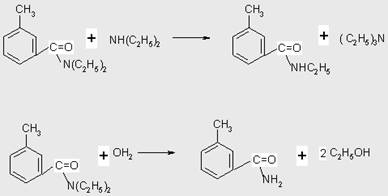
Все процессы прямого амидирования можно разделить на жидкофазные, проводимые в аппаратах периодического действия в присутствии катализаторов на основе титансодержащих соединений (37), фосфорных, полифосфорных, надфосфорных кислот и их солей, фосфорного ангидрида или галогенидов фосфора (38) и комплексных соединений типа (PO N(R)R’)3 (R и R’- C1-C4 ал-килы) (39); и газофазные, проводимые в проточных реакторах над гетеро-генными катализаторами типа оксидов алюминия или силикагеля (35), фосфата бора (40) и т.д.
Получение ДЭТА согласно патенту (37) осуществляют при температурах 150-3000C в отгонно-реакционном режиме. В качестве катализатора используют ТiCl4, Ti(OR)4, в частности Ti (OBu)4, а также катализаторы фирмы Tizor марок ТЕ, АА, OG, LA, представляющие собой внутрикомплексные соединения, например, с триэтаноламином (марка ТЕ) или аммонийную соль лактата титана (марка LA):
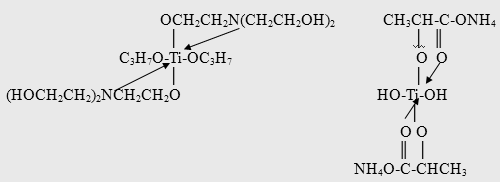
Катализатор вводят в бензольный раствор диэтиламмонийной соли м-толуиловой кислоты в количестве 0,001-0,2 г на 1 г кислоты при мольном соотношении реагентов 1-2:0,5-1 соответственно. Реакция протекает в отгонно-реакционном режиме при 220-240°С в течение 16-24 ч. Реакционную массу обрабатывают горячим щелочным раствором и для улучшения расслоения органического слоя вводят некоторое количество хлорида натрия. Бензольный раствор ДЭТА подвергают ректификации (выход 75%), конверсия кислоты 90-93%; продукт характеризуется чистотой в 95%.
По данным работы (41), лучшие результаты по синтезу ДЭТА достигаются не при использовании хелатных комплексов, а при введении в растворы тетрахлорида или тетрабутоксититана, при этом требуется применение повышенного давления и температуры 150-300°С.
Недостатками этих методов являются низкая конверсия м-толуиловой кислоты, что требует ее нейтрализации, применение растворителей, сложность отделения гомогенных катализаторов. Кроме того, титанаты достаточно коррозионно агрессивны и токсичны.
Применение в качестве катализаторов фосфорных кислот и хлорпроизводных фосфора (38) позволяет достичь 98%-ного выхода ДЭТА при температуре синтеза 250°С и давлении 1 МПа, процесс протекает в автоклаве в течении 6 ч. Катализаторы вводят в количестве 0,01 моля на 1 моль м-толуиловой кислоты, мольное отношение последней к диэтиламину 1:1,5. Применение алкиламидов фосфорной кислоты (39) в отношении к толуиловой кислоте 1-2:3 при 180-200°С к времени реакции 2 ч позволяет достичь выхода ДЭТА в 84%. В данном процессе реакция автокаталазируется фосфорной кислотой, которая образуется в результате разложения катализатора по схеме:
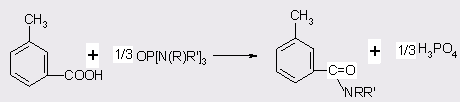
После отгонки органических продуктов H3PO4 может быть выделена и возвращена на стадию получения алкиламидов фосфорной кислоты. Непрореагированная м-толуиловая кислота также легко выделяется кристаллизацией и может повторно использоваться. Недостатком процесса в целом является его двухстадийностъ: синтез катализатора, сопровождающийся образованием кислых сточных вод, и синтез ДЭТА. Использование PCl3 (3) для синтеза алкиламидов не решает указанных проблем: отходами процесса являются солянокислый диэтиламин, кислые сточные воды и моноэтиламид фосфорной кислоты. Реакция протекает при 115-120°С в течение 3-4 ч, в среде толуола. Целевой продукт выделяют из предварительно нейтрализованной реакционной массы перегонкой (выход 89%).
Представляет интерес метод поучения ДЭТА обработкой м-толуиловой кислоты диэтиламином в присутствии солей вольфрамовой кислоты, например, гидровольфрамата аммония (3) В процессе не требуется проводить одновременную отгонку воды, т.к. разлагающаяся при температуре синтеза соль вольфрама уводит воду, превращаясь в нерастворимую H2WO4. При температуре 200-2200C за 8 ч конверсия м-толуиловой кислоты достигает 75% при селективности образования ДЭТА 96%.
Осуществление синтеза в газовой фазе над гетерогенными катализаторами позволяет перейти от периодических аппаратов смешения к непрерывно работающим установкам. В вертикальный реактор, заполненный гетерогенным катализатором, подают раствор диэтиламмонийной соли м-толуиловой кислоты. Катализат, собираемый снизу, подвергают, если необходимо, нейтрализации, далее перегоняют или ректификуют для выделения целевого продукта. В качестве катализаторов используют традиционные системы типа оксидов алюминия или силикагель (3) В этом случае процесс проводят температуре 250-350°С, мольном соотношении м-толуиловая кислота: диэтиламин 1:2-6, времени контакта 0,4-0,8 мин; выход ДЭТА 92-97%. Побочными продуктами являются: этиламин, моноэтилтолуамид, нитрил толуиловой кислоты и другие. Катализаторы этого типа работают эффективно в течение 10-12 ч, после чего необходим отжиг при 400-4500С в токе воздуха. Иногда предусматривают узел испарения м-толуиловой кислоты (42) при 285°С для предварительной очистки кислоты от смол и изомеров, получающихся при ее синтезе. Для извлечения целевого продукта из катализата используют экстракцию и ректификацию.
Для нивелирования направлений реакции, приводящих к образованию побочных продуктов, предлагают применять катализатор под общим названием "фосфат бора" (40) при температуре синтеза 280-290°С, времени контакта 0,5-1 мин (выход ДЭТА 83-84% при конверсии кислоты 80-82%). Способ предусматривает извлечение м-толуиловой кислоты из катализата и возврат ее в цикл.
Из нетрадиционных методов получения ДЭТА достойно упоминания электрохимическое окисление производных бензола общей формулы R1C6H4R2 (R1 и R2- Me или CH(OR)2) в присутствии спирта (43) и триалкиламина, а в качестве электролита применяют 1-70%-ные растворы исходного производного бензола в спирте. Выделенный ректификацией эфир электрохимически амидируют (44). Особенностями таких процессов являются новейшее технологическое оформление химических процессов, повышенная чистота исходных продуктов, возможность создания непрерывного процесса по всей технологической нитке. Однако применение электрохимических методов требует больших энергозатрат и производственных площадей.
Методам аналитического контроля ДЭТА также посвящено несколько работ (45); значительно больший акцент сделан на токсикологических испытаниях, из которых следует упомянуть исследования ориентированные на изучение его действия на организм человека (46).
2. Экспериментальная часть
Спектры ЯМР регистрировали на приборе марки BS 567 А. Рабочая частота для 1Н 100 МГц, 10%-ный раствор м-ДЭТА в CDCL3, внутренний стандарт ГМДС, δ: 1.13 (ушир. Сигнал. 6Н – 2CH3), 2.32 (о, ЗН-CH3-Ar), 3.23, 3.50 (у.с., 4Н – CH2N), 7.16 (м, 4Н - аром. Н). Рабочая частота для 13C 25.142 МГц, 50%-ный раствор м-ДЭТА в CD3CN, расчет относительно известных сигналов растворителя. Спектры снимали в условиях полного подавления спин-спинового взаимодействия (13С – 1Н) и в условиях "off-резонанса", δ: 13.6 (у.к. СН3-СН2), 20.8 (к. CH3-Ar), 40.0, 43.3 (т, CH2N), 123.4, 127.0, 128.5, 129.8 (д.аром. С-Н), 138.4, 139.0 (с, аром.третичн. С), 171.0 (с, С=С-N).
Продукты реакции анализировали методом ГЖХ на приборе ЛХМ-8МД-5 с пламенно-ионизационным детектором, колонка 3 м х 3 мм, заполнена 15% Апиозона L на хроматоне N-AW-DMCS. Температура хроматографирования от 80 до 240°С с программой 8 К/мин, скорость газа-носителя (азот) 20 см3/мин. Стандартная хроматограмма приведена на рис. 2.1. Воду, содержащуюся в катализате, анализировали на приборе ЛХМ-80 с катарометром, колонка 2 м х 3 мм, заполнена 20% ПЭГ 20М на хроматоне, импрегнированном 2,5% КОН. Температура хроматографирования 150°С, скорость газа-носителя (гелий) 40-45 см3/мин, внутренний стандарт – диметилацетамид. Реакцию амидирования изучали в лабораторном проточном интегральном реакторе стандартной конструкции. Раствор м-толуиловой кислоты в диэтиламине (мольное соотношение 1:1-1:7) насосом-дозатором подавали в верхнюю часть реактора, послойно заполненного кварцевой насадкой и катализатором. Обогрев осуществляли электропечью, контроль температуры проводили в трех точках по высоте слоя катализатора хромелъ-копелевыми термопарами. Охлажденные продукты реакции собирались в ловушке, откуда отбирались на анализ. При обработке оксида алюминия минеральными кислотами выявлено, что катализаторы должны эксплуатироваться сразу после стадии сушки. Предварительная прокалка приводит к потере активности либо до уровня немодифицированного Al2O3, либо снижается в еще более значительной степени. Эксплуатация выбранного гидроксилапатита кальция не требует после стадии приготовления дополнительных активационных обработок. Физико-химические характеристики КФ-70: насыпной вес 0,60 г/см3, прочность 1,0 кг/мм, удельная поверхность 80 м2/г, объем пор 0,65 см3/г, кислотность 5 мг-экв./г; структура - широкопористая (сдвиг кривой распределения пор по эквивалентным радиусам до 150 Å). Активность кальцийфосфатных катализаторов в реакциях кислотного катализа пропорциональна количеству групп HPO42-, содержание которых в исследованном нами образце контакта достигало 30%, что близко к теоретически возможному (33,3%). При необходимости проверки кислотности катализаторов на основе оксидов алюминия порошок контакта суспендировали в ацетонитриле и титровали н-бутиламином, за ходом процесса следили потенциометически. Применение Н0-индикаторов не дает лучших результатов.
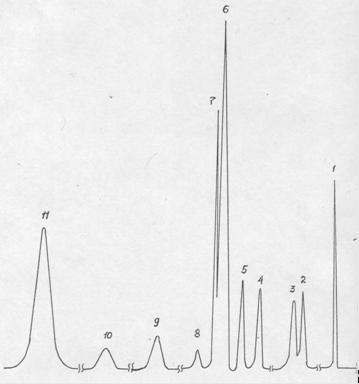
Рис. 2.1. Хроматограмма основных продуктов катализата синтеза м-ДЭТА на катализаторе КФ-70.
1 – диэтиламин, 2,3,8,9,10 – неидентифицированные продукты, 4 – диэтилбензамид, 5- о-ДЭТА, 6 – м-ДЭТА, 11 – тетраэтилизофталамид.
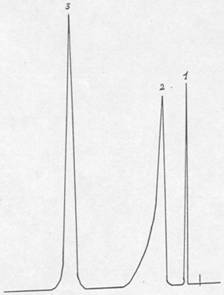
Рис. 2.2. Хроматограмма водных погонов синтеза м-ДЭТА
1 – диэтиламин, 2 – вода, 3 – диэтилацетат (внутренний стандарт)
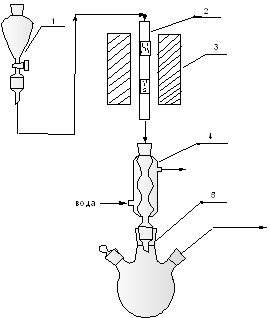
Рис. 2.3. Схема лабораторной установки амидирования в присутствии гетерогенных катализаторов. 1 – бюретка с насос-дозатором, 2 - реактор, 3 – электропечь, 4 - холодильник, 5 – приёмник.
3. Обсуждение результатов. Исследование гетерогенных катализаторов амидирования м-толуиловой кислоты
3.1 Термодинамика процесса
Поскольку реакция амидирования м-толуиловой кислоты (МТК) является обратимой, на первом этапе исследований были изучены термодинамические характеристики процесса. С целью определения состава равновесной смеси и условий, при которых могут быть сняты термодинамические ограничения, на первых порах был проведен расчет констант равновесия при различных температурах в диапазоне 260-320°С для реакции (табл. 3.1).
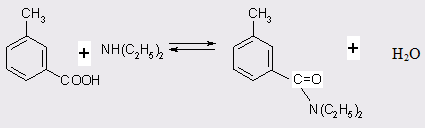
толуамид катализатор кислота токсикологический
Расчет констант равновесия проводился по экспериментальным данным после достижения в статических условиях устойчивых равновесных концентраций компонент (51). В качестве катализатора реакции в данном случае использовали 0,5 мас.% хлорной кислоты. Достижение равновесия при любых температурах определялось только с одной стороны (опыты по гидролизу диэтилтолуамида не проводились).
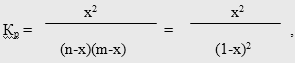
где х - степень превращения МТК или ее мольная доля (52); n и m - мольные доли исходных компонентов (для простоты принято, что n = m = 1).
Обработка полученных значений Кр по методу наименьших квадратов (53) позволила аппроксимировать их следующим эмпирическим уравнением:
Кр = exp(8,81 – 3019,25/Т),
которое, в частности, может быть использовано при синтезе химико-технологических систем на стадии проектирования.
Расчет термодинамически возможной степени превращения при различных температурах и мольных отношениях реагентов осуществлялся по формуле (51)
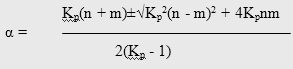
Таблица 3.1 Расчетные значения констант равновесия и термодинамически возможные степени превращения м-толуиловой кислоты при различных условиях синтеза м-ДЭТА
t, 0С | К | Соотношение МТК:диэтиламин | Кр | Степень превращения МТК (α) |
| 260 | 533 | 1:1 1:5 | 21,49 | 0,549 0,880 |
| 280 | 553 | 1:1 1:2 1:5 | 27,96 | 0,840 0,967 0,990 |
| 300 | 573 | 1:1 1:3 1:5 | 36,00 | 0,857 0,986 0,990 |
| 320 | 593 | 1:1 1:2 1:3 1:5 | 40,35 | 0,860 0,970 0,988 0,990 |
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Диэлектрические композиты на основе модифицированного субмикронного титаната бария и цианового эфира ПВС
- Капельный анализ
- Катионы второй аналитической группы
Министерство народного образования РБПрофессиональное училище № 19КУРСОВАЯ РАБОТАТема: « Катионы второй аналитической группы»Обуча
- Расчет ректификационной колонны
- Способы подготовки и очистки газов
В основную группу процессов очистки и переработки газов входят следующие:- Сепарация конденсата – отделение жидкой фазы, выносимой г
- Этические и юридические аспекты применения генных технологий
- Ромашка аптечная
Ромашка аптечная (ромашка лекарственная) — однолетнее травянистое растение из семейства сложноцветных. Стебель прямостоячий, ветвист
Copyright © https://www.referat-web.com/. All Rights Reserved
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

