Витамины В12 и В15
Содержание
Введение Краткий исторический очерк Номенклатура корриноидов Химия витамина В12
Кислотный гидролиз витамина B12
Механизм действия
Некоторые В12-зависимые ферменты
Витамин В15
Клиника
Заключение Список использованной литературы | 3 4 4 6 7 7 8 8 9 9 10 11 11 12 12 13 14 15 16 16 16 17 20 21 23 23 24 24 25 25 25 26 27 27 28 29 29 29 31 31 32 33 34 |
Введение
Lascante ogni speranza voi ch’entrate!
Dante
Витамины (от лат. Vita – жизнь) - группа органических соединений разнообразной химической природы, необходимых для питания человека, животных и других организмов в ничтожных количествах по сравнению с основными питательными веществами (белками, жирами, углеводами и солями), но имеющих огромное значение для нормального обмена веществ и жизнедеятельности.
Первоисточником витаминов служат главным образом растения. Человек и животные получают витамины непосредственно с растительной пищей или косвенно – через продукты животного происхождения. Важная роль в образовании витаминов принадлежит также микроорганизмам. Например, микрофлора, обитающая в пищеварительном тракте жвачных животных, обеспечивает их витаминами группы В. Витамины образуют в организме большое количество разнообразных производных (например, эфирные, амидные, нуклеотидные и др.), которые, как правило, соединяются со специфическими белками, выступая в роли коферментов. Наряду с ассимиляцией, в организме постоянно осуществляется диссимиляция витаминов, причем продукты их распада, а иногда и малоизмененные молекулы витаминов выводятся наружу. Недостаточность снабжения организма витаминами ведет к его ослаблению, резкий недостаток витаминов – к нарушению обмена веществ и заболеваниям – авитаминозам, которые могут закончится гибелью организма. Авитаминозы могут возникать не только от недостаточного поступления витаминов с пищей, но и вследствие нарушения процессов их усвоения и использования организмом.
Основоположник учения о витаминах русский врач Н. И. Лунин установил (1880), что при кормлении белых мышей только искусственным молоком, состоящим из казеина, жира, лактозы и солей, животные погибают. Следовательно, в натуральном молоке содержатся другие вещества, незаменимые для питания. В 1912 году польский врач К. Функ предложил само название «Витамины», обобщил накопленные к тому времени экспериментальные и клинические данные и пришел к выводу, что такие заболевания, как рахит, цинга, пеллагра, бери-бери, - болезни витаминной недостаточности. С этого времени наука о витаминах (витаминология) начала интенсивно развиваться, что объясняется значением витаминов не только для борьбы со многими заболеваниями, но и для познания сущности ряда жизненных явлений. Метод обнаружения витаминов, примененный Луниным (содержание животных на специальной диете – вызывание экспериментальных авитаминозов), был положен в основу исследований.
Оба витамина, которым посвящен этот реферат, впервые были обнаружены в экстрактах печени высших животных. Действие обоих из них связано с переносом метильной группы от одной молекулы к другой, причем пангамовая кислота может являться донором метильной группы, а витамин В12 – промежуточным переносчиком. Однако если относительно принадлежности цианкобаламина к витаминам споров не возникает, то причисление к ним пангамовой кислоты оспаривается большинством ученых. В «Энциклопедическом Химическом Словаре», например, утверждается, что факт принадлежности пангамовой кислоты к витаминам не доказан, Березовский в своей книге «Химия Витаминов» приводит статью о пангамовой кислоте в заключающей книгу рубрике «Некоторые биологически активные вещества». Вообще сведения о витамине В15, доступные мне, оказались весьма скудны и в основном затрагивают вопросы его клинического применения в ущерб химическим свойствам.
Краткий исторический очерк
Витамин В12, пожалуй, самый сложный из всех витаминов, впервые заявил о себе научному миру, когда в 1926-м году американские врачи Джордж Мино и Уильям Мэрфи обнаружили, что включение в состав питания больших количеств полусырой печени оказывает лечебное воздействие при злокачественной анемии. Однако попытки выделения антианемического фактора к успеху не привели. Лишь в конце 40-ых годов Мэри Шорб обнаружила вид бактерий, рост которых зависел от этого фактора, благодаря чему у ученых появилась возможность оценивать содержание витамина в данном субстрате по скорости роста колонии. В 1948 г. Э. Лестер Смит (Англия), а также Эдвард Рикес и Карл Фолкерс (США) получили витамин В12 в кристаллическом виде.
Однако потребовалось еще десять лет для того, чтобы методом рентгеноструктурного анализа определить его структуру, которая оказалась чрезвычайно сложной. За расшифровку структуры витамина В12 (1955 г.) Дороти Ходжкин была присуждена нобелевская премия.
Витамин В15 (пангамовая кислота) был впервые обнаружен в 1950-м году Томиямой в экстракте печени быка. Название пангамовой кислоты происходит от латинских корней «пан» - всюду и «гами» - семя, так как позже она была обнаружена в составе семян огромного количества растений.
Номенклатура корриноидов
Ц
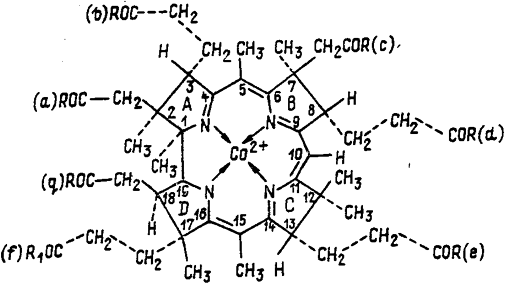
Рисунок 1. Структура корриноидов.
R1=OH – кобириновая кислота; R-NH2; R1=OH – кобировая кислота; R-OH; R1-остаток 1-амино-2-пропанола – кобиновая кислота; R=NH2; R1-остаток 1-амино-2-пропанола – кобинамид; R=OH; R1-остаток D-рибофуранозил-З-фосфата – кобамовая кислота; R-NH2: R1=остаток D-рибофуранозил-З-фосфата – кобамид
ианкобаламин относится к классу корриноидов - производных коррина, структура которого родственна порфирину. Однако, наряду с близостью их структур, имеются два важных химических различия между этими макроциклами. В то время как порфирин содержит систему из 12 сопряженных двойных связей, коррин состоит из частично восстановленных пиррольных (пирролиновых) гетероциклов. Корриновое кольцо содержит 6 двойных связей, входящих в состав линейной сопряженной системы, включающей 12 из 15 атомов, составляющих внутренний контур макроцикла. Корриновое кольцо сужено по сравнению с порфириновым. Если в порфирине каждая пара пиррольных колец отделена метиновыми мостиками, то в коррине кольца А и D соединены непосредственно связью между α-положениями. Поэтому внутренний контур корринового макроцикла содержит на один атом углерода меньше, чем порфириновый.
В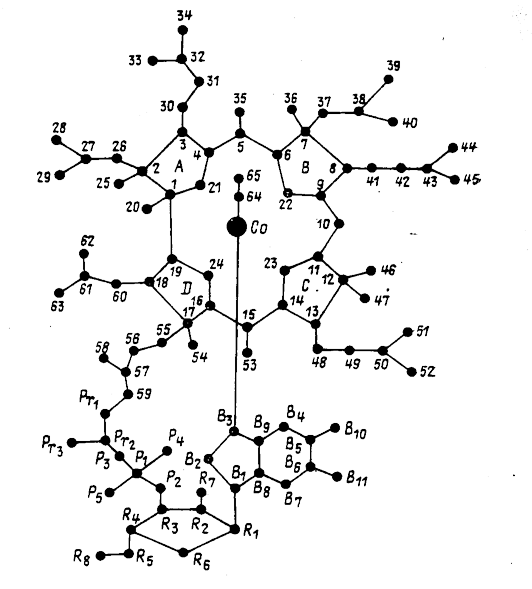
Рисунок 2. Нумерация атомов в молекуле цианкобаламина.
соответствии с номенклатурой корриноидов, утвержденной в 1975 г. Международной комиссией по биохимической номенклатуре, органический экваториальный лиганд, состоящий из четырех восстановленных пиррольных колец с атомом кобальта в центре, назван коррином, а соединения его содержащие - корриноидами. Гептакарбоновая кислота, изображенная на рис. 1, названа кобириновой кислотой. Карбоксильные группы обозначены буквами а-g, как показано на этом рисунке. a,b,c,d,e,g-гексаамид кобириновой кислоты назван кобировой кислотой. Кобиновая кислота является амидом кобириновой кислоты с D-1-амминопропанолом-2 в положении f; его гексаамид назван кобинамидом. Кобамовая кислота является фосфодиэфирным производным кобиновой кислоты, в котором гидроксил 2 положения аминопропанола замещен остатком α-D-рибофуранозил-З-фосфата; его гексаамид назван кобамидом. Кобамиды, которые имеют 5,6-диметилбензимидазольный лиганд, связанный гликозидной связью через N1 с С1 рибофуранозы, называются кобаламинами. Корриноиды, имеющие в α-аксиальном положении вместо 5,6-дииметилбензимидазола другие основания, также называются кобамидами.
Химия витамина В12
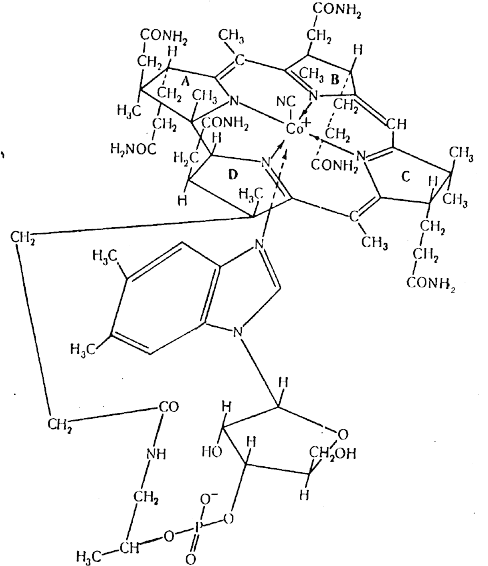
В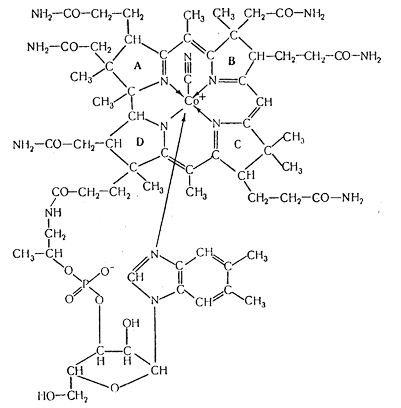
Рисунок 3. Структура цианкобаламина.
итамин B12 кристаллизуется в виде темно-красных игл или призм; цвет варьирует в зависимости от величины кристаллов. Кристаллы темнеют при 210-220°, но не плавятся при температуре ниже 3000Ц. Первыми установленными константами были показатели преломления, а именно α = 1,616, β = 1,652, γ = 1,664. Кристаллографические измерения показывают, что кристаллы относятся к орторомбической системе и имеют призматическую форму. При кристаллизации из водного раствора и из смеси воды с ацетоном они содержат значительное, но изменчивое количество непрочно связанной кристаллизационной воды. Ее можно удалить нагреванием при пониженном давлении, причем кристаллы не теряют своей формы. После этого обезвоженный материал может снова поглощать влагу из атмосферного воздуха в количестве 10-12%; это и есть тот продукт, который обычно выпускается под названием витамина B12 и зарегистрирован в фармакопеях Англии и США. Витамин B12 довольно хорошо растворим в воде (около 1,2% при комнатной температуре), а также в низших спиртах, в низших алифатических кислотах и в фенолах, но нерастворим во многих других органических жидкостях. Он практически не растворяется в пиридине и других третичных аминах, но растворим в некоторых жидких или расплавленных амидах, например в ацетамиде и диметилформамиде. Витамин является левовращающим веществом, но интенсивная, окраска затрудняет измерение оптического вращения. Витамин B12 обладает диамагнитными свойствами, что указывает на трехвалентное состояние кобальта.Обычно витамин выделяют из микробной массы или животных тканей, используя растворы, содержащие цианид-ионы, играющие роль шестого лиганда кобальта. Однако сам цианкобаламин метаболически не активен. В состав ферментов входит соединение, в котором цианогруппа замещена остатком 5-дезоксиаденозина или метильным радикалом.
Строение
Признанная формула витамина B12 –C63H88O14N14PCo. Молекулу можно подразделить на две основные части, известные как "планарная группа" и "нуклеотид"; вторая часть лежит в плоскости, почти перпендикулярной к плоскости первой части, которая обладает очень большим, хотя и неполным, сходством с порфиринами Центральный атом кобальта соединен с четырьмя восстановленными пиррольными кольцами, образующими макрокольцо. Три из четырех соединений между кольцами образованы мезоуглеродным атомом (углеродным мостиком), характерным для порфиринов. Однако в четвертом месте соединения существует прямая связь между двумя α-углеродными атомами колец D и А. Макрокольцо содержит 6 сопряженных двойных связей, образующих единую сопряженную систему.
У 13 из 19 углеродных атомов, составляющих макрокольцо, водород полностью замещен метильными группами или длинными боковыми цепями – либо ацетамидными, либо пропионамидными радикалами
В отличие от нуклеотидов нуклеиновых кислот так называемый нуклеотид витамина B12 не содержит пурина или пиримидина. Вместо них основанием служит 5,6-диметилбензиминазол. Сахар представлен рибозой, но с α-гликозндпой связью, опять-таки в отличие от β-связи в нуклеиновых кислотах. Рибоза фосфорилирована при 3-м атоме углерода. Фосфат образует эфирную группу с 1-амино-2-пропиловым спиртом, который, кроме того, соединен амидной связью с цепью пропионовой кислоты при кольце D. Наконец, атом кобальта несет CN-группу (в цианкобаламине) и соединен координационной связью с одним из атомов азота в бензиминазоле, образуя, таким образом, второй мостик между двумя частями молекулы. Полагали, что третий гидроксил фосфатной группы тоже этерифицирован, пока не стало ясно, что неустойчивость триэфиров фосфорной кислоты исключает такую структуру. Витамин B12 является по существу внутренней солью; отрицательный заряд на атоме фосфора нейтрализован положительным зарядом на координационном комплексе кобальта.
Кобаламины
Первые химические данные о витамине B12 содержались в одновременных сообщениях из лаборатории Глаксо и Мерка, в которых указывалось на присутствие в его молекуле кобальта и фосфора. Самые ранние английские публикации касались второго красного фактора, появляющегося на хроматограммах наряду с витамином B12; Этот фактор был получен в кристаллическом виде Пирсом и его Сотрудниками в лаборатории Ледерле и был назван витамином B12b. Тем временем исследователи из лабораторий Мерка описали витамин В12а как вещество, образующееся при обработке витамина В12 водородом в присутствии платинового катализатора. Позже он оказался идентичным витамину В12b.В лабораториях Глаксо было описано еще одно родственное соединение – витамин B12c. В 1950 г. отношения между этими "витаминами B12" выяснились в результате почти одновременных сообщений из лабораторий "Органон" (Голландия) и Мерка, в которых было показано, что витамин B12 содержит группу цианида, соединенную координационной связью с кобальтом. Группу цианида можно было удалить фотолизом или путем восстановления в определенных условиях с выходом витамина B12a, который, как предполагали, содержит на месте цианида гидроксильную группу. При обработке водным раствором цианида витамин B12a быстро превращается в тот пурпурный дицианидный комплекс, который возникает из самого витамина B12. После подкисления вторая группа цианида теряется и остается витамин B12. Для всей молекулы B12, исключая группу цианида, был предложен термин "Кобаламин", так что витамин B12 стал называться цианкобаламином, а витамин B12a оксикобаламином. Эта терминология получила широкое признание.
Путем обработки витамина B12a различными кислотами удалось получить ряд других аналогов. К ним относится витамин B12c, содержащий группу азотистой кислоты; он был назван нитриткобаламином, или нитрокобаламином. По-видимому, витамин B12a обычно существует не в форме оксикобаламина, а в форме аквокобаламина, молекула которого содержит нейтральную молекулу воды, что сообщает всему координационному комплексу основные свойства; это согласуется с данными о том, что соединение титруется как основание. Можно получить другие основные кобаламины, содержащие вместо воды молекулу аммиака или некоторых аминов. Кроме этих основных и нейтральных соединений, существует еще класс кислых кобаламинов. Из них наиболее известно пурпурное вещество, образующееся при добавлении избытка цианида, к витамину B12. Оно содержит 2 молекулы цианида, соединенные координационными связями с кобальтом. Бивен и сотр. получили довольно убедительные спектроскопические данные о наличии координационной связи между свободным атомом азота в бензиминазоле и кобальтом. Избыток цианида разрывает ее, по-видимому, потому, что ион цианида образует с металлом более прочную координационную связь. Дицианосоединение, однако, устойчиво только в щелочном растворе. Дицианкобаламин легко замещает цианогруппу на ОН-, NO2-, SO3-, Cl-, Br-, SCN- и пр. Все производные в присутствии цианид-ионов превращаются в цианкобаламин.
Устойчивость и взаимопревращения различных классов Кобаламинов изучали с помощью изотопов и другими методами. Все эти вещества без исключения превращаются в витамин B12 под действием цианида. Неудивительно поэтому, что все они обнаруживают биологическую активность в отношении микроорганизмов, а также животных и больных пернициозной анемией, хотя некоторые из них менее активны, чем цианкобаламин.
До сих пор мы рассматривали витамин В12 как нейтральное вещество, хотя в действительности это чрезвычайно слабое основание. Это обнаружилось еще в ранних исследованиях при титровании в растворах уксусной кислоты.
Кислотный гидролиз витамина B12
При обработке витамина B12 неорганическими кислотами в различных условиях получено много продуктов расщепления. Одним из первых был идентифицирован аммиак, образующийся при гидролизе амидных групп. Химическое изучение концентратов антипернициозного фактора привело к предположению, что он представляет собой вещество полипептидной природы. Однако при исследовании кислотных гидролизатов обычным методом хроматографии на бумаге в чистых образцах кристаллического витамина не нашли никаких признаков наличия α-аминокислот. Тем не менее, группа исследователей из Британской палаты медицинских препаратов обнаружила на хроматограмме пятно, дающее нингидриновую реакцию*; эта реакция была обусловлена не аминокислотой, а пропаноламином.
При взаимодействии с концентрированной HCl при 65оС происходит отщепление нуклеотида и образование кобинамида (фактора В – см. ниже), затем происходит отщепление и образование кобировой кислоты (фактора V1a).
Нуклеотид
При кислотном гидролизе витамина B12 в жестких условиях образуется 5,6-диметилбензиминазол. Было показано, что полностью нуклеотид соответствует названию 1-α-D-рибофуранозид-5,6-диметилбензиминазол. Сомнительным оставалось только то, в каком положении - 2 или 3 - фосфорилирована рибоза. Окончательно этот вопрос был решен лишь с помощью рентгеноструктурного анализа.
Продукты мягкого кислотного гидролиза
В первом приближении, мягкий гидролиз разбавленной хлороводородной кислотой приводит к частичному дезаминированию, последовательному образованию моно-, ди-, три-, тетра-, пента-, гекса-, гептакарбоновых кислот с сохранением нуклеотида.
Продолжительная обработка витамина B12 холодной разведенной соляной кислотой приводила к медленной потере микробиологической активности, при этом интенсивность красной окраски не изменялась. Было обнаружено, что с увеличением длительности гидролиза возникает все более сложная смесь продуктов. Среди них одно-, двух-, трех- и четырехосновные кислоты, образующиеся при последовательном удалении аммиака из амидных групп. При добавлении азотистой кислоты в этих условиях образовывались также небольшие количества пяти- и шестиосновных кислот, обладающих красной окраской. Монокарбоновые кислоты можно разделить на три. Дикарбоновые кислоты также разделяются на три изомера; трикарбоновые кислоты фракционировать не удавалось. Этого и следовало ожидать при случайном гидролизе трех лабильных амидных групп. Относительные количества получаемых изомеров показывали, что одна из этих групп значительно лабильнее остальных. Три остальные амидные связи гидролизовались только при обработке кислотой в более жестких условиях или при каталитическом воздействии азотистой кислоты. Когда в результате рентгеноструктурного анализа строение витамина было выяснено, появилась возможность истолковать эти наблюдения. Три лабильные амидные группы, очевидно, принадлежат трем цепям пропионамида, а три стабильные группы - ацетамидным цепям.
Это описание продуктов кислотного гидролиза упрощено, так как, за исключением случаев самого мягкого гидролиза, при электрофорезе выявлялась еще одна группа кислот. Эти кислоты образуются в результате отщепления не только ряда молекул аммиака, но также и нуклеотида.
В водном растворе при мягком кислотном гидролизе (а также фотолитически или при каталитическом гидрировании) цианкобаламин, через промежуточную стадию В12r (см. Восстановление витамина В12) с последующим окислением кислородом воздуха переходит в оксикобаламин.
Фактор В
Исследователи из лаборатории Глаксо нашли, что молекулу витамина можно аккуратно разделить на две части кратковременным нагреванием с концентрированной соляной кислотой или, еще лучше, с хлорной кислотой. При тщательно контролируемых условиях (например, 5 мин при 65°) амидные группы почти не подвергались гидролизу и главными продуктами были, нуклеотид и неизмененная остальная часть молекулы. Последний продукт сохранял микробиологическую активность и оказался идентичным природному фактору, выделенному из содержимого рубца жвачных. В присутствии цианида растворы этого вещества имели пурпурную окраску даже при слабо кислой реакции среды. Спектр поглощения был очень сходен со спектром дицианкобаламина, так что в этом состоянии вещество почти наверное содержало два остатка цианида, соединенных координационной связью с кобальтом. Однако в то время как дицианкобаламин имел кислотные свойства, новое соединение было нейтральным. Причина такого различия состояла в отщеплении кислого нуклеотидного остатка. Это наблюдение по существу явилось главным основанием для представления о витамине B12 как внутренней соли.
Ряд кислот, образующихся при гидролизе амидных групп в факторе В, обладал той же относительной стабильностью в их дициано-конфигурации.
Были получены указания на то, что существует 7-я карбоксильная группа, связанная не с аммиаком, а через амин с нуклеотидом. Это подтверждало более раннее предположение о том, что аминопропиловый спирт служит мостиком между двумя частями молекулы, будучи соединенным амидной связью с одной из цепей пропионовой кислоты в планарной группе и эфирной связью - с фосфорной кислотой. В кислых растворах (с рН примерно менее 3) фактор В теряет обе группы цианида и ведет себя как основание. Соответствующие кислоты ведут себя сходным образом, так как карбоксильные группы не подвергаются заметной ионизации. Поэтому все вещества, не содержащие нуклеотида, можно отделить от веществ, еще сохранивших его.
Щелочной гидролиз
Жесткий щелочной гидролиз приводит к отщеплению 5,6-диметилбензимидазола и образованию дилактампента- и монолактамгексакарбоновых кислот.
П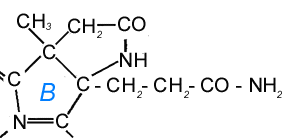
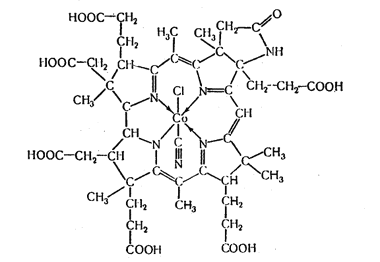
Рисунок 4. Рисунок 4. Дегидровитамин В12 (Строение кольца В корринового макроцикла и прилегающих к нему структур)
Рисунок 5. Гексакарбоновая кислота, образующаяся при щелочном гидролизе.
ри обработке витамина B12 перекисью водорода и разведенной щелочью на холоду и получаются микробиологически активные кислые продукты красного цвета. Реакция состоит в гидролизе, катализируемом перекисью водорода. Однако полученные кристаллические продукты, по-видимому, представляли собой смеси моно- и дикарбоновых кислот, образовавшихся в результате мягкого гидролиза, с неизмененным витамином B12, который обусловливал их биологическую активность. Под действием холодной разведенной щелочи, по-видимому, образуются те же продукты, что и при мягком кислотном гидролизе. Однако в присутствии горячей щелочи реакция идет по-иному. Если нагревать витамин B12 в растворе NaOH в отсутствие кислорода, то окраска становится коричневой, а затем приобретает зеленоватый оттенок, это может указывать на уменьшение валентности атома кобальта, сопровождающееся окислением какой-то другой части молекулы. При доступе воздуха цвет снова становится красным. Кратковременное кипячение со щелочью при доступе воздуха дает в качестве главного продукта нейтральное кристаллизующееся красное вещество. Оно почти неотличимо от витамина B12 по физическим свойствам, но не обладает микробиологической активностью. Структура этого соединения была выяснена главным образом путем рентгеноструктурного анализа кристаллов. Продукт, по-видимому, содержит лактамное кольцо, имеющее 2 общих атома с кольцом В и образующееся из ацетамидной цепи; остальная часть молекулы такая же, что и в самом витамине. Добавление тиогликолата натрия или цианида натрия к раствору витамина в основном защищает его от воздействия щелочи и кислорода. Полагают, что реакция протекает при участии свободных радикалов. Производное, содержащее лактам, было названо дегидровитамином B12. Лактамное кольцо чрезвычайно устойчиво и при дальнейшем воздействии щелочи сохраняется. При гидролизе последовательно отщепляются остающиеся амидные группы и нуклеотид. Таким образом, получаются два ряда кислот – с нуклеотидом и без нуклеотида, - но все они отличаются от соответствующих продуктов кислотного гидролиза. Конечным продуктом щелочного гидролиза является гексакарбоновая кислота, а не гептакарбоновая, как при кислотном гидролизе. Это связано с участием одной из потенциальных кислотных групп в построении лактамного кольца. Основное значение этого кристаллического продукта распада состоит в использовании его для рентгеноструктурного анализа.Продукты окисления
Исследование гидролиза дало ценные сведения о том, что можно было бы назвать периферией молекулы. Гораздо труднее оказалось изучить химическими методами структуру части молекулы, непосредственно окружающей атом кобальта. Кембриджская группа показала, что среди продуктов окисления витамина B12 нельзя обнаружить амида м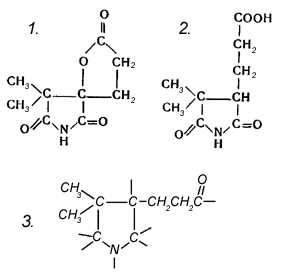
Рисунок 6. Продукты окисления.
алеиновой кислоты, так что вряд ли можно было относить витамин к истинным порфиринам. Но эти исследователи выделили в довольно большом количестве оксамовую кислоту. Единственные азотсодержащие продукты расщепления "ядра" молекулы выделили в 1955 г. Фолкерс и сотр. Контролируемое окисление хроматом натрия в уксусной кислоте привело к образованию двух продуктов, изображенных на рисунке 6 (1 и 2). Полагали, что они образуются из группировки, имеющей пирролидиновую, пирролиновую или пирролениновую структуру (рис. 6, 3). Это были первые химические данные, указывающие на присутствие пирролоподобной структуры в молекуле, если не считать более ранних данных по пиролизу, позволявших предполагать такую структуру. Несколько позже был выделен и соответствующий продукт, содержащий амидную группу (амид кислоты, представленной на рис. 6, 2). Это явилось прямым химическим подтверждением местоположения по крайней мере, одной из амидных групп.При окислении цианкобаламина Н2О2 в среде с рН меньше семи наблюдается выход продуктов, обладающих антагонистическим биологическим действием для lactobacillus leichmannii, в отличие от ростового для Euglena gracilis. При окислении перманганатом калия отщепляется синильная кислота, а также образуются уксусная кислота, щавелевая кислота и ее амид, бутандиовая кислота, 2-метилбутандиовая и 2,2-диметилпропандиовая кислоты.
Восстановление витамина B12
При каталитическом гидрировании на платиновом катализаторе цианкобаламин присоединяет пять атомов водорода и отщепляет метиламин, кобальт переходит в двухвалентное состояние с образованием т. н. В12r. При длительном восстановлении и при использовании более сильных восстановителей, таких как ацетат хрома при рН 9,5 или борогидрид натрия получают так называемый В12s, содержащий одновалентный кобальт.
Восстановление внесло разочаровывающе малый вклад в наши знания о строении витамина, и даже теперь детальная структура продуктов восстановления еще достаточно не выяснена. Обработка водородом в качестве катализатора или некоторыми другими восстановительными агентами вызывает переход окраски в коричневую и, наконец, в серо-зеленую. Эти изменения, за исключением потери цианида, обратимы при контакте с кислородом воздуха, причем образуется витамин B12а. Вопрос об изменениях валентности кобальта, происходящих при восстановлении. Работа Бивена и Джонсона, появившаяся после опубликования предположительной структуры витамина, пролила некоторый свет на не решенный еще вопрос о том, содержит он 5 или 6 сопряженных двойных связей.
Обратимое восстановление легко продемонстрировать, добавляя к щелочному раствору витамина B12 тиогликолевую кислоту. Красная окраска медленно переходит в оранжево-бурую; после встряхивания раствора в присутствии воздуха она тотчас же вновь становится красной. По мере использования кислорода снова медленно появляется цвет восстановленного витамина B12. Эти изменения окраски можно повторно вызывать почти до бесконечности: окончательный результат состоит в том, что витамин катализирует окисление тиогликолевой кислоты (по-видимому, до дисульфида) кислородом воздуха.
Реакция с галогенами
Хлор обесцвечивает раствор цианкобаламина, другие галогены – нет. Продуктом хлорирования является фиолетовое кристаллическое вещество.
Энергичное хлорирование витамина B12 давало продукт, содержащий 30% хлора, природа его не была охарактеризована точнее. Петров и сотр. описали ряд продуктов, образующихся при обработке витамина хлором или хлорамином Т, которые можно было разделить методом хроматографии. Эти вещества имели пурпурный цвет, переходящий при избытке цианида в голубой, и содержали 2 атома хлора в молекуле.
Воздействие одной молекулы хлорамина Т или брома дает в качестве главного продукта нейтральное кристаллизующееся вещество красного цвета. По физическим свойствам оно было очень сходно с витамином B12, но не обладало микробиологической активностью. Электрофорез и инфракрасная спектроскопия доказали, что это был лактон; полагают, что его строение идентично строению лактама показанного на рис. 5, только вместо NH следует поставить О. Образование лактона, по-видимому, связано с промежуточным образованием иона карбония в активированном β-положении кольца В.
Йод действует на витамин B12 только в щелочных растворах, и при этом образуются как лактам, так и лактон, относительные количества которых зависят от концентрации щелочи и йода.
Дальнейшая обработка хлорамином Т или бромом вела к образованию пурпурных веществ, которые становились голубыми при избытке цианида и содержали в молекуле соответственно хлор или бром. Эти продукты не были полностью охарактеризованы, но сходное вещество, возникавшее при действии хлорамина Т на лактам (дегидровитамин B12), было изучено в Кембридже, и оказалось, что оно содержит только один атом хлора. Полагают, что хлор замещал водород при мезоуглеродном атоме между кольцами В и С. Эта работа в сочетании с другими данными помогла установить, что в молекуле витамина имеется 6 сопряженных двойных связей, а не 5, как предполагалось вначале.
Метилирование
При действии избытка СН3-HgJ на JCbl в спиртовом растворе при температуре 65оС в течение трех часов можно получить метилкобаламин с выходом около 50%. Вообще реакциями корриноидов с сильными нуклеофилами получают соответствующие органокорриноиды.
М![]()
ежду диметилсульфатом и самим витамином B12 никакой реакции не происходит, так как атом азота участвует в координационной связи с кобальтом. Эта связь должна быть сначала разорвана путем превращения витамина B12 в дицианкобаламин; даже и после этого реакция зависит от значения рН. Образующийся при этом четвертичный азот обусловливает возникновение добавочной основной группы в молекуле дицианида, которая в результате этого, обладает нейтральной реакцией (а не кислой, как молекула дицианкобаламина); эта структура устойчива в кислых растворах, так как метилирование препятствует образованию координационной связи между N3 и Со. Эта реакция была использована для изучения более сложных свойств аналога витамина B12 – фактора III, который может быть метилирован или в любом из двух положений или в обоих одновременно.
Рентгеноструктурный анализ
И
Рисунок 7. Пространственная конфигурация молекулы витамина В12.
зучение витамина B12 методом рентгеноструктурного анализа начала Дороти Ходжкин в Оксфорде в 1948 г., как только были получены первые кристаллы. Независимо подобную же работу проводил Уайт в Принстоне; позже обе группы исследователей объединили свои силы. Трудоемкие вычисления на основе результатов измерения отражении рентгеновских лучей позволили составить карты электронной плотности в трех измерениях. Постепенно, в несколько последовательных этапов, по мере того как определялось положение все большего числа атомов в структуре, расчеты уточнялись. Вся программа работы с витамином B12 и теми его аналогами, которые были получены, потребовала примерно около 10 млн. вычислений. Для этого на последних этапах пришлось использовать электронные счетные машины. Никогда еще рентгеноструктурный анализ не применялся для изучения структуры столь сложной молекулы, и полный успех этой программы изучения явился замечательным достижением, несколько смутившим химиков-органиков и, кажется, удивившим даже самих специалистов по рентгеноструктурному анализу. Как заметила Дороти Ходжкин, "возможность записать химическую структуру главным образом на основании чисто кристаллографических данных о размещении атомов в пространстве – и притом для такой устрашающе сложной молекулы - это для всякого кристаллографа нечто похожее на мечту". Огромное преимущество этого метода состояло в том, что в отличие от химических методов он "работает" от центра к периферии. Иными словами, относительно тяжелый атом кобальта с наибольшей точностью указывал положение ближайших к нему атомов, а именно атомов макрокольца. Когда работа приближалась к завершению, оказалось, что единственными атомами, положение которых оставалось несколько сомнительным, были те, для которых оно было выяснено Фолкерсом и его сотрудниками в результате изучения продуктов окисления витамина. Вычисления, относившиеся к самому витамину B12, были на время отложены, когда исследователи смогли получить кристаллическую гексакарбоновую кислоту. Это более простое соединение неожиданно легко поддавалось рентгеноструктурному анализу, в связи с чем и были достигнуты большие успехи. К счастью, основные структурные особенности этого вещества и самого витамина оказались идентичными, так что исследования этих веществ взаимно дополняли друг друга. Однако они в обоих случаях независимо привели к весьма редкой структуре макрокольца. Макрокольцо содержит 4 восстановленных пиррольных кольца с прямой α-α-связьюю между кольцами А и D. Дальнейшие уточнения в расчётах сделались возможными в результате изучения двух кобаламинов, содержащих относительно тяжелые атомы, а именно производных тиоцианата и селеноцианата; позже для этой же цели был использован аналог витамина B12, содержавший два атома хлора на месте метильных групп у бензиминазола. Наконец, выяснилась природа боковых цепей, и можно было почти с полной уверенностью написать всю структурную формулу. Все оставшиеся сомнения были, по-видимому, разрешены дальнейшими вычислениями, позволившими даже установить, что в макрокольце 6 двойных связей.
Устойчивость
В литературе накопилось много данных об устойчивости витамина B12 к действию как реактивов, так и лекарственных препаратов; многие из этих данных можно теперь истолковать, и
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Влияние поверхностного потенциала воды на реологические свойства дисперсных систем
- Влияние углекислого газа
Взаимосвязь между энергопотреблением, экономической деятельностью и поступлением в атмосферу. Потребление энергии и выбросы углекисл
- Влияние физических и химических факторов на основность алкиламинов
- Вода и её свойства
ГЛАВНЫЙ СОСТАВИТЕЛЬ РЕФЕРАТАПЕТРУНИНААЛЛА БОРИСОВНАМУНИЦИПАЛЬНАЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯСРЕДНЯЯ ШКОЛА №4РЕФЕРАТпо химии на тему:“Вода
- Водонефтяные эмульсии
Министерство образования РТАГНИКафедра химииРЕФЕРАТпо химиина тему: «водонефтяные эмульсии»Выполнил: ст.гр. 11-11Жирнов А.ЕПроверил: Буд
- Вред и польза химии
- Выделение жирных кислот из растительных масел
Московский Государственный Университет Пищевых Производств. Учебно-исследовательская работа. «Выделение жирных кислот из растительн
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

