Висмут и его соединения в природе
1.1 Происхождение висмута
1.3 Химические свойства
2. НАХОЖДЕНИЕ В ПРИРОДЕ
2.1.1 Висмутин
2.1.2 Прочие руды, содержащие висмут
2.1.3 Добыча и производство
3. ФИЗИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ВИСМУТА
4. ПРИМЕНЕНИЕ В ПРОМЫШЛЕННОСТИ
4.1 Применение в металлургической промышленности и машиностроении
4.3 Другие способы применения
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
ВВЕДЕНИЕ
Среди элементов периодической системы висмут – последний практически не радиоактивный элемент, И он же открывает шеренгу тяжелых элементов – естественных альфа-излучателей. Действительно, тот висмут, который мы знаем по химическим соединениям, минералам и сплавам, принято (и не без оснований) считать стабильным, а между тем, тонкими экспериментами установлено, что стабильность висмута –кажущаяся. В действительности же ядра его атомов иногда «гибнут», правда, очень нечасто: период полураспада основного природного изотопа висмута ![]() – более
– более ![]() лет. Это примерно в полмиллиарда раз больше возраста нашей планеты...
лет. Это примерно в полмиллиарда раз больше возраста нашей планеты...
Кроме висмута-209, известны еще 26 изотопов элемента № 83. Все они радиоактивны и короткоживущие: периоды полураспада не превышают нескольких суток.
Двадцать изотопов висмута с массовыми числами от 189 до 208 и самый тяжелый ![]() подучены искусственным путем, остальные - 210Bi, 211Bi, 212Bi, 213Bi и 214Bi – образуются в природе в результате радиоактивного распада ядер урана, тория, актиния и нептуния.
подучены искусственным путем, остальные - 210Bi, 211Bi, 212Bi, 213Bi и 214Bi – образуются в природе в результате радиоактивного распада ядер урана, тория, актиния и нептуния.
Таким образом, несмотря на то что на практике мы встречаем лишь практически стабильный висмут-209, не следует забывать о важной роли элемента № 83 во всех областях знания, так или иначе связанных с радиоактивностью. Не будем, однако, впадать в другую крайность. Практическую важность приобрел прежде всего стабильный (или правильнее – псевдостабильный) висмут. Поэтому именно ему быть главным «героем» дальнейшего повествования.
1. ОБЩИЕ СВЕДЕНИЯ О ВИСМУТЕ
1.1 Происхождение висмута
Висмут (лат. Bismuthum) – химический элемент V группы периодической системы Д.И. Менделеева. Среди нерадиоактивных элементов висмут имеет самый большой атомный номер – 83 и атомную массу – 208,9804.
Происхождение названия этого элемента трактуют по-разному. Одни исследователи склонны считать его производным от древнегерманского слова «Wismuth» (белый металл), другие – от немецких слов «Wiese» (луг) и «muten» (разрабатывать рудник), поскольку в Саксонии, висмут издревле добывали на лугах округа Шнееберг. Есть еще одна версия, согласно которой название элемента произошло от арабского «би исмид», что означает «обладатель свойств сурьмы». Висмут действительно на нее очень похож. Какая из этих точек зрения наиболее близка к истине, сказать трудно. Нынешний символ элемента №83, Bi, впервые введен в химическую номенклатуру в 1819 г. шведским химиком Берцелиусом.
Висмут известен со средневековья (впервые упомянут в письменных источниках в 1450 году как Wismutton или Bisemutum). Первые сведения о висмуте появились в начале XVI в. в трудах минералога и металлурга Георга Бауэра (Агриколы). Однако до XVIII века его считали разновидностью свинца, олова или сурьмы. Лишь в 1753 француз Клод Жофруа (Claude J. Geoffroy) высказал мнение, что это отдельный элемент. Эту точку зрения подтвердил в 1793 г. Потт (J. H. Pott), описавший свойства висмута. В 1739 г. немецкий химик Потт установил самостоятельность элемента висмута. Окончательно как элемент он был открыт в 1799 г. шведским химиком Т. Бергманом.
Известный металлург и минералог средневековья Георг Агрикола в своей книге "О месторождениях и рудниках в старое и новое время", написанной в 1546 году, возвел висмут в ранг одного из основных металлов, присовокупив его к известной с древности "великолепной семерке" - золоту, серебру, меди, железу, свинцу, олову и ртути. Однако окончательно "права гражданства" висмут обрел лишь в XVIII веке. Этому металлу, пожалуй, как ни одному другому химическому элементу, повезло с названиями: по подсчетам некоторых ученых, в литературе XV-XVIII веков можно встретить более 20 "псевдонимов" висмута и среди них такие выразительные, как демогоргон, глаура, нимфа.
Висмут является последним членом подгруппы мышьяка. Относится к халькофильным элементам. Ближайшие аналоги висмута — сурьма и свинец. Кларк его по А. П. Виноградову составляет 9–10%. Содержание висмута повышается от ультраосновных магматических пород (1–10%) к кислым (1– 10%). Он представлен одним изотопом с массовым числом 209. Характеризуется переменной валентностью, в природных условиях преобладает Bi3+. Высокое сродство к сере, способность существовать в свободном состоянии и склонность к образованию основных солей определяют важнейшие формы нахождения висмута в природе. На магматическом этапе висмут не концентрируется. Его накопление связано с постмагматическими процессами гранитоидных магм. Из магматических очагов он выносится в хлоркомплексах (BiCl2+, BiCl0) и гидрооксокомплек-сах (Bi(OH)3, Bi(OH)2J). При экзогенных процессах первичные сульфидные соединения висмута окисляются (образуются оксидные и карбонатные соединения). При слабом проявлении процессов окисления висмутин и самородный висмут могут образовать россыпи.
1.2 Физические свойства
Висмут – это серебристо-серый металл с розоватым оттенком, хрупкий, легкоплавкий, плотность при 20 оС – 9,80 г/см3. Висмут — белый металл с розоватым оттенком. При комнатной температуре Висмут легко раскалывается по плоскостям спайности, в фарфоровой ступке растирается в порошок.Он обладает диамагнитностью, плохой теплопроводностью, низкой температурой плавления (271,4 оС), высокой температурой кипения (1560 °С) и способностью расширяться в объеме при затвердевании. Удельная магнитная восприимчивость равна -1,35·10-6. Висмут – самый диамагнитный металл: если его поместить между полюсами обычного магнита, то он, стремясь с одинаковой силой оттолкнуться от обоих полюсов, займет положение на равном от них расстоянии. Под влиянием магнитного поля электрическое сопротивление висмута увеличивается в большей степени, чем у других металлов; этим его свойством пользуются для измерения индукции сильных магнитных полей (прибор, служащий для этой цели, называется висмутовой спиралью). После расплавления висмута его электросопротивление падает вдвое, а при охлаждении резко возрастает (например, при понижении температуры от нуля до -180° С сопротивление этого металла увеличивается в 60 раз).
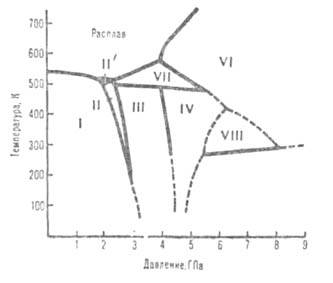
Рис. 1. Диаграмма состояния висмута при высоких давлениях. Пунктирные линии-приблизительные границы областей существования фаз.
Сечение захвата тепловых нейтронов у Висмута мало (34·10-31 м2 или 0,034 барна). Висмут и его соединения обладают дезинфицирующими и антисептическими свойствами. Он устойчив к действию кислорода и воды и растворим в концентрированной серной кислоте.
Висмут имеет ромбоэдрическую решетку с периодом а = 4,7457 Å и углом ά = 57°14'13". Удельная теплоемкость (20 °С) 123,5 Дж/(кг·К) (0,0294 кал/(г·°С)); термический коэффициент линейного расширения при комнатной температуре 13,3·10-6; удельная теплопроводность (20 °С) 8,37 вт/(м·К) (0,020 кал/(см·сек·°С)); удельное электрическое сопротивление (20° С) 106,8·10-8 ом·м (106,8·10-6ом·см). При температуре 120-150°С ковок; горячим прессованием (при 240-250°С) из него можно изготовить проволоку диаметром до 0,1 мм, а также пластинки толщиной 0,2-0,3 мм. Твердость по Бринеллю 93 Мн/м2 (9,3 кгс/мм2), по Моосу 2,5. При плавлении Висмут уменьшается в объеме на 3,27%.
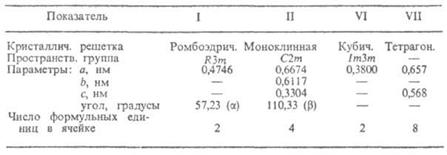
Таблица 1. Характеристика некоторых кристаллических модификаций висмута.
1.3 Химические свойства
Висмут в сухом воздухе устойчив, во влажном наблюдается его поверхностное окисление. При нагревании выше 1000° С сгорает голубоватым пламенем с образованием оксида Bi2O3. В ряду напряжений Висмут стоит между водородом и медью, поэтому в разбавленной серной и соляной кислотах не растворяется; растворение в концентрированных серной и азотной кислотах идет с выделением SO2 и соответствующих оксидов азота.
Висмут проявляет валентность 2, 3 и 5. Соединения Висмута низших валентностей имеют основной характер, высших - кислотный. Из кислородных соединений Висмута наибольшее значение имеет оксид Bi2O3, при нагревании меняющий свой желтый цвет на красно-коричневый. Bi2O3 применяют для получения висмутовых солей. В разбавленных растворах висмутовые соли гидролизуются. Хлорид BiCl3 гидролизуется с выпадением хлороксида BiOCl, нитрат Bi(NO3)3 - с выпадением основной соли BiONО3·BiOOH. Способность солей Висмут гидролизоваться используется для его очистки.
Соединения 5-валентного Висмута получаются с трудом; они являются сильными окислителями. Соль КВiO3 (соответствующая ангидриду Bi2O5) образуется в виде буро-красного осадка на платиновом аноде при электролизе кипящего раствора смеси КОН, КСl и взвеси Bi2O3. Висмут легко соединяется с галогенами и серой. При действии кислот на сплав висмута с магнием образуется висмутин (висмутистый водород) BiH3; в отличие от арсина AsH3, висмутин - соединение неустойчивое и в чистом виде (без избытка водорода) не получено. С некоторыми металлами (свинцом, кадмием, оловом) Висмут образует легкоплавкие эвтектики; с натрием, калием, магнием и кальцием - интерметаллические соединения с температурой плавления, значительно превышающей температуры плавления исходных компонентов. С расплавами алюминия, хрома и железа висмут не взаимодействует.
Металлические свойства у него выражены посильней, но к этому его просто обязывает положение в таблице элементов: он ближе к "полюсу металличности" (левый нижний угол таблицы), чем другие элементы его подгруппы. В сухом воздухе висмут устойчив, но во влажном он облачается в тончайшее покрывало оксида. Если же металл нагреть выше 1000 °С, он сгорает красивым голубоватым пламенем.
Как известно, при электролизе ионы металла переносятся с анода на катод. Так считали почти полтора столетия - с тех пор как английский ученый Майкл Фарадей установил важнейшие законы электролиза. Но вот в 1975 году сотрудники Института общей и неорганической химии Академии наук УССР обнаружили, что некоторые металлы при электролитических процессах устремляются к аноду. В опытах украинских ученых катод был изготовлен из висмута, анод - из никеля, а роль электролита выполнял расплавленный едкий натр. Когда был включен ток, висмутовый катод начал таять на глазах, и уже вскоре на поверхности анода появились блестящие шарики из чистого висмута.
Это открытие не опровергает, а лишь уточняет закон Фарадея. Большинство металлов действительно выделяется на катоде, и лишь некоторые - висмут, свинец, олово, сурьма - "предпочитают" анод, правда, при условии, что электролитом служит расплав солей щелочных и щелочноземельных металлов.
"Поправка к закону" может быть использована для очистки многих металлов и сплавов от примесей висмута, свинца и других "нарушителей порядка". Для этого металлическую заготовку, которую нужно подвергнуть рафинированию, вводят в электролит в качестве катода. Начинается электролиз, и ненужные примеси, расставшись с основной массой металла, перебазируются на анод. Этот экономичный способ назван катодной очисткой.
Как известно, все металлы, да и вообще большинство твердых тел, имеют кристаллическую структуру, при которой их атомы (ионы, молекулы) располагаются в пространстве в строго определенном порядке.
В ходе многочисленных опытов удалось установить, что если на переохлажденную металлическую пластинку, находящуюся в камере, где обеспечены указанные условия, нанести пары какого-либо металла, то на пластинке тут же образуется "стеклянная" пленка. Подобный эксперимент, в частности, был проделан с висмутом. Оказалось, что пленка из висмутового "стекла" толщиной всего в несколько микрон обладает буквально сказочными магнитными и сверхпроводящими свойствами. Даже при обычной температуре ее сопротивление электрическому току во много раз ниже, чем у того же висмута в кристаллическом состоянии.
Висмут помог советским физикам синтезировать ядра 107-го элемента периодической системы. Помещенная в ускоритель висмутовая мишень подверглась ожесточенной бомбардировке ионами хрома. Более двух месяцев непрерывно работал ускоритель, сопоставлялись и анализировались результаты десятков тончайших экспериментов, и вот, наконец, можно было с уверенностью заявить, что при слиянии иона хрома с ядром висмута образуются ядра 107-го элемента, период полураспада которых всего около двухтысячных долей секунды.
1.4 Получение висмута
Основное количество Висмута добывается попутно при огневом рафинировании чернового свинца (веркблея). Пирометаллургический способ основан на способности Висмута образовывать тугоплавкие интерметаллические соединения с К, Na, Mg и Са. В расплавленный свинец добавляют указанные металлы и образовавшиеся твердые соединения их с Висмутом (дроссы) отделяют от расплава. Значительное количество Висмута извлекают из шламов электролитического рафинирования свинца в кремнефтористоводородном растворе, а также из пылей и шламов медного производства. Содержащие Висмут дроссы и шламы сплавляют под щелочными шлаками. Полученный черновой металл содержит примеси As, Sb, Cu, Pb, Zn, Se, Те, Ag и некоторых других элементов. Выплавка Висмута из собственных руд производится в небольшом масштабе. Сульфидные руды перерабатывают осадительной плавкой с железным скрапом. Из окисленных руд Висмут восстанавливают углем под слоем легкоплавкого флюса.
Для грубой очистки чернового Висмут применяются в зависимости от состава примесей различные методы: зейгерование, окислительное рафинирование под щелочными флюсами, сплавление с серой и другими. Наиболее трудноотделяемая примесь свинца удаляется (до 0,01%) продуванием через расплавленный металл хлора. Товарный Висмут содержит 99,9-99,98% основного металла. Висмут высокой чистоты получают зонной перекристаллизацией в кварцевых лодочках в атмосфере инертного газа.
Висмут получают сплавлением сульфида с железом:
Bi2S3 + 3Fe = 2Bi + 3FeS,
или последовательным проведением процессов:
2Bi2S3 + 9O2 = 2Bi2O3 + 6SO2↑;
Bi2O3 + 3C = 2Bi + 3CO↑.
2. НАХОЖДЕНИЕ В ПРИРОДЕ
2.1 Содержание в земной коре
Висмутовые руды — природные минеральные образования, содержащие Висмут в количествах, при которых экономически целесообразно его извлечение современными методами производства.
Висмут – малораспространенный элемент. Его кларк (содержание в земной коре по массе) составляет 2х10-5% и по этому показателю он близок к серебру. Обратите внимание на двойственность поведения висмута в природе. С одной стороны, он может концентрироваться в минералах, а с другой – рассеиваться в рудах (особенно сульфидных) так, что содержание его в них можно определить лишь одним словом – «следы». Ярко выраженная способность висмута к образованию собственных минералов не позволяет отнести его к рассеянным элементам в общепринятом значении этого слова. В «чужие» кристаллические решетки он, как правило, не входит. Исключение – свинцовый минерал галенит PbS, в решетке которого при определенных условиях висмут может удерживаться без образования собственных минералов.
Тем не менее, скопления богатых висмутовых руд встречаются очень редко. Они крайне ограниченны в пространстве и отличаются неравномерностью распределения, что, конечно, доставляет огорчения геологам и горнякам, занимающимся разведкой и эксплуатацией висмутовых месторождений.
Минералы висмута как бы прячутся в рудах других элементов: вольфрама, олова, меди, никеля, молибдена, урана, кобальта, мышьяка, золота и других элементов – разных и непохожих.
Висмут встречается в природе в виде многочисленных минералов в основном гидротермального происхождения, главные из которых: висмутин или висмутовый блеск (Bi2S3), висмут самородный (Bi), бисмит или висмутовая охра (Bi2O3), тетрадимит (Bi2Te3) и пр. Эти минералы рассеяны и встречаются как примеси в свинцово-цинковых, медных, молибденово-кобальтовых и олово-вольфрамовых рудах (поэтому и добывается висмут как побочный продукт переработки полиметаллических руд). Естественными источниками поступления висмута в природные воды являются процессы выщелачивания висмутсодержащих минералов. Источником поступления в природные воды могут быть также сточные воды фармацевтических и парфюмерных производств, некоторых предприятий стекольной промышленности.
Висмут в том или ином количестве в виде изоморфной примеси входит в состав некоторых сульфидов, а также образует самостоятельные минералы. Известно около 90 минералов висмута, но промышленное значение имеют немногие из них: самородный висмут, висмутин, виттихенит, тетрадимит, галеновисмутит, козалйт, айкинит, бисмит, бисмутит.
Самородный висмут (содержание Bi 99,9 %) кристаллизуется в тригональной сингонии, кристаллы ромбоэдрические, псевдокубические, агрегаты зернистые, листоватые, перистые, дендриты. Цвет желтовато-белый, блеск металлический, твердость 2—2,5, плотость 9,8 г/см3.
Обнаруживает совершенную спайность. В свежем изломе серебристо-белый с желтоватым оттенком, обычно с красноватой побежалостью. Твёрдость по минералогической шкале 2,5, плотность 9780—9830 кг/м3. В. с. образуется в месторождениях скарнового типа и в гидротермальных месторождениях, в ассоциации с касситеритом, вольфрамитом, молибденитом, шеелитом и сульфидами Pb, Zn, Cu, Fe, а также в рудах, содержащих сульфиды и арсениды Со и Ni, урановую смолку, самородное серебро и др.
Природный висмут состоит из одного изотопа 209Bi, который считался самым тяжёлым из существующих в природе стабильных изотопов. Однако в 2003 было экспериментально доказано, что он является альфа-радиоактивным с периодом полураспада 1,9±0,2×1019 лет.
Кроме 209Bi, известны ещё более трех десятков (пока 34) изотопов и ещё больше изомеров. Среди них есть три долгоживущих:
207Bi 31,55 год
208Bi 0,368×106 лет
210mBi 3,04×106 лет
Все остальные радиоактивны и короткоживущи: периоды их полураспада не превышают нескольких суток.
Тринадцать изотопов висмута с массовыми числами от 197 до 208 и самый тяжелый 215Bi получены искусственным путём, остальные — 210Bi, 211Bi, 212Bi, 213Bi и 214Bi — образуются в природе в результате радиоактивного распада ядер урана, тория, актиния и нептуния.
2.1.1 Висмутин
Висмутин (англ. Bismuthinite) Bi2S3 (Bi 81,3 %) – минерал, сульфид висмута подкласса простых сульфидов кристаллизуется в ромбической сингонии, кристаллы призматические и игольчатые, цвет свинцово-серый, белый с желтоватой и синей побежалостью, блеск металлический, твердость 2—2,5, плотность 6,8 г/см3. Встречается в гидротермальных месторождениях жильного типа в ассоциации с топазом, бериллом, в золото-кварцевых жилах и медно-висмутовых месторождениях. Впервые обнаружен в 1832 г. в Боливии. Син.: бисмутин, висмутинит, висмутовый блеск.
Вi - 81,3 %, S - 18,7 %. Нередки примеси в небольших количествах РЬ, Сu, Fе, Аs, SЬ, Те и др. Из них РЬ, Sb и Те могут изоморфно замещать висмут.
Сингония ромбическая, ромбо-дипирамидальный вид симметрии 3L23PC. Простр. гр. Pbnm (D162b). a0 = 11,13; b0 = 11,27; c0 = 3,97. Кристаллическая структура аналогична структуре антимонита.
Хорошо образованные кристаллы редки, облик кристаллов призматический или игольчатый. Так же как и антимонит, встречается в удлинённых шестоватых кристаллах, образованных чаще всего гранями призм {110}, {120}, {130} и пинакоидов {100}, {010}, {001}. Большей частью грани покрыты тонкой вертикальной штриховкой.
Распространён также в виде сплошных зернистых масс, иногда лучистых или волокнистых агрегатов.
Цвет висмутина оловяно-белый до серебристо-белого со свинцово-серым оттенком. Часто наблюдается жёлтая или пёстрая побежалость. Непрозрачен. Черта серая. Блеск сильный металлический. Твёрдость 2 - 2,5. Спайность совершенная по {010} и несовершенная по {100} и {001}. Режется ножом, гибкий, но не упругий. Плотность 6,4 - 6,8, в отдельных случаях до 7,1. Электричества не проводит.
Диагностические признаки. От похожего на висмутин антимоииата отличается более сильным блеском, большим удельным весом в реакцией с КОН. В агрегатах он похож также на многие сложные по составу сульфоаптимониты и сульфовисмутиты, от которых без химических реакций его бывает нелегко отличить, а зачастую и невозможно. Под п. тр. на угле легко плавится, кипит и разбрызгивается вокруг во все стороны. В восстановительном пламени дает королёк висмута, оставляя на угле лимонно-жёлтый налёт окиси висмута. Характернейшей реакцией на висмут является получение йодистого висмута в виде ярко-красного налёта при сплавлении с йодистым калием (в виде каймы вокруг пробы). В HNO3 легко растворяется с выделением всплывающей серы.
Висмутин встречается исключительно в высокотемпературных гидротермальных месторождениях, связанных с грейзенами или скарнами. В качестве минерала-спутника наблюдается в месторождениях олова, вольфрама, мышьяка, часто в ассоциации с самородным висмутом, арсенопиритом, халькопиритом, иногда самородным золотом, топазом, бериллом, пиритом, галенитом и многими другими сульфидами. Очень редко образует самостоятельные месторождения.
В зоне окисления легко разрушается, образуя основные карбонаты в виде псевдоморфоз по висмутину.
В России известен в олово-вольфрамовых высокотемпературных кварцевых жилах Белухи и Букуки с кварцем, касситеритом, арсенопиритом, сфалеритом, халькопиритом, галенитом и самородным висмутом, в оловоносных грейзенах Шерловой Горы (Восточное Забайкалье). Встречается на всех скарновых месторождениях Дальнегорска (Приморье) в виде вкрапленности, гнёзд и включений в полиметаллической и боросиликатной руде. Существенный интерес представляют месторождения Средней Азии, например скарны Устарасая (в 70 км. к северо-востоку от г. Ташкента), где висмутин с самородным висмутом встречается в ряде кварцевых жил в известняках в ассоциации с пиритом, арсенопиритом, халькопиритом и др.
Крупнейшие в мире висмутовые месторождения находятся в Боливии (Тасна, Чоролк и др.) и в Перу (Серро-де-Паско) и генетически связаны с молодыми изверженными породами.
Из других зарубежных месторождений стоит отметить: месторождения Рудных гор (Нижняя Саксония, Германия), Коннектикут (США), Мексика, Великобритания, Швеция, Италия (окрестности Турина), Чехия, Венгрия, Румыния. Характерен для оловянно-свинцово-цинковых месторождений Японии.
2.1.2 Прочие руды, содержащие висмут
Виттихенит минерал состава SCu 2S.Bi2S3 (Bi 42,15 %) кристаллизуется в ромбической сингонии, кристаллы тетраэдрические, агрегаты зернистые, цвет темно-серый до светло-серого, черта черная, блеск металлический, твердость 2—3, плотность 6,3 г/см3. Встречается в гидротермальных жилах богатых медью и висмутом.
Тетрадимит Вi2Те2S (Bi 59,27 %) кристаллизуется в тригональной сингонии, кристаллы ромбоэдрические, агрегаты листоватые и зернистые. Цвет стально-серый, блеск металлический, твердость 1,5—2, плотность 7,3 г/см3. Распространен в гидротермальных и контактово-метасомати-ческих месторождениях. Кристаллическая структура типичная слоистая. Пятнадцатислойная плотнейшая ромбоэдрическая упаковка содержит в вертикальном периоде повторяемости три идентичных пакета, состоящих из пяти слоёв, каждый из которых сложен атомами своего рода. Состав и порядок заполнения слоёв в каждом пакете следующий: ТеВiSВiТе.
Таблитчатые или ромбоэдрические кристаллы чаще всего являются четверниками с плоскостью срастания по {0118) и {0115). Встречается преимущественно в виде листоватых или пластинчатых агрегатов.
По многим внешним признакам похож на молибденит; отличается от него более сильным блеском, большим удельным весом.
В России он встречен во Фроловском руднике из группы Турьинских рудников (Северный Урал), Шилово-Исетском золоторудном месторождении (в 66 км. к востоку от Екатеринбурга), в ряде пунктов Западной и Восточной Сибири. Отмечен с золотом, гесситом и висмутином в кварцевых жилах Дарасунского месторождения (Восточное Забайкалье). Совместно с пиритом, висмутом и цумоитом (ВiТе) наблюдается в кальцитовых жилах, вмещаемых гранат-диопсидовыми скарнами Тырныауза (Кабардино-Балкария, Северный Кавказ).
В Северо-Западном Казахстане отмечен в кварцевых золотосодержащих жилах месторождения Кумак. Наблюдался также в ряде золоторудных месторождений США, Мексики, Британской Колумбии и др.
Галеновисмутит PbBi2S4 (Bi 55,48 %) кристаллизуется в ромбической сингонии, кристаллы игольчатые, столбчатые пластинчатые, агрегаты зернистые. Цвет минерала оловянно-белый до светло-серого, черта светло-серая, блестящая, твердость 2,5—3,5, плотность 7,1 г/см3. Встречается в высокотемпературных месторождениях висмута, скарнах и золото-кварцевых жилах.
Козалит Pb2Bi2S5 (Bi 42,10%) (по руднику Козала в Мексике) кристаллизуется в ромбической сингонии, кристаллы призматические, игольчатые, агрегаты шестоватые, лучистые, зернистые, цвет свинцово-серый, черта черная, твердость 2,5—3, плотность 6,7—7,0 г/см3.
Айкинит CuPbBiS3 (Bi 36,29 %) (по фамилии Айкин) кристаллизуется в ромбической сингонии, кристаллы длинностолбчатые до игольчатых, агрегаты зернистые и друзы. Цвет минерала серый с цветной побежалостью, черта серовато-черная, блестящая, твердость 2—2,5, плотность 7,1 г/см3.
Бисмит Bi2О3 (Bi 89,6 %) кристаллизуется в моноклинальной сингонии, кристаллы псевдоромбические, агрегаты тонкозернистые и порошковатые, цвет серовато-зеленый, желтый, блеск полуалмазный, матовый, твердость 4,5, плотность 9,2 г/см3. Развит в зоне окисления.
2.1.3 Добыча и производство
Традиционные потребители висмута – металлургическая, фармацевтическая и химическая промышленность. В последние десятилетия к ним прибавились ядерная техника и электроника. Широкому применению висмута в металлургии и электронике способствовало и то обстоятельство, что висмут – наименее токсичный из всех тяжелых металлов.
Из соединений висмута шире всего используют его трехокись Bi2O3. В частности, ее применяют в фармацевтической промышленности для изготовления многих лекарств от желудочно-кишечных заболеваний, а также антисептических и заживляющих средств. В производстве полимеров трехокись висмута служит катализатором; ее применяют, в частности, при получении акриловых полимеров. Bi2O3 употребляют также в производстве эмалей, фарфора и стекла – главным образом в качестве флюса, понижающего температуру плавления смеси неорганических веществ, из которой образуются эмаль, фарфор или стекло. Соли висмута находят применение в областях, весьма далеких друг от друга. Это, к примеру, производство перламутровой губной помады и производство красок для дорожных знаков. Далеко в прошлое ушло то время, когда висмут считался малоценным металлом с ограниченной сферой применения. Сейчас он нужен всем странам с высокоразвитой промышленностью. Поэтому и спрос на него продолжает расти.
Собственно висмутовые месторождения имеют ограниченное распространение и обычно этот металл образует комплексные руды с другими металлами в ряде рудных формаций гидротермальных месторождений. Среди них выделяются следующие:
1. Вольфрам-медно-висмутовые
2. Месторождения пятиэлементной формации (Co-Ni-Bi-Ag-U)
3. Золото-висмутовые
4. Мышьяк-висмутовые
5. Медно-висмутовые
6. Кварц-висмутовые
Трудно назвать рудное месторождение, в котором не было бы висмута, но еще сложнее назвать такое месторождение, в котором концентрация его была бы столь высокой, что оно могло бы с выгодой разрабатываться только ради висмута. Как же быть? Поступают просто: висмут берут отовсюду, где извлечение его экономически (или технологически) оправдано. Вот перечень сырьевых источников висмута, обеспечивающих около 3/4 мирового (без СССР) спроса: медные, свинцовые и серебряные рудники Перу, свинцовые месторождения Мексики, медные и свинцово-цинковые руды Японии, медные, свинцовые и серебряно-кобальтовые месторождения Канады, вольфрамово-оловянные и оловянно-серебряные руды Боливии.
За исключением боливийских, все перечисленные руды висмутом бедны. Основной производитель висмута – свинцовая промышленность – извлекает его из концентратов, в которых не больше сотых, реже десятых процента висмута, а в исходных рудах полиметаллических месторождений от 0,0001 до 0,01% Bi. Та же примерно картина наблюдается и в медной промышленности. Обычно висмут здесь извлекают из анодных шламов, образующихся при электролитическом рафинировании меди. Источником висмута может быть и вторичное сырье. Например, в ФРГ значительное количество висмута извлекают при переработке пиритных огарков и из металлического лома. Сколько же висмута получают ежегодно во всем мире? Известно, что в 1968 г. мировое производство висмута (без СССР) составило 3800 т. Предполагают, что мировая потребность в висмуте в 2000 г. составит 5...6 тыс. т.
Эндогенные месторождения висмута формировались на средней и поздней стадиях геосинклинального этапа, а также в процессе тектономагматической активизации консолидированных участков складчатых областей и платформ. Собственно висмутовые месторождения не имеют широкого распространения и обычно этот металл образует комплексные руды с другими металлами в ряде рудных формаций. Месторождения висмута и висмутсодержащих руд формировались в различные эпохи рудообразования. В докем-брийскую эпоху образовались месторождения висмутсодержащих руд в Канаде (Большое Медвежье озеро, Эльдорадо и др.), в позднепалеозойскую (герцинскую) — месторождения в Рудных горах (Яхимов в Чехии), Средней Азии (Адрасман в Таджикистане, Брич-Мулла и Устарасай в Узбекистане), в мезозойскую эпоху — месторождения в Южной Корее (Санг-Донг и др.). Значительное количество месторождений висмутсодержащих руд принадлежит альпийской металлогенической эпохе (Таена в Боливии, Сан-Грегори в Перу).
Минерально-сырьевая база висмутодобывающей промышленности представлена как собственно висмутовыми, так и комплексными висмутсодержащими месторождениями. Общие запасы висмута в мире (без учета стран СНГ) составляют около 130 тыс. т. Ведущими странами-держателями запасов висмута являются: Япония (более 40 тыс. т), США (30 тыс. т) и Австралия (20 тыс. т). Значительные запасы этого металла сосредоточены в Боливии, Мексике, Перу, Канаде, Китае, России и других странах. Уникальные месторождения висмута встречаются редко (месторождение Теннант-Крик в Австралии). Богатые руды содержат Bi более 1 %, рядовые — 1—0,2 %, бедные — менее 0,2 % (в комплексных рудах).
В мировой практике висмут в основном добывается в качестве попутного компонента из комплексных руд: Со-Ni—Bi—Ag—U, As—Bi, Cu—Bi, а также из висмутсодержащих свинцовых и медных руд. Общая добыча и производство висмута составляла: в 1937 г. — 600—700 т, в 1960 г. -2600 т, в 1975 г. - 5380 т и в 2000 г. - более 10000 т. Главными производителями висмута в настоящее время являются Боливия, Перу, Мексика, Австралия и США.
Известны следующие типы месторождений висмутовых и висмутсодержащих руд:
1) грейзеновые,
2) скарновые,
3) плутоногенные гидротермальные,
4) вулканогенные гидротермальные.
Грейзеновые месторождения представлены комплексными W— Sn—Bi рудами. Формирование их связано с аляски-товыми гранитами. Рудные тела имеют форму штокверков, труб и жил, приуроченных к трещинам скола. Наиболее характерным и хорошо изученным представителем этого типа является месторождение Альтенберг в Германии. В рудах месторождения помимо олова и вольфрама содержится висмут в виде висмутина и самородного висмута.
Скарновые месторождения пространственно связаны с гранат-пироксеновыми и другими известковистыми скарнами. Они формируются на контакте гранитоидов с карбонатными породами или на некотором удалении от этого контакта и реже в гранитоидах. Это, как правило, комплексные W—Mo—Bi месторождения. Главными рудными минералами являются шеелит, молибденит, висмутин, второстепенными — касситерит, магнетит, пирротин, пирит, арсенопирит, вольфрамит, халькопирит, сфалерит и галенит. Месторождения этого типа выявлены в России (Восток-П в Приморье, Тырныаузское на Северном Кавказе), Южной Корее (Санг-Донг), Канаде (Эмеральд-Фини) и других странах.
Плутоногенные гидротермальные месторождения известны в Узбекистане (Брич-Мулла, Устарасай), Германии (Нейбулак, Шнееберг), Перу (Сан-Грегори), США (Монте-Кристо), Канаде (Эльдорадо). Оруденение связано с гранитоидными интрузиями. Рудные тела представлены в основном жилами и линзами. Среди месторождений этого типа выделяются две формации — арсенопирит-висмутовая и пятиэлементная (Со—Ni—Ag—Bi—U). В качестве примера месторождений арсенопирит-висмутовой формации охарактеризуем месторождение Устарасай. Оно расположено в Узбекистане в пределах Брич-Муллинского рудного поля (Чаткальский хребет). Участок месторождения сложен кварцитами, песчаниками, известняками и доломитами верхнего девона.
Интрузивные породы представлены штоком монцонитов, дайками сиенит-аплитов, а также гранодиоритами и дайками диабазов и диабазовых порфиритов. Верхнедевонские отложения слагают юго-восточное крыло Коксуйской антиклинали, осложненной продольными разломами, надвигами и крутыми сбросами. Оруденение развито в известняках в виде секущих кварц-висмутовых жил, пластообразных рудных залежей и столбообразных мышьяк-висмутовых метасоматических тел.
Формирование месторождения протекало в течение трех стадий: мышьяковую, свинцово-висмутовую и свинцово-сурьмяную.
Первая стадия проявлена слабо и представлена метасоматическими пластообразными телами, сложенными арсенопиритом (70-80 %) и кварцем (20-30 %).
Вторая стадия характеризовалась образованием разнообразных рудных минералов — пирита, пирротина, висмутина, самородного висмута, висмутовых сульфосолей и жильных минералов (кварц, доломит, кальцит).
Третья стадия минерализации развита незначительно в виде маломощных (до 2—7 см) крутопадающих жил. На этой стадии выделялись кварц и ассоциирующие с ним сфалерит, галенит, буланжерит, бурнонит, арсенопирит.
Вулканогенные гидротермальные месторождения висмута встречаются относительно редко. Они известны в Таджикистане (Адрасман), Швейцарии (Аннивере), Германии (Шварцвальд), Италии (Бочегиано), Боливии (Таена). Генетически тесно связаны с вулканогенными комплексами дацит-риолитовой формации, а пространственно — с субвулканическими дайками, жерловинами и некками и локализуются в вулканических структурах, синвулканических разломах и трещинах. Рудные тела представлены ветвящимися жилами, линзами, штокверками, реже трубами. Глубина формирования месторождений 0,5—1,0 км. Среди них выделяются халькопирит-висмутовая и касситерит-вольфрамит-висмутовая рудные формации. Типичным представителем халькопирит-висмутовой рудной формации является месторождение Адрасман. Оно расположено в Восточном Карамазаре (Таджикистан). Участо
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Влияние состава растворителя на микроволновый синтез нанопорошка CuInSe2
Нанотехнология в последние годы стала одной из наиболее важных и захватывающих областей знаний на переднем крае физики, химии, биологи
- Каталітичні процеси
ЗмістВступ1.Каталітичні процеси1.1 Активність каталізаторів1.2 Селективність (вибірковість каталізаторів)2.Гомогенний і гетерогенний к
- Радон, его влияние на человека
Федеральное агентство по образованиюУральский государственный лесотехнический университет РЕФЕРАТ РАДОН Исполнитель: ИЭФ, гр.1
- Расчет насадочной ректификационной колонны непрерывного действия по разделению смеси хлороформ-бензол
Разделение жидких и газообразных смесей на индивидуальные компоненты имеет большое значение в химической, нефтехимической и родствен
- Фармацевтический анализ производных фенотиазина
- Химическая термодинамика. Скорость химических процессов
- Компоненты, обладающие свойствами понижать горючесть полимерных материалов
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

