Ароматические углеводороды (арены)
С.Ю. Елисеев
Понятие ароматических углеводородов, их применение, физико-химические и пожаровзрывоопасные свойства.
Современное представление о строении молекулы бензола. Гомологический ряд бензола, номенклатура, изомерия. Токсичность аренов.
Основные химические реакции:
замещения (галогенирование, нитрование, сульфирование, алкилирование)
присоединения (водорода и галогенов);
окисления (неполное окисление, особенности процесса горения, склонность к самовозгоранию при контакте с сильными окислителями);
Правила замещения в бензольном кольце. Заместители первого и второго ряда.
Промышленные методы получения ароматических углеводородов.
Краткая характеристика основных ароматических углеводородов: толуола, бензола, ксилола, этилбензола, изопропилбензола, стирола и т.д.
Нитросоединения ароматического ряда, физико-химические и пожароопасные свойства нитробензола, толуола. Реакции их получения.
Ароматические амины: номенклатура, изомерия, способы получения, отдельные представители (анилин, дифениламин, диметиланилин).
Ароматические углеводороды (арены)
Ароматическими соединениями обычно называют карбоциклические соединения, в молекулах которых имеется особая циклическая группировка из шести углеродных атомов – бензольное ядро. Простейшим веществом, содержащим такую группировку, является углеводород бензол; все остальные ароматические соединения этого типа рассматривают как производные бензола.
Благодаря наличию в ароматических соединениях бензольного ядра они по некоторым свойствам значительно отличаются от предельных и непредельных алициклических соединений, а также и от соединений с открытой цепью. Отличительные свойства ароматических веществ, обусловленные наличием в них бензольного ядра, обычно называют ароматическими свойствами, а бензольное ядро – соответственно ароматическим ядром.
Следует отметить, что само название “ароматические соединения” теперь уже не имеет своего первоначального прямого значения. Так были названы первые изученные производные бензола, потому что они обладали ароматом или же были выделены из природных ароматических веществ. В настоящее же время к ароматическим соединениям относят многие вещества, обладающие и неприятными запахами или совсем не пахнущие, если в его молекуле содержится плоское кольцо с (4n + 2) обобщенными электронами, где n может принимать значения 0, 1, 2, 3 и т.д., - правило Хюккеля.
Ароматические углеводороды ряда бензола.
Первый представитель ароматических углеводородов – бензол – имеет состав C6H6 . Это вещество было открыто М.Фарадеем в 1825 г. в жидкости, образующейся при сжатии или охлаждении т.н. светильного газа, который получается при сухой перегонке каменного угля. Впоследствии бензол обнаружили (А.Гофман, 1845г.) в другом продукте сухой перегонки каменного угля – в каменноугольной смоле. Он оказался весьма ценным веществом и нашел широкое применение. Затем было установлено, что очень многие органические соединения являются производными бензола.
Строение бензола.
Долгое время оставался неясным вопрос о химической природе и о строении бензола. Казалось бы, что он представляет собой сильно непредельное соединение. Ведь его состав C6H6 по соотношению атомов углерода и водорода отвечает формуле CnH2n-6, тогда как соответствующий по числу углеродных атомов предельный углеводород гексан имеет состав C6H14 и отвечает формуле CnH2n+2. Однако бензол не дает характерных для непредельных соединений реакций; он, например, не обеспечивает бромной воды и раствора KMnO4, т.е. в обычных условиях не склонен к реакциям присоединения, не окисляется. Напротив, бензол в присутствии катализаторов вступает в характерные для предельных углеводородов реакции замещения, например, с галогенами:
C6H6 + Cl2 ® C6H5Cl + HCl
Выяснилось все же, что в определенных условиях бензол может вступать и в реакции присоединения. Там, в присутствии катализаторов он гидрируется, присоединяя 6 атомов водорода:
C6H6 + 3H2 ® C6H12
Под действием света бензол медленно присоединяет 6 атомов галогена:
C6H6 + 3Cl2 ® C6H6Cl6
Возможны и некоторые другие реакции присоединения, но все они протекают с трудом, во много раз менее активно, чем присоединение к двойным связям в веществах с открытой целью или в алициклических соединениях.
Далее, было установлено, что однозамещенные производные бензола C6H5X не имеют изомеров. Это показало, что все водородные и все углеродные атомы в его молекуле по своему положению равноценны, что также долго не находило объяснения.
![]()
![]()
![]() Впервые формулу строения бензола предложил в 1865г. немецкий химик Август Кекуле. Он высказал предложение, что 6 углеродных атомов в бензоле образуют цикл, соединяясь друг с другом чередующимися простыми и двойными связями, и, кроме того, каждый из них соединен с одним атомом водорода: СН
Впервые формулу строения бензола предложил в 1865г. немецкий химик Август Кекуле. Он высказал предложение, что 6 углеродных атомов в бензоле образуют цикл, соединяясь друг с другом чередующимися простыми и двойными связями, и, кроме того, каждый из них соединен с одним атомом водорода: СН
![]()
![]()
![]()
![]() СН СН
СН СН
![]()
![]()
![]() СН СН
СН СН
СН
![]()
![]()
![]()
![]()
![]()
![]() Кекуле предположил, что двойные связи в бензоле не неподвижны; по его представлениям, они непрерывно перемещаются (осцилируют) в кольце, что можно представить схемой: СН (I) СН (II)
Кекуле предположил, что двойные связи в бензоле не неподвижны; по его представлениям, они непрерывно перемещаются (осцилируют) в кольце, что можно представить схемой: СН (I) СН (II)
![]() Формулы I и II, согласно Кекуле, СН СН СН СН
Формулы I и II, согласно Кекуле, СН СН СН СН
![]() совершено равнозначны и лишь ½ ½ <=> ½ ½
совершено равнозначны и лишь ½ ½ <=> ½ ½
![]()
![]()
![]()
![]()
![]() выражают 2 взаимно переходящие СН СН СН СН
выражают 2 взаимно переходящие СН СН СН СН
![]() фазы соединения молекулы бензола. СН СН
фазы соединения молекулы бензола. СН СН
К этому выводу Кекуле пришел на том основании, что если бы положение двойных связей в бензольном было зафиксировано, то его двухзамещенные производные C6H4X2 с заместителями при соседних углеродах должны были бы существовать в виде изомеров по положению простых и двойных связей:
Х Х
½ (III) ½ (IV)
![]()
![]()
![]()
![]()
![]()
![]() С С
С С
НС С—Х НС С—Х
½½ ½ <=> ½ ½½
![]()
![]()
![]()
![]()
![]()
![]() НС СН НС СН
НС СН НС СН
СH СH
В одном (III) атомы углерода, при которых расположены заместители X, были бы соединены двойной связью, в другом (IV) – простой. Однако все попытки получить такие изомеры не увенчались успехом. С точки зрения же представлений об осцилляции связей эти изомеры не могут существовать, т.е. формулы III и IV выражают строение одного и того же вещества, для которого возможны две взаимно переходящие фазы состояния молекулы.
Формула Кекуле получила широкое распространение. Она согласуется с представлениями о четырехвалентности углерода, объясняет равноценность водородных атомов в бензоле. Наличие в последнем шестичленного цикла доказано; в частности, оно подтверждено тем, что при гидрировании бензол образует циклогексан, в свою очередь циклогексан путем дегидрирования превращается в бензол.
Однако формула Кекуле имеет существенные недостатки. Допуская, что в бензоле имеются три двойных связи, она не может объяснить, почему бензол в таком случае с трудом вступает в реакции присоединения, устойчив к действию окислителей, т.е. не проявляет свойств непредельных соединений.
Исследование бензола с применением новейших методов указывает на то, что в его молекуле между углеродными атомами нет ни обычных простых, ни обычных двойных связей. Например, изучение ароматических соединений при помощи лучей Рентгена показало, что 6 атомов углерода в бензоле, образующие цикл, лежат в одной плоскости в вершинах правильного шестиугольника и центры их находятся на равных расстояниях друг от друга, составляющих 1,40 А. Эти расстояния меньше, чем расстояния между центрами углеродных атомов, соединенных простой связью (1,54 А), и больше, чем м. соединенными двойной связью (1,34 А). Таким образом, в бензоле углеродные атомы соединены при помощи особых, равноценных между собой связей, которые были названы ароматическими связями. По природе своей они отличаются от двойных и простых связей; наличие их и обуславливает характерные свойства бензола. С точки зрения современных электронных представлений природу ароматических связей объясняют следующим образом.
Как уже было указано ранее, простая связь между атомами углерода осуществляется одной парой, а двойная – двумя парами обобщенных электронов. Одна из электронных пар двойной связи находится в таком же состоянии, как пара электронов, осуществляющая простую связь (s-связь). Вторая же электронная пара осуществляет связь особого характера (π-связь). В соответствии с формулой Кекуле в бензоле должны быть три π-связи. На самом же деле в бензоле нет обычных пар π-электронов фиксированных между двумя определенными С-атомами, как это изображает схема I. В шестичленном цикле бензола все простые связи С-С и С-Н (s-связи) лежат в одной плоскости. Облака π-электронов всех С-атомов, имеющие форму объемных восьмерок, направлены перпендикулярно плоскости бензольного кольца. Каждое из таких облаков перекрывается облаками двух соседних углеродных атомов. Это показано на следующем рисунке:
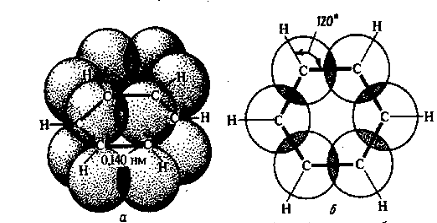 |
Рис. 9. Взаимное перекрывание 2р-орбиталей в молекуле бензола:
а – вид сбоку, б – вид сверху.
Плотность облаков π-электронов в бензоле равномерно распределена между всеми С-С-связями. Следовательно, π-электроны обобщены всеми углеродными атомами кольца, образуя единое кольцевое облако шести электронов (ароматический электронный секстет). Таким образом объясняется равноценность (выравненность) ароматических связей, придающих бензольному ядру характерные (ароматические) свойства. Равномерное распределение облака π-электронов и выравненность связей в бензоле иногда изображают формулой (4). И в настоящее время бензол продолжают изображать формулой Кекуле (1). Но всегда надо помнить, что она неверно отражает характер связей в бензоле.
Очень часто для простоты формулу бензола по Кекуле представляют шестиугольником с двойными связями без символов углерода и водорода (2). Иногда можно встретить изображение бензола и просто шестиугольником (3); но такой способ не рекомендуется, так принято изображать кольцо циклогексана; следовательно, в каждом его углу подразумевается группа СН2, а не СН. В последние годы, когда хотят подчеркнуть выравненность связей в бензоле, его изображают шестиугольником с кружочком внутри (4).
![]()
![]()
![]() НС (1) (2) (3) (4)
НС (1) (2) (3) (4)
![]()


![]()
 НС СН
НС СН
![]()
![]() ½½
½½
![]()
![]()
![]() НС СН
НС СН
НС
Гомологи бензола.
Гомологи бензола представляют собой его производные, образованные в результате замещения атомов водорода бензольного ядра предельными углеводородными заместителями; состав их, так же как и бензола, выражает формулой Сn Н2n-6.
Гомологи бензола, так же как и другие соединения, в которых наряду с бензольным ядром имеются ацикличические группировки (группировки жирного ряда), иногда называют жирноароматическими соединениями.
Число ароматических соединений, содержащих ядра бензола, очень велико, и они находят большое и разнообразное применение. Основой их являются ароматические углеводороды, среди которых различают: а) ароматические углеводороды ряда бензола, содержащие одно бензольное ядро (одноядерные), и б) многоядерные ароматические углеводороды, содержащие два и более бензольных ядер. Среди них различают: а) ароматические углеводороды с конденсированными бензольными ядрами; в них два или несколько ядер имеют общие углеродные атомы; б) ароматические углеводороды с неконденсированными бензольными ядрами, в которых каждое ядро изолировано, т.е. не имеет общих с другими ядрами углеродных атомов.
Все остальные одноядерные и многоядерные ароматические соединения являются замещенными производными соответствующих ароматических углеводородов.
![]()
![]()
![]()
![]() 8 1 8 9 1
8 1 8 9 1
![]() a a a a
a a a a
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 7 b 9 b 2 7 b b 2 дифенил
7 b 9 b 2 7 b b 2 дифенил
6 b b 3 6 b b 3 С12Н10
a 5 10 a 4 a 5 10 a 4
нафталин антрацен —СН2—
C10H8 C14H10
дифенилметан
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() —СН— —CH2—CH2—
—СН— —CH2—CH2—
I
CH3 1,1-дифенилэтан 1,3-дифенилэтан (дибензил)
—CH=CH—
![]()
![]()

 симм-дифенилэтилен
симм-дифенилэтилен
![]()
![]() —CºC— CH
—CºC— CH
![]() ½
½
![]() дифенилацетилен
дифенилацетилен
трифенилметан
Номенклатура и изомерия.
В названиях гомологов бензола указывают наименования заместителей, соединенных с бензольным ядром, и, если требуется, их число. Простейшим в этом ряду является метилбензол С6Н5 –СН3; за ним следует этилбензол С6Н5-СН2-СН3. Т.к. в бензоле все водородные атомы равноценны, эти соединения, являющиеся его однозамещенными производными, не имеют изомеров, строение их можно представить формулами:
CH3 СН2—СН3

 ½ ½
½ ½
метилбензол этилбензол
(толуол)
В ряду ароматических углеводородов часто применяют тривиальные названия, например, метилбензол иначе называют толуолом.
По международной номенклатуре (правила ИЮПАК) все ароматические углеводороды объединяют названием – арены. Соответственно, их одновалентные остатки, образованные отнятием водорода от углеродных атомов ядра (одновалентные ароматические радикалы), называют арилами и обозначают - Ar. Остаток бензола – С6Н5 называется фенилом, строение его можно обозначить символом
![]()
![]()

 ½ ½
½ ½
![]()
![]()
![]() — (радикал фенил)
— (радикал фенил)
![]() ;
;
или
Ациклические (жирные) остатки, соединенные с бензольным ядром, называют боковыми цепями.
Этилбензолу изомерны двухзамещенные гомологи бензола, содержащие в соединении с ароматическим ядром два метильных остатка (заместителя) С6Н5(СН3)2. Они называются диметилбензолами или ксилолами.
Если в бензоле имеется не один, а несколько заместителей, то для обозначения их положения углеродные атомы ядра нумеруют. Взаимное расположение двух заместителей (Х) в ядре бензола обозначают специальными символами: 1,2-(или, что то же, 1,6-) положение, т.е. когда заместители находятся рядом (при соседних углеродах), называют орто – (или сокращенно О-) положением; 1,3-(или, что то же, 1,5-) положение, т.е. когда заместители расположены через один углерод друг от друга, называют мета-(или м-) положением; наконец, 1,4-положение, когда заместители расположены друг от друга через два углерода, называют пара (или п-) положением:
Х Х Х


 ½1 ½1 ½1
½1 ½1 ½1
![]()
![]()
![]()
![]() 6 2 Х 6 2 6 2
6 2 Х 6 2 6 2
![]() 5 3 5 3 5 3
5 3 5 3 5 3
![]() 4 4 Х 4
4 4 Х 4
Х
орто- мета- пара-
Таким образом, двухзамещенные производные бензола существуют в виде трех изомеров. В частности, в виде трех изомеров существуют и диметилбензолы (ксилолы); они имеют следующее строение и названия:
1) СН3 2) СН3 3) СН3 1) 1,2-диметилбенол; о-диме-


 ½1 ½1 ½1 тилбензол; о-ксилол.
½1 ½1 ½1 тилбензол; о-ксилол.
![]()
![]()
![]()
![]() 6 2 СН3 6 2 6 2 2) 1,3-диметилбензол; м-ди-
6 2 СН3 6 2 6 2 2) 1,3-диметилбензол; м-ди-
![]() 5 3 5 3 5 3 метилбензол; м-ксилол.
5 3 5 3 5 3 метилбензол; м-ксилол.
![]() 4 4 СН3 4 3) 1,4-диметилбензол; п-ди-
4 4 СН3 4 3) 1,4-диметилбензол; п-ди-
СН3 метилбензол; п-ксилол.
Очевидно, что для гомологов бензола возможны заместители двух типов: образованные отнятием водорода от углеродного атомов бензольного ядра (собственно арилы), либо от атомов углерода боковой цепи. Так, из толуола СН3—С6Н5 за счет бензольного ядра образуетсяся остаток толил СН3—С6Н4—, а за счет боковой метильной группы – бензил С6Н5—СН2—. При этом в бензольном ядре водород может быть отнят от углерода в орто-, мета- и пара- положении к метильной группе; таким образом, толилов может быть три:
СН3 СН3 СН3

![]()
![]()

 ½1 ½1 ½1
½1 ½1 ½1
![]()
![]()
![]()
![]() 6 2 6 2 6 2 —СН2—
6 2 6 2 6 2 —СН2—
![]() 5 3 5 3 5 3
5 3 5 3 5 3
![]() 4 4 4
4 4 4
о-толил м-толил п-толил бензил
Двухвалентные остатки ароматических углеводородов объединяют названием арилены. Для бензола возможны три двухвалентных радикала ¾С6Н4—, называемых фениленами:


 ½1 ½1 ½1
½1 ½1 ½1
![]()
![]()
![]()
![]() 6 2 6 2 6 2
6 2 6 2 6 2
![]() 5 3 5 3 5 3
5 3 5 3 5 3
![]() 4 4 4
4 4 4
о-фенилен м-фенилен п-фенилен
Физические свойства.
Бензол и его простейшие гомологи – бесцветные жидкости с характерными запахами, не смешивающиеся с водой. Некоторые высшие гомологи – твердые вещества. Температуры кипения и плавления ароматических углеводородов зависят от величины и изомерии боковых целей, а также от взаимного положения их в бензольном ядре.
Химические свойства
Как уже было указано, бензол, несмотря на то, что по составу он является ненасыщенным соединением, проявляет склонность преимущественно к реакциям замещения, и бензольное ядро очень устойчиво. В этом заключаются свойства бензола, которые называют ароматическими свойствами. Последние характерны и для других ароматических соединений; однако различные заместители в бензольном ядре влияют на его устойчивость и реакционную способность; в свою очередь бензольное ядро оказывает влияние на реакционную способность соединенных с ним заместителей. Рассмотрим следующие группы реакций ароматических углеводородов: а) реакции замещения, б) реакции присоединения и в) действие окислителей.
Реакции замещения
Галогенирование.
В обычных условиях ароматические углеводороды практически не реагируют с галогенами; как уже было указано, чистый бензол не обесцвечивают бромной воды, но в присутствии катализаторов (чаще всего применяют железо в виде очищенных стружек, опилок и т.д.) в безводной среде хлор и бром энергично вступают в реакцию с бензолом при комнатной температуре. При этом атомы галогена замещают атомы водорода бензольного ядра с образованием галогенпроизводных и галогенводорода. Например, реакция хлорирования бензола протекает следующим образом:
![]()
![]()
![]()
![]()
![]() Cl
Cl
+ Сl2 ¾¾¾® + HCl
Fe; FeCl3
бензол хлорбензол
Гомологи бензола при обычной температуре и в присутствии катализатора реагируют с галогенами аналогично, образуя галогенпроизводные с галогеном в бензольном ядре; если же вести реакцию при нагревании в отсутствие катализатора, то галоген замещает атом водорода лишь в боковой цепи. Например, при хлорировании толуола в присутствии катализатора образуется хлортолуол СН3—С6Н4—Cl, а при нагревании или освещении без катализатора – хлористый бензил С6Н5—СН2—Сl.
Действие азотной кислоты (реакция нитрования)
Реакция заключается в замещении атомов водорода в бензольном ядре остатками азотной кислоты – нитрогруппами (—NO2); в результате образуются ароматические нитросоединения и вода. Например:
![]()
![]()

![]()
![]() NO2
NO2
+ HO—NO2 ¾® + H2O
бензол нитробензол
Для реакции применяют концентрированная HNO3, часто в смеси с концентрированной H2SO4 (нитрующая смесь). Серная кислота играет роль катализатора и водоотнимающего средства.
Действие серной кислоты (реакция сульфирования)
Реакция заключается в замещении атомов водорода бензольного ядра остатками серной кислоты – сульфогруппами (¾SO2OH или, что то же ¾SO3H – катион гидросульфония); в результате образуется ароматические сульфокислоты. Например:
![]()
![]()
![]()
![]()
![]() t SO3H
t SO3H
+ НО—SO3H ¾¾® + H2O
Реакция происходит при нагревании под действием концентрированной H2SO4.
Направляющее влияние заместителей
(правила замещения в бензольном ядре)
В незамещенном бензоле реакционная способность всех шести атомов углерода в реакциях замещения одинакова; заместители могут становиться взамен водорода к любому углеродному атому. Если же в бензольном ядре уже имеется заместитель, то под его влиянием состояние ядра изменяется и положение, в которое вступает любой новый заместитель, зависит от природы первого заместителя. Из этого следует, что каждый заместитель в бензольном ядре проявляет определенное направляющее (ориентирующее) влияние и способствует введению новых заместителей лишь в определенные по отношению к себе положения.
По направляющему влиянию различные заместители подразделяют на две группы:
а) заместители I рода (электронодонорные – нуклеофильные). К ним относятся аминогруппы, гидроксильная группа, метил и др. алкилы, а также гологены, т.е. —NH2, —NHR, —NR2, —OH, —OR, —CH3, (и другие —R), —Cl, —Br, —J и др.
Заместители I рода направляют новый электрофильный заместитель в орто- и пара- положения по отношению к себе. При этом все они (за исключением галогенов) уменьшают устойчивость ароматической группировки и облегчают как реакции замещения, так и все другие реакции бензольного ядра. В содержащих заместители I рода производных бензола водородные атомы ядра замещаются с большей скоростью, чем в самом бензоле, и само бензольное ядро значительно теряет свою ароматическую устойчивость. Особенно активны как ориентанты I рода и активаторы бензольного ядра амино- и гидроксильные группы.
Отличительная особенность приведенных выше заместителей I рода – наличие в них только простых связей.
б) заместители II рода (электроноакцепторные – электрофильные) (—NO2, —SO3H, —COOH, —CO—, —CH=O, —COCl, —CONH2, —CºN и др.)
направляют новый электрофильный заместитель в мета-положение по отношению к себе. Они увеличивают устойчивость ароматической группировки и затрудняют реакции замещения.
В производных бензола, содержащих эти заместители, атомы водорода ядра замещаются с меньшей скоростью, чем в самом бензоле.
В свете электронных представлений направляющее влияние заместителей в бензольном ядре объясняют следующим образом. В незамещенном бензоле имеется равномерно распределенное облако шести π-электронов. Замещаться водород может у любого С-атома, т.к. электронная плотность у всех атомов бензольного кольца одинакова (схема 1):
1) 2) А 3) В
![]()
![]()
![]() ¯
¯
![]()
![]()
![]() d- о о d- d+ о о d+
d- о о d- d+ о о d+
м м
п d- п d+
Введение заместителей (I рода) нарушает равномерность облака π- электронов и вызывает перераспределение электронной плотности; при этом она изменяется преимущественно в орто- и пара- положении по отношению к заместителю (условно это можно обозначить как ![]() ).
).
Особенность заместителей I рода – они способны подавать электроны (электронодонорные заместители). Заместители II рода, наоборот, склонны оттягивать на себя (принимать) электроны (электронно-акцепторные заместители).
Подавая электроны к бензольному ядру, заместители I рода увеличивают его электронную плотность, которая особенно повышается в орто- и пара- положении по отношению к заместителю. В схеме 2 показано смещение электронной плотности под влиянием заместителя I рода (А). Электрофильные реагенты, несущие положительный заряд, направляются преимущественно к С-атомам, у которых электронная плотность повышена (относительно увеличен отрицательный частичный заряд, δ-) и поэтому замещают водород в орто- и пара- положениях к заместителю I рода.
Заместители II рода (В) вследствие их электронно-акцепторных свойств оттягивают на себя π-электроны бензольного ядра, уменьшая его электронную плотность, причем (схема 3) больше всего электронная плотность оттягивается от С-атомов в орто- и пара- положениях к заместителю; эти С-атомы становятся относительно более положительными (приобретают d+). Поэтому при наличии заместителя II рода электрофильные реагенты замещают водород преимущественно у С-атома в мета-положении, т.к. у них электронная плотность понижается в меньшей степени и они реакционноспособны.
Увеличение общей электронной плотности бензольного ядра под влиянием заместителей I рода повышает его реакционную способность, тогда как заместители II рода, уменьшая общую электронную плотность, понижают активность бензольного ядра в реакциях.
Разберем правила замещения на следующих примерах.
При нитровании бромбензола нитрогруппа замещает водород в орто- и в пара- положениях по отношению к брому, т.к. он является заместителем I рода, в результате получается смесь о-бромнитробензола и п-бромнитробензола, из которой можем выделить оба соединения:
![]()
![]()

![]() Br Br + H2O
Br Br + H2O
![]()
![]()
 ¾® NO2
¾® NO2
![]() + HO—NO2 ® о-бромнитробензол
+ HO—NO2 ® о-бромнитробензол
![]()
![]()
![]() Br
Br
бромбензол ¾¾¾¾¾® + H2O
![]() NO2
NO2
п-бромнитробензол
Если же взять нитробензол и подвергнуть его бромированию, то также будет получаться бромнитробензол, но уже мета-изомер, поскольку нитрогруппа – заместитель II рода, и направляет бром по отношению к себе в мета-положение:
![]()
![]() NO2 NO2
NO2 NO2
 | |||
 | |||
![]()
![]() + Br2 ¾® + HBr
+ Br2 ¾® + HBr
![]() Br
Br
нитробензол м-бромнитробензол
Следует иметь в виду, что почти во всех реакциях, несмотря на наличие в бензольном ядре заместителей I рода, образующиеся орто- и пара- замещенные являются главными, но не единственными продуктами. Наряду с н
Категории:
- Астрономии
- Банковскому делу
- ОБЖ
- Биологии
- Бухучету и аудиту
- Военному делу
- Географии
- Праву
- Гражданскому праву
- Иностранным языкам
- Истории
- Коммуникации и связи
- Информатике
- Культурологии
- Литературе
- Маркетингу
- Математике
- Медицине
- Международным отношениям
- Менеджменту
- Педагогике
- Политологии
- Психологии
- Радиоэлектронике
- Религии и мифологии
- Сельскому хозяйству
- Социологии
- Строительству
- Технике
- Транспорту
- Туризму
- Физике
- Физкультуре
- Философии
- Химии
- Экологии
- Экономике
- Кулинарии
Подобное:
- Современная химия
Рождение современной химии ...нет науки, которая была бы замечательнее и поучительнее истории химии. Юстус фон Либих Введение Представле
- Одно и многоатомные спирты. Простые эфиры
С.Ю. ЕлисеевОбщая классификация спиртов. Предельные одноатомные спирты, их гомологический ряд, общая формула, изомерия, номенклатура. Фи
- Морфофункциональный анализ стелющейся колонии у гидроидов на примере cordylophora inkermanica marfenin
(athecata, clavidae)Гидроид приспособлен к обитанию на .“мозаичном” субстрате (зостера, мидии) и специализирован на питании зоопланктоном. Прим
- Редкие и исчезающие птицы Ставропольского края
- Белки
- Птицы Камчатки
В настоящее время на Камчатке насчитывается более 240 видов птиц, принадлежащих к 17 отрядам и 40 семействам.Наиболее полно представлены во
- Кораллы: разнообразие и значение
 referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.
referat-web.com Бесплатно скачать - рефераты, курсовые, контрольные. Большая база работ.

